Ход работы. 1. Обнаружение в молекулах белков пептидных связей (биуретовая реакция)1. Обнаружение в молекулах белков пептидных связей (биуретовая реакция). К 1-2 мл разбавленного раствора белка прибавляют двойной объем 30%-ного раствора гидроксида натрия, хорошо перемешивают и добавляют 2-3 капли 1%-ного раствора сульфата меди. Снова тщательно перемешивают. Развивается сине-фиолетовое окрашивание. При малом содержании белка чувствительность реакции можно повысить, наслаивая на раствор белка в щелочи 1 мл 1%-ного раствора сульфата меди. При стоянии на границе двух слоев появляется фиолетовое кольцо. Реакция названа биуретовой потому, что аналогичную цветную реакцию дает биурет, легко получаемый из мочевины при ее нагревании при температуре 150 - 1600С.
Биурет в щелочной среде претерпевает енолизацию по схеме:
Две молекулы биурета в енольной форме взаимодействуют с гидроксидом меди (II) с образованием комплексного соединения меди:
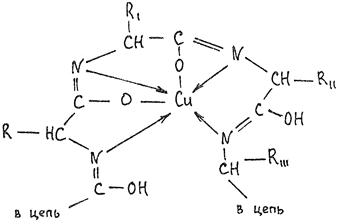
Аналогично построено комплексное соединение меди с енолизированными пептидными группами любого белка:
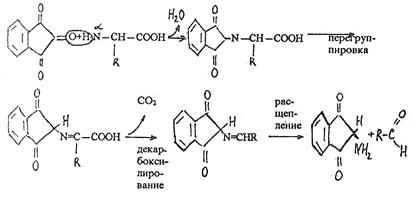
2. Нингидриновая реакция К 2 - 3 мл разбавленного белка приливают 3 - 4 капли 1%-ного раствора нингидрина в 95%-ном ацетоне. Раствор перемешивают и ставят в водяную баню при 700С на несколько минут. Появляется сине-фиолетовое окрашивание. Сначала в результате взаимодействия a-аминогруппы аминокислоты (или белка) с нингидрином возникает Шиффово основание. Затем оно претерпевает перегруппировку, декарбоксилируется и расщепляется на альдегид и аминодикетогидринден.
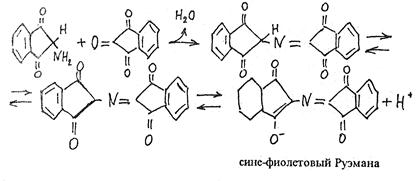
Аминодикетогидринден конденсируется еще с одной молекулой нингидрина, и образовавшееся соединение, енолизируясь, переходит в окрашенную форму, получившую название " сине-фиолетовый Руэмана" - по имени исследователя, впервые в 1910 г. изучившего эту реакцию.
В присутствии органических растворителей (ацетона, этанола, пиридина и др.), на которых обычно готовят раствор нингидрина, протекает реакция:
Продукт этой реакции содержит в своем составе радикал (R) исходной аминокислоты, который обусловливает различную окраску (голубую, красную и т.п.) соединений, возникших при реакции аминокислот с нингидрином. В настоящее время нингидриновая реакция широко используется как для открытия отдельных аминокислот, так и для определения их количеств.
3. Ксантопротеиновая реакция. К 1 мл разбавленного белка добавляют 5-6 капель концентрированной азотной кислоты до появления белого осадка или мути от свернувшегося белка. При нагревании раствор и осадок окрашиваются в ярко-желтый цвет. При этом осадок почти полностью растворяется. Охлаждают смесь и осторожно добавляют к раствору, имеюще-му кислую реакцию, не взбалтывая, по каплям избыток щелочи до щелочной реакции. Выпадающий вначале осадок кислотного альбумината растворяется, и жидкость окрашивается в ярко-оранжевый цвет. Ксантопротеиновая реакция происходит только при наличии в белках остатков ароматических аминокислот (фенилаланина, тирозина и триптофана). Желатин, не содержащий ароматических аминокислот, не дает ксантопротеиновой пробы. В результате реакции нитрования по радикалам ароматических аминокислот образуются желтоокрашенные нитросоединения. Изменение желтой окраски на оранжевую в щелочной среде обусловлено появлением хромофорной группы. Рассмотрим в качестве примера механизм ксантопротеиновой реакции по радикалу тирозина:
4. Реакция Сакагучи. Берут в пробирку 2 мл разбавленного раствора белка, добавляют 1 мл 10%-ного раствора гидроксида натрия и вслед за этим несколько капель 0, 2%-ного спиртового раствора 1-нафтола. Перемешивают, доливая 0, 5 мл раствора гипобромида натрия и вновь перемешивают. Развивается оранжево-красное окрашивание. Появление окраски объясняется взаимодействием 1-нафтола в присутствии окислителя с гуанидиновыми группировками радикалов аргинина. Хотя механизм реакции еще полностью не выяснен, ряд наблюдений свидетельствует в пользу следующей схемы. Сначала 1-нафтол в присутствии окислителя соединяется с гуанидиновой группировкой аргинина:
Затем при дальнейшем окислении нафтиларгинина образуется соединения типа хинонимина:
Так как производные хинониминов (в данном случае нафтохинонимина), у которых водород иминогруппы замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона, то, по-видимому, оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именного производного нафтохинонимина. Не исключена, однако, вероятность образования еще более сложного соединения за счет дальнейшего окисления NH-групп гуанидинового остатка и бензольного ядра 1-нафтола.
5. Реакция Адамкевича. Наливают в пробирку несколько капель неразбавленного белка и прибавляют 2 мл уксусной кислоты, к которой добавляют немного глиоксиловой кислоты. Смесь слегка нагревают до растворения образующегося осадка. Охлаждают пробирку со смесью, а затем, сильно наклонив ее, осторожно, по стенке приливают 1 мл концентрированной серной кислоты так, чтобы обе жидкости не смешивались. При стоянии на границе двух жидкостей получается красно-фиолетовое кольцо. Окраска возникает за счет реакции триптофана с глиоксиловой кислотой, всегда присутствующей в уксусной кислоте в виде примеси. Триптофан в этой реакции конденсируется с формальдегидом, выделяющимся из глиоксиловой кислоты под воздействием концентрированной серной кислоты:
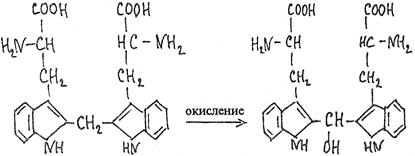
Продукт конденсации окисляется до бис-2-триптофанилкарбинола:
Последний в присутствии минеральных кислот образует окрашенные в сине-фиолетовый цвет соли (явление галохромии).
6. Реакция Паули. К 1 мл 1%-ного раствора сульфаниловой кислоты в 5%-ном растворе соляной кислоты приливают 2 мл 0, 5%-ного раствора нитрита натрия, сильно встряхнув, быстро добавляют сначала 2 мл разбавленного раствора белка, а затем, после перемешивания содержимого, 6 мл 10%-ного раствора карбоната натрия. После смешивания растворов развивается вишнево-красное окрашивание. Возникновение окраски обусловлено наличием в белковой молекуле остатков гистидина и тирозина. При взаимодействии кислого раствора сульфаниловой кислоты с нитритом натрия осуществляется реакция диазотирования и образуется диазобензолсульфоновая кислота
сульфаниловая n-сульфабензолдиазонит кислота (диазобензолсульфоновая кислота) При реакции последней с гистидином образуется соединение вишнево-красного цвета:
2, 5-бис-n-сульфобензол-
7. Реакция “на слабосвязанную серу”. В пробирку наливают 0, 5 - 1, 0 мл неразбавленного белка, добавляют двойной объем концентрированного раствора щелочи, кладут несколько “кипятильников” и кипятят смесь (осторожно, жидкость может выбросить!). При этом выделяется аммиак, который может быть обнаружен по запаху и посинению лакмусовой бумажки, поднесенной к отверстию пробирки (не касаться стенки!). Образующийся незначительный осадок растворяется при кипячении. К горячей щелочной жидкости приливают раствор плюмбита натрия, образуется черный осадок. Под действием щелочи наблюдается отщепление части аминогрупп (реакция дезаминирования) в виде аммиака. В щелочной среде происходит также постепенное отщепление ионов серы со степенью окисления +2 от радикалов аминокислот, содержащих серу. Образование ионов серы можно обнаружить с помощью ионов свинца, образующих с ионами серы черный нерастворимый осадок сульфида свинца:
Na2S + Na2PbO2 + 2H2O ® PbS¯ + 4NaOH. плюмбит натрия
Работа 4. Выделение рибонуклеопротеинов из дрожжей и качественное определение
Нуклеопротеины – сложные белки, простетической группой которых являются нуклеиновые кислоты – ДНК или РНК. В дезоксирибонуклеопротеинах (ДРНП) и рибонуклеопротеинах (РНП) нуклеиновые кислоты и белки связаны друг с другом в основном солевыми связями, которые могут легко диссоциировать, что и происходит достаточно часто в процессе выделения ДРНП и РНП, особенно в момент воздействия крепких растворов солей. Выделение нуклеопротеинов можно осуществить различными методами: 1) извлечением дистиллированной водой с последующим осаждением нуклеопротеина уксусной кислотой; 2) экстракцией слабым раствором (0, 2 - 0, 4%) щелочи с последующим действием уксусной кислоты; 3) экстракцией растворами хлорида натрия средних концентраций, из которых нуклеопротеины выпадают при разбавлении раствора; 4) последовательным извлечением различных нуклеопротеинов сначала 0, 15 М раствором хлорида натрия, затем 1 М его раствором и, наконец, 0, 27%-ным раствором гидроксида натрия; 5) ультрацентрифугированием в градиенте плотности сахарозы или хлорида цезия; 6) фильтрованием через гель сефадекса. Оборудование, реактивы: центрифуга, колба круглодонная на 100 мл с обратным прямым воздушным холодильником, ступка (диаметр 110 мм), стакан стеклянный на 200 мл, цилиндр мерный на 50 мл, воронка стеклянная, пробирки химические, песок промытый и прокаленный, гидроксид натрия (0, 4%-ный), уксусная кислота (10%-ная), соляная кислота (конц.), сульфат меди (1%-ный), орциновый реактив, аммиак (конц.), аммиачный раствор оксида серебра, молибдат аммония, диэтиловый эфир, серная кислота (10%-ная). Материал: дрожжи пекарские (высушенные).
|