Электролитическая диссоциация. В зависимости от характера химической связи в веществе оно может переходить в жидкий растворитель в виде атомов
В зависимости от характера химической связи в веществе оно может переходить в жидкий растворитель в виде атомов, молекул или ионов. В растворителе эти частицы подвергаются сольватации (гидратации). Дальнейшая судьба сольватированных молекул и ионов может быть различной. Молекулы могут диссоциировать на ионы, а ионы рекомбинировать с образованием молекул. Если перешедшие в жидкость молекулы растворяемого вещества и молекулы (частицы) растворителя полярны, то сольватированные молекулы растворяемого вещества в результате взаимодействия с молекулами растворителя с большой вероятностью диссоциируют на положительные и отрицательные ионы (катионы и анионы соответственно): АВ ® A + + B -. Наличие ионов в растворе делает его электропроводящим, т. е. электролитом. Поэтому такой процесс образования ионов в растворе называется электролитической диссоциацией. В дальнейшем будем называть ее просто диссоциацией. Большая часть водных растворов неорганических веществ с ионным или ковалентным полярным типом связи (основания, кислоты, соли) является электролитами. Если ионов в растворе нет, то он не проводит электрический ток и является неэлектролитом. Примером могут служить растворы, образованные неполярными органическими и неорганическими молекулами, такие как раствор бензола в толуоле, сахара в воде и т.д. Наличие в растворе противоположно заряженных ионов, независимо от способа их образования, обусловливает вероятность их рекомбинации (ассоциации) с образованием молекул: A + + B - ® AB. Таким образом, процесс электролитической диссоциации является обратимым. Скорости диссоциации и рекомбинации зависят от концентрации частиц и их природы. Отметим, что для простоты мы рассматриваем молекулы и ионы как частицы, не имеющие сольватной оболочки. В реальных условиях сольватная оболочка влияет на скорости процессов. В результате в растворе установится состояние динамического равновесия, при котором скорости диссоциации и рекомбинации равны и определенная часть растворенного вещества будет находиться в виде ионов, а оставшееся количество – в виде молекул. Равновесие, в зависимости от концентрации и природы веществ, может быть сдвинуто в сторону либо диссоциации, либо рекомбинации. Таким образом, в одних растворах будут преобладать ионы, а в других – молекулы. Соотношение количеств растворенного вещества, находящегося в виде ионов и в виде молекул, характеризуется степенью диссоциации. Степень диссоциации (a) будет равна отношению числа молекул, находящихся в растворе в виде ионов (N д), к общему числу молекул растворенного вещества (N 0). Она равна соответственно отношению их молярных концентраций (С ди С 0):
Степень диссоциации часто выражается в процентах. В зависимости от величины степени диссоциации электролиты условно делятся на сильные (a > 50%), слабые, (a < 5%) и средние (5% < a < 50%). Деление весьма условно, так как степень диссоциации сильно зависит от концентрации растворенного вещества. Для состояния равновесия существует константа равновесия, которая в данном случае называется константой диссоциации (К д). Пусть реакция диссоциации описывается уравнением AB Û A + + B -. Тогда выражение для константы диссоциации имеет вид
где [ A +], [ B -], [ AB ] – равновесные молярные концентрации соответствующих частиц. Для учета неидеальности реальных растворов вместо концентраций соответствующих частиц в выражении константы равновесия используются их активности аi =g i× Сi, где g i – коэффициент активности. Отметим, что для оценочных расчетов равновесия разбавленных растворов можно принять g i× = 1. В случае растворов электролитов величина коэффициента активности может значительно отличаться от единицы (табл.3.2).
Таблица 3.2 Средние ионные коэффициенты активности g± сильных электролитов в водных растворах при Т 0=298 К
На практике для оценки активности ионов пользуются средним значением активностей (а ±) и коэффициентов активности (g±) ионов данного электролита: а ± = g±× m ±, m ± = где m ± – средняя ионная моляльная концентрация; С м – моляльная концентрация растворенного вещества (число молей растворенного вещества содержащихся в 1 кг растворителя); n+, n- – число катионов и анионов в молекуле электролита, n =n+ + n-. Средние ионные коэффициенты активности g±, приведены в справочной литературе. Величину коэффициентов активности в разбавленных растворах также, согласно теории ионных растворов Дебая-Хюккеля (Debye, Hü ckel), можно рассчитать по ионной силе раствора (I):
где С м i – моляльная концентрация и Zi – заряд i -го иона в растворе. Для разбавленных водных растворов при Т 0=298 К коэффициент активности ионов может быть аппроксимирован выражением
Поскольку равновесие в растворе может быть описано как степенью, так и константой диссоциации, то они должны быть связаны между собой. Отметим, что величина К дне зависит, а величина a зависит от концентрации растворенного вещества. Согласно уравнению реакции, концентрации катионов и анионов равны между собой и соответственно равны концентрации вещества, находящегося в растворе в виде ионов: [ A +] = [ B -] = C д. Тогда концентрация вещества АВ, находящегося в недиссоциированной форме, [ AB ] = C 0– C д. Поскольку a = С д/ С 0, то С д=a× C 0 и
Величины К д для различных электролитов лежат в широких пределах, например, для HNO2 К д=6, 9× 10-4, а для HCl К д=1× 107. Если К д® 0, то a ® 0. В этом случае a < < 1 и K д»a2× C 0. Тогда a» Если молекула электролита содержит несколько однотипных ионов, то ее диссоциация протекает ступенчато, например: A 2 B Û A + + АB - AB - Û A + + B 2- Каждая ступень характеризуется своим значением константы диссоциации (К д1, К д2). При расчете состава раствора необходимо учитывать диссоциацию по обеим ступеням.
|

 .
. ,
,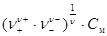 ,
, ,
, .
. .
. . Поскольку K д – величина постоянная, то степень диссоциации растет с уменьшением концентрации растворенного вещества. Эта зависимость известна как закон разбавления Оствальда. С увеличением константы диссоциации соответственно увеличивается степень диссоциации и для сильных электролитов a ® 1.
. Поскольку K д – величина постоянная, то степень диссоциации растет с уменьшением концентрации растворенного вещества. Эта зависимость известна как закон разбавления Оствальда. С увеличением константы диссоциации соответственно увеличивается степень диссоциации и для сильных электролитов a ® 1. ,
, .
.


