Химические свойства. В молекуле бензола каждый из шести атомов углерода, находящийся в состоянии sp2-гибридизации, располагается под углом 1200 друг к другуВ молекуле бензола каждый из шести атомов углерода, находящийся в состоянии sp2 -гибридизации, располагается под углом 1200 друг к другу, а вместе они образуют плоское шестичленное кольцо. Негибридизированные р -электроны располагаются перпендикулярно к плоскости бензольного кольца и равномерно перекрываются друг с другом над и под этой плоскостью. В результате образуется единая замкнутая система нелокализованных π -электронов и происходит «выравнивание» одинарных и двойных связей, т.е. в молекуле бензола отсутствуют классические двойные и одинарные связи. Поэтому для бензола и его гомологов не типичны реакции присоединения и окисления. Для ароматических углеводородов характерны реакции электрофильного замещения водорода на другие атомы или группы атомов. 1. Реакции электрофильного замещения. К ним относятся реакции галогенирования, нитрования, сульфирования, алкилирования и др. а) Галогенирование: C6H6 + Br2 бензол бромбензол б) Нитрование: С6Н6 + HNO3 нитробензол в) Алкилирование: C6H6 + CH3Cl метилбензол (толуол) C6H6 + CH2=CH2 этилбензол 2. Реакции присоединения. Эти реакции протекают с большим трудом. Только в особых условиях (высокая температура, облучение УФ светом, катализатор) бензол может проявлять слабо выраженный непредельный характер и присоединять водород или галогены: С6Н6 + 3Н2
+ 3Н2
бензол циклогексан
+ 3Cl2
бензол гексахлорциклогексан
|

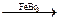 C6H5− Br + HBr
C6H5− Br + HBr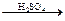 C6H5− NO2 + H2O
C6H5− NO2 + H2O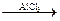 C6H5− CН3+ HCl
C6H5− CН3+ HCl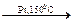 С6Н12
С6Н12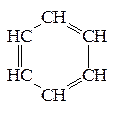
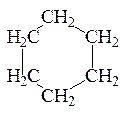
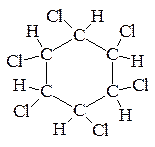 С6Н6 + 3Cl2
С6Н6 + 3Cl2  C6H6Cl6
C6H6Cl6


