Данные для построения градуировочных графиков
Для построения градуировочных графиков и проведения анализа последовательно проводят две серии измерений с соответствующими светофильтрами. Сначала устанавливают светофильтр, выделяющий характеристическую линию Na. Настраивают пламенный фотометр на работу в необходимом диапазоне концентраций в соответствии с инструкцией к прибору, используя дистиллированную воду и градуировочный раствор с максимальной концентрацией натрия. Затем фотометрируют все пять стандартных растворов в порядке увеличения концентраций и анализируемый раствор, промывая капилляр дистиллированной водой после введения каждого раствора. Переключают светофильтр на характеристическую линию K и повторяют операции по настройке прибора на рабочий диапазон концентраций, используя дистиллированную воду и градуировочный раствор с максимальной концентрацией калия. Проводят фотометрирование стандартных растворов и анализируемого раствора со светофильтром для определения K. Проводят обработку результатов измерений методом наименьших квадратов, желательно с использованием ПК. По результатам измерений строят градуировочные графики в координатах i (Na+), усл. ед. – С (NaCl), моль/л и i (K+), усл. ед. – С (KCl), моль/л. По графикам определяют концентрации (моль/л) натрия и калия в анализируемом растворе и рассчитывают массу Na+ и K+ (г) в пробе.Вариант 2. Метод ограничивающих растворов Сущность работы. Для выполнения анализа методом ограничивающих растворов (методом двух стандартов) готовят серию стандартных растворов и измеряют величины силы фототока i этих растворов и пробы в одинаковых условиях. Затем выбирают два стандартных раствора – «ограничивающие растворы» – так, чтобы С 1 < Сx < С 2 и i 1 < ix < i 2. (9.1) Расчет неизвестной концентрации проводят по формуле
Для получения точных результатов необходимо использовать рабочую область концентраций, в пределах которой выполняется линейная зависимость между величиной фототока и концентрацией элемента в растворе. Поэтому предварительно с помощью эталонов должна быть проверена эта зависимость и выбрана рабочая область концентраций. Выполнение работы. Готовят пять эталонных растворов и фотометрируют их, как описано в варианте 1. Проводят обработку результатов измерений методом наименьших квадратов, желательно с использованием ПК. Строят графики в координатах i (Na+), усл. ед. – С (NaCl), моль/л и i (K+), усл. ед. – С (KCl), моль/л. Проверяют линейную зависимость между силой фототока и концентрациями натрия и калия. Получают в мерную колбу вместимостью 100, 0 мл анализируемый раствор, который разбавляют водой до метки. Фотометрируют испытуемый раствор в тех же условиях, что и эталонные растворы, и подбирают из эталонного ряда два ограничивающих раствора согласно условию (9.1). Трижды фотометрируют три раствора (два эталонных и испытуемый) и берут средний результат из трех полученных отсчетов. Неизвестную концентрацию определяют по формуле (9.2). Вариант 3. Метод одного стандарта Сущность работы. Для проведения анализа готовят один стандартный раствор с концентрацией определяемого вещества С ст, затем измеряют величины фототока этого раствора (i ст) и пробы (iх) в одинаковых условиях. Поскольку iх = kCх и i ст = kC ст, то
Следовательно, неизвестную концентрацию можно рассчитать по формуле
Метод стандартов применим только в случае соблюдения линейной зависимости между величиной фототока и концентрацией определяемого элемента, которую необходимо предварительно проверить. Выполнение работы. Готовят пять эталонных растворов и фотометрируют их, как описано в варианте 1. Проводят обработку результатов измерений методом наименьших квадратов, желательно с использованием ПК. Строят графики в координатах i (Na+), усл. ед. – С (NaCl), моль/л и i (K+), усл. ед. – С (KCl), моль/л. Проверяют линейную зависимость между силой фототока и концентрациями натрия и калия. Получают в мерную колбу вместимостью 100, 0 мл анализируемый раствор, который разбавляют водой до метки. Фотометрируют испытуемый раствор в тех же условиях, что и эталонные растворы, и подбирают из эталонного ряда стандартный раствор. Трижды фотометрируют выбранный стандартный раствор и анализируемый раствор и берут средний результат из трех полученных отсчетов. Неизвестную концентрацию определяют по формуле (9.3). Вариант 4. Метод серии добавок
Рис. 9.1. Определение неизвестной концентрации методом серии добавок
Метод добавок можно применять только в том случае, когда зависимость сигнала от концентрации является линейной, что необходимо проверить предварительно путем фотометрирования серии стандартных растворов. Чаще всего метод добавок используют при анализе проб сложного состава, так как прирост аналитического сигнала при добавке стандартного раствора связан только с определяемым компонентом, а сигналы от мешающих компонентов пробы остаются постоянными. Водопроводная вода имеет сложный катионный и анионный состав, поэтому при проведении анализа с использованием методов градуировочного графика или стандартов возможны ошибки из-за влияния посторонних элементов на излучение определяемого за счет различного химического состава анализируемой пробы и эталонных растворов. Если же для определения натрия и калия в водопроводной воде воспользоваться методом добавок, то состав пробы не окажет влияния на результаты анализа. Выполнение работы 1. Проверка линейности зависимости i – C. При определении концентрации натрия и калия в водопроводной воде методом добавок следует предварительно убедиться в линейности зависимости аналитического сигнала от концентрации. Стандартные растворы готовят в соответствии с данными табл. 4. Таблица 4
|

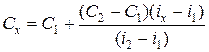 . (9.2)
. (9.2) .
. . (9.3)
. (9.3) Сущность работы. Для проведения анализа измеряют величины фототока пробы и нескольких растворов той же пробы с добавками стандартных растворов натрия и калия при двух светофильтрах. Строят два графика в координатах i – C добавки и по ним находят Сх как величину отрезка, отсекаемого прямой на оси абсцисс (рис. 9.1).
Сущность работы. Для проведения анализа измеряют величины фототока пробы и нескольких растворов той же пробы с добавками стандартных растворов натрия и калия при двух светофильтрах. Строят два графика в координатах i – C добавки и по ним находят Сх как величину отрезка, отсекаемого прямой на оси абсцисс (рис. 9.1).



