Лабораторная работа № 7. Цель работы: провести опыты, подтверждающие способность различных типов солей к гидролизуГИДРОЛИЗ СОЛЕЙ Цель работы: провести опыты, подтверждающие способность различных типов солей к гидролизу. Определить рН растворов этих солей. Сделать вывод о влиянии различных факторов на степень гидролиза. Гидролизом называют реакцию обмена между водой и ионами соли, приводящую к образованию слабого электролита. В результате гидролиза смещается равновесие электролитической диссоциации воды:
Раствор будет нейтральным, когда концентрации [ H+ ] и [ OH- ] будут равны: [ H+ ] = [ OH- ] = Для характеристики кислотности (щелочности) среды введен специальный параметр – водородный показатель, или рН: pH где a – степень диссоциации, С – молярная концентрация. В нейтральной среде рН = 7, кислой – рН < 7, щелочной – рН > 7. Концентрация Точное значение рН растворов определяется на приборах рН-метрах, а приблизительное – с помощью универсального индикатора. В результате гидролиза солей в растворе появляется избыточное количество ионов [ H+ ] или [ OH– ] и рН изменяется. 1. Гидролизу не подвергаются соли, образованные сильными основаниями и сильными кислотами. Например, KCl, Na 2 SO 4. 2. Гидролиз соли, образованной сильным основанием и слабой кислотой, протекает по аниону, ионы водорода связываются анионом соли, образуя слабую кислоту. В растворе накапливаются гидроксид-ионы, что обеспечивает щелочную реакцию раствора (рН > 7). Число ступеней гидролиза определяется зарядом аниона. Например, гидролиз ортофосфата натрия, Na 3 PO 4, может быть представлен уравнениями:
3. Гидролиз соли, образованной слабым основанием и сильной кислотой, протекает по катиону. В растворе происходит связывание гидроксид-ионов катионами соли с образованием слабого основания, в результате накапливаются ионы водорода, и раствор приобретает кислую реакцию (рН < 7). Число ступеней гидролиза определяется зарядом катиона. Например, гидролиз хлорида меди, CuCl 2:
4. Гидролиз соли, образованной слабым основанием и слабой кислотой, протекает до конца, как по катиону, так и по аниону. NH 4 CN + H 2 O = NH 4 OH + HCN; NH 4 + + CN– + H 2 O = NH 4 OH + HCN. Характер среды в подобных случаях зависит от относительной силы кислоты и основания, образующих соль. Если они одинаковы по силе, то реакция среды нейтральна, если образующая кислота сильнее основания – реакция будет слабокислой, слабощелочной она будет, если основание сильнее кислоты. Гидролиз – процесс обратимый. Однако, если в результате гидролиза образуются малорастворимые либо газообразные продукты, то гидролиз протекает практически до конца. Это имеет место в случае совместного гидролиза двух солей, одна из которых гидролизуется по катиону, другая – по аниону. При этом образующиеся в результате ионы H+ и ОH– будут нейтрализовать друг друга, что вызовет усиление гидролиза обеих солей. Результат – образование конечных продуктов гидролиза. Поэтому при взаимодействии растворов солей алюминия, хрома, железа (III) с растворами карбонатов, сульфидов в осадок выпадают не карбонаты и сульфиды этих катионов, а соответствующие гидроксиды. Например: 2 FeCl 3 + 3 Na 2 S + 6 H 2 O = 2 Fe (OH)3¯ + 3 H 2 S + 6 NaCl; 2 Fe 3+ + 3 S 2– + 6 H 2 O = 2 Fe (OH)3¯ + 3 H2S . Процесс гидролиза может быть количественно охарактеризован с помощью двух величин: степени гидролиза h и константы гидролиза КГ. Степенью гидролиза называется отношение числа молекул, подвергшихся гидролизу, к общему числу растворенных молекул:
Степень гидролиза зависит от следующих факторов: природы соли, ее концентрации, температуры раствора. Степень гидролиза возрастает с увеличением температуры, уменьшением концентрации соли, уменьшением константы диссоциации кислоты или основания, образующих соль. Константа гидролиза определяет состояние химического равновесия в растворе гидролизованной соли. Для солей, гидролизующихся по катиону по катиону и аниону Таким образом, количественно подтверждается сделанный ранее вывод: чем более слабый электролит образуется в результате гидролиза, тем полнее протекает гидролиз. Экспериментальная часть
|

 ,
, = 10–7 моль/л, где КВ = 10-14 моль2/л2 – константа воды, или ионное произведение воды.
= 10–7 моль/л, где КВ = 10-14 моль2/л2 – константа воды, или ионное произведение воды. ; [ H+ ] = a× С,
; [ H+ ] = a× С, .
. сокращенные
сокращенные
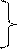 первая ступень
первая ступень
 , которая выражается в долях единиц или процентах.
, которая выражается в долях единиц или процентах. , по аниону
, по аниону  ,
, .
.


