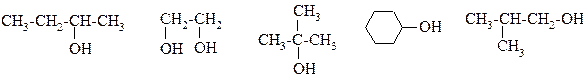Занятие № 4ХИМИЧЕСКИЕ СВОЙСТВА ГАЛОГЕНАЛКАНОВ, СПИРТОВ И ФЕНОЛОВ Мотивация цели. Функциональная группа спиртов и фенолов – гидроксильная группа – является фрагментом многих лекарственных соединений, а также таких биологически важных соединений, как оксикислоты, углеводы, белки. Поэтому важно изучить химические свойства спиртов и фенолов. Галогенпроизводные алканов являются исходными соединениями в синтезе спиртов, аминов и других соединений. Цель самоподготовки. Необходимо усвоить реакционную способность спиртов и фенолов в реакциях нуклеофильного замещения, их кислотно-основные свойства, а также нуклеофильные свойства в реакциях ацилирования и алкилирования. План изучения темы 1. Изомерия, номенклатура и химические свойства галогеналканов (Самостоятельная работа № 2). 2. Спирты – определение, классификация в зависимости от числа гидроксильных групп и от характера атома углерода, с которым связана гидроксильная группа. 3. Реакционные центры в молекулах спиртов. 4. Кислотные и основные свойства спиртов. Сравнение кислотных свойств одно- и многоатомных спиртов. Качественная реакция на многоатомные спирты. 5. Реакции нуклеофильного замещения в спиртах. Получение галогеналканов. Условия и механизм реакции. Реакция межмолекулярной дегидратации (получение простых эфиров). Условия и механизм реакции. Роль концентрированной серной кислоты. 6. Реакции элиминирования. Внутримолекулярная дегидратация спиртов. Условия и механизм реакции. Правило Зайцева. 7. Нуклеофильные свойства спиртов. Реакции алкилирования и ацилирования. 8. Реакции окисления спиртов. Сравнение способности к окислению первичных, вторичных и третичных спиртов. 9. Реакции, используемые для идентификации этанола (окисление раствором K2Cr2O7 в кислой среде, йодоформная реакция). 10. Фенолы – определение. Многоатомные фенолы – пирокатехин, резорцин, гидрохинон. 11. Окислительно-восстановительная система гидрохинон-хинон. Хиноидные структуры в биологически активных соединениях (Самостоятельная работа № 3). 12. Сравнение кислотных и основных свойств спиртов и фенолов. 13. Сранение нуклеофильных свойств спиртов и фенолов. Условия реакций ацилирования и алкилирования фенолов. 14. Сравнение способности спиртов моно- и многоатомных фенолов к реакциям окисления 15. Реакции электрофильного замещения в феноле. Сравнение активности фенола и бензола в этих реакциях. 16. Реакции, используемые для идентификации фенола (бромирование, реакция с FeCl3). Рекомендуемая литература А - с. 154-162, 225-226, 245-246, 249, 221. А* - с. 153-158, 167-169, 175-177, 218, 223. А** - с. 160, 162-164, 165-167, 171-172, 175, 177, 182-183, 228, Б - тема 1.7, обучающая задача 3 (с. 86-88). Вопросы для самоконтроля (задания, обозначенные*, обязательны для выполнения в письменном виде) 1. Укажите тип спирта (первичный, вторичный, третичный), назовите по заместительной номенклатуре:
Приведите схемы реакций окисления данных спиртов. 2. Сравните кислотные свойства следующих соединений: - метанол, вода, фенол; - этанол, этиленгликоль; - метанол, вода, глицерин. 3*. Сравните способность этанола, фенола и пирокатехина к окислению. Приведите схемы соответствующих реакций. 4*. Приведите схемы реакций бутанола-2 с концентрированной серной кислотой в различных условиях (t=20o, t=140о, t=200o). 5. Приведите качественные реакции следующих соединений: этанол, глицерин, фенол. Укажите признак каждой реакции. 6*. Сравните нуклеофильные свойства этанола и фенола. Приведите схемы реакций их ацилирования. 7. Укажите, для каких спиртов характерна йодоформная реакция: метанол, этанол, пропанол-1, пропанол-2, бензиловый спирт. План работы на предстоящем занятии 1. Определение исходного уровня знаний (тестовый контроль). 2. Разбор основных вопросов темы. 3. Выполнение лабораторной работы: - Получение этилхлорида из этилового спирта; - Дегидратация этилового спирта; - Окисление этилового спирта бихроматом калия в кислой среде. 4. Оформление лабораторного журнала, контроль выполнения лабораторной работы.
|