ТЕМА 10 ФЕНОЛЫ И НАФТОЛЫФенолами называются соединения общей формулы АrОН, где Аr-фенил, замещенный фенил или одна из других арильных групп (например нафтил). Фенолы отличаются от спиртов тем, что ОН-группа в феноле связана непосредственно с ароматическим кольцом:
СН3 ОН ОН
Фенолы проявляют кислотные свойства и образуют фенолята с основаниями. Кислый характер гидроксилной группы у фенола обусловлен влиянием бензольного кольца. В свою очередь, гидроксильная группа сильно увеличивает реакционную способность бензольного кольца (заменитель 1 рода). Для нафтолов характерны обычные реакции фенолов. Реакция сочетания с солями диазония особенно важна в производстве красителей. 1. Слабокислотные свойства. Всем фенолам присущи слабокислые свойства, что проявляется в их способности растворяться в щелочах с образованием фенолята:
C6H5OH + NaOH → C6H5ONa + H2O.
Кислотные свойства фенолов выражены очень слабо. Так, фенолы не окрашивают лакмусовую бумагу. Самая слабая неорганическая кислота – угольная – вытесняет фенолы из их солеобразных соединений – фенолятов:
C6H5ONa + H2CO3 → C6H5OH↓ + NaHCO3.
Исходя из констант диссоциации, кислотные свойства фенола выражены в 3300 раз более, чем у угольной кислоты. Кислотные свойства фенольного гидроксила (по сравнению со спиртовым) объясняются тем, что в фенольном гидроксиле свободная пара электронов кислорода взаимодействует с π -электронами бензольного кольца, сдвигаясь в сторону кольца. Атом кислорода, так как его отрицательный заряд уменьшается, а положительный вследствие этого несколько увеличивается, сильнее притягивает к себе электрон от атома водорода из гидроксила; это облегчает отщепление водорода в виде протона, т. е. диссоциацию:
2. Образование простых эфиров. Фенолы, подобно спиртам, способны давать соединения типа простых эфиров. Практически для получения простых эфиров фенолов на феноляты действуют гелогеналкинами (а) или галогенарилами (б):
а) C6H5О Na + I C2H5 → C6H5 – O – C2H5 + NaI;
б) C6H5O Na + Br C6H5 → C6H5 – O – C6H5 + NaBr.
В первом случае (а) получается простой эфир, содержащий радикал фенола и радикал спирта, т. е. смешанный жирноароматический простой эфир. Во втором случае (б) получается простой эфир, содержащий два остатка фенола, т. е. ароматический простой эфир. 3. Образование сложных эфиров. Подобно спиртам фенолы могут давать соединения типа сложных эфиров. Практически для получения сложных эфиров фенолов обычно на феноляты действуют галогенангидридами кислот, например:
O O
Фенолы дают сложные эфиры как с органическими, так и с минеральными кислотами. 4. Реакция окрашивания с хлорным железом. Все фенолы с хлорным железом образуют окрашенные соединения; одноатомные фенолы обычно дают окрашивание фиолетового или синего цвета. 5. Замещение атомов водорода в бензольном ядре. Остаток бензола в фенолах влияет на гидроксильную группу, сообщая ей кислотные свойства. И гидроксил, введенный в молекулу бензола, влияет на остаток бензола, увеличивая подвижность атомов водорода в бензольном ядре. В результате атомы водорода в ядре молекулы фенола замещаются гораздо легче, чем у бензола. Замещение галогенами. При действии на фенолы галогенов, даже бромной воды, три атома очень легко замещаются и получаются тригалогенозамещенные фенолы:
Br Атомы брома замещают атомы водорода, находящиеся в орто- и пара-положении по отношению к гидроксильной группе. Замещение остатком азотной кислоты. Фенолы очень легко нитрируются. Так, при действии даже очень разбавленной азотной кислоты получается смесь о- и n-нитрофенола:
Замещение остатком серной кислоты. Фенолы легко сульфируются; из фенола при этом получается смесь о- и n-фенолсульфо-кислот:
6. Окисление фенолов. Фенолы легко окисляются даже при действии кислорода воздуха. При этом они изменяют свой цвет, окрашиваясь в розовый, красно-розовый или темно-красный цвет. Примеси к фенолам ускоряют окисление и поэтому неочищенные фенолы обычно темнеют очень сильно и быстро. Первой стадией при окислении фенолов является отщепление атома водорода от гидроксильной группы с образованием свободного феноксильного радикала с одновалентным кислородом. Эти радикалы далее вступают в различные сложные химические превращения, часто с образованием более крупных молекул. При более энергичном окислении фенолов (например, хромовой смесью) наряду с окислением фенольного гидроксила окисляется атом водорода, находящийся в пара-положении по отношению к гидроксильной группе; при этом образуются бензохинон и продукты его дальнейших превращений: H H
C = C H H
В условиях еще более энергичного окисления бензольное ядро фенолов разрушается. 7. Антисептические свойства. Фенолы убивают многие микроорганизмы. Это свойство используют в медицине, применяя фенолы и их производные как дезинфицирующие и антисептические средства. Фенол (карболовая кислота) был превым антисептическим средством, введенным в хирургию Листером в 1867 г. Антисептические свойства фенолов основаны на их способности свертывать белки. Гомологи фенола – крезолы – обладают более сильным бактерии-цидным действием, чем сам фенол. Антисептическое действие различных антисептических средств часто сравнивают с таковым фенола. «Фенольный коэффициент» – число, показывающее, во сколько раз антисептическое действие данного вещества больше (или меньше) действия фенола, принимаемого за единицу. Путем введения в молекулы фенолов различных заместителей – ато-мов галогена и т. д. – был получен ряд антисептических средств, более ценных, чем сам фенол. Итак, в данном разделе разработаны химические и антисептические свойства фенолов и нафтолов. [ 1, с. 130− 132; 3, с. 112− 126; 5, с. 389− 397].
|












 – O – H – O- + H+.
– O – H – O- + H+.








 C6H5ONa + Cl – C – CH3 → C6H5 – O – C – CH3 + NaCl.
C6H5ONa + Cl – C – CH3 → C6H5 – O – C – CH3 + NaCl. OH
OH


 ОН
ОН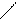







 Br Br
Br Br


 +3Br2 + 3HBr
+3Br2 + 3HBr

 OH
OH
 NO2
NO2

 2 + 2HNO3 –OH + O2N– –OH +2Н2О
2 + 2HNO3 –OH + O2N– –OH +2Н2О
 OH OH OH
OH OH OH
 SO3H
SO3H 
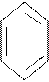
 2 + 2H2SO4 + + 2Н2О
2 + 2H2SO4 + + 2Н2О SO3H
SO3H
 C = C
C = C



