Стандартные окислительно-восстановительные потенциалы
| Элемент
| Полуреакция
| Е 0, В
| | Ag
| Ag+ + 1 ē; = Ag
| +0,80
| | AgCl + 1 ē; = Ag + Cl-
| + 0,22
| | Ag2+ + 1 ē; = Ag+
| + 1,98
| | Ag2О + Н2О + 2 ē; = 2Ag + 2ОН-
| + 0,34
| | 2AgО + Н2О + 2 ē; = Ag2О + 2ОН-
| + 0,607
| | Ag2S + 2 ē; = 2Ag + S2-
| – 0,691
| | Ag2S + 2Н+ + 2 ē; = 2Ag + Н2S
| – 0,0366
| | AgI + 1 ē; = Ag + I-
| – 0,15
| | Al
| AlO  + 2H2O + 3 ē; = Al + 4OH- + 2H2O + 3 ē; = Al + 4OH-
| – 2,35
| | Al(OH)3 + 3 ē; = Al + 4OH-
| – 2,328
| | As
| H3AsO4 + 2H+ + 2 ē; = HAsO2 + 2H2O
| + 0,56
| AsO  + 2H2O + 2 ē; = AsO + 2H2O + 2 ē; = AsO  + 4OH- + 4OH-
| – 0,71
| | Be
| Be2O 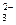 + 3H2O + 4 ē; = 2Be + 6OH- + 3H2O + 4 ē; = 2Be + 6OH-
| – 2,63
| | Bi
| NaBiO3 + 6H+ + 2 ē; = Bi3+ + 3H2O + Na+
| +1,81
| | Br
| BrO3- + 3H2O + 6 ē; = Br-+ 6OH-
| +0,61
| | Br2 + 2 ē; = 2Br-
| +1,09
| | HBrO + H+ + 2 ē; = Br- + H2O
| +1,34
| | Cl
| Cl2 + 2 ē; = 2Cl-
| +1,36
| | ClO3- + 6H+ + 6 ē; = Cl- + 3H2O
| +1,46
| | ClO- + H2O + 2 ē; = Cl- + 2OH-
| +0,92
| | 2ClO- + 2H2O + 2 ē; = Cl2 + 4OH-
| +1,56
| ClO  + 2H2O + 4 ē; = Cl- + 4OH- + 2H2O + 4 ē; = Cl- + 4OH-
| +0,76
| ClO  + H2O + 2 ē; = ClO- + 2OH- + H2O + 2 ē; = ClO- + 2OH-
| +0,66
| ClO  + 8H+ + 8 ē; = Cl- + 4H2O + 8H+ + 8 ē; = Cl- + 4H2O
| +1,389
| ClO  + H2O + 2 ē; = ClO + H2O + 2 ē; = ClO  + 2OH- + 2OH-
| +0,36
| | HClO2 + 2H+ + 2 ē; = HClO + H2O
| + 1,645
| | Cr
| Cr2O72- + 14H+ + 6 ē; = 2Cr3+ + 7H2O
| +1,33
| CrO 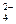 +2H2O + 3 ē; = CrO2- + 4OH- +2H2O + 3 ē; = CrO2- + 4OH-
| - 0,21
| CrO 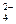 + 4H2O + 3 ē; = Cr3+ + 8OH- + 4H2O + 3 ē; = Cr3+ + 8OH-
| +1,45
| CrO 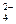 + 8H+ + 3 ē; = Cr3+ + 4H2O + 8H+ + 3 ē; = Cr3+ + 4H2O
| +1,47
| | Cr(OH)3 + 3 ē; = Cr + 3OH-
| – 1,48
| | CrO3 + 6H+ + 3 ē; = Cr3+ + 3H2O
| – 0,11
| CrO 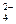 + 4H2O + 3 ē; = Cr(OH)3 + 5OH- + 4H2O + 3 ē; = Cr(OH)3 + 5OH-
| – 0,13
| | H
| 2H2O + 2 ē; = H2 + 2OH-
| – 0,83
| | H2O2 + 2H+ + 2 ē; = 2H2O
| +1,776
| | I
| 2IO3- + 12H+ + 10 ē; = I2 + 6H2O
| +1,195
| | 2IO- + 4H+ + 2 ē; = I2 + 2H2O
| +1,10
| | HIO + H+ + 2 ē; = I- + H2O
| +0,987
| | IO- + H2O + 2 ē; = I- + 2OH-
| +0,485
| IO  + 6H+ + 6 ē; = I- + 3H2O + 6H+ + 6 ē; = I- + 3H2O
| +1,085
| IO  + 2H2O+ 4 ē; = IO- + 4OH- + 2H2O+ 4 ē; = IO- + 4OH-
| +0,15
| IO  + 3H2O+ 6 ē; = IO- + 6OH- + 3H2O+ 6 ē; = IO- + 6OH-
| +0,26
| | I2 + 2 ē = 2I-
| +0,54
| | 2HIO + 2H+ + 2 ē; = I2 + 2H2O
| +1,439
| | Fe
| Fe(OH)3 + 1 ē; = Fe(OH)2 + OH-
| – 0,56
| | Fe2O3 + 4H+ + 2 ē; = 2FeOH+ + H2O
| +0,16
| | Mn
| MnO2 + 4H+ + 2 ē; = Mn2+ + 2H2O
| +1,24
| MnO  + 8H+ + 5 ē = Mn2+ + 4H2O + 8H+ + 5 ē = Mn2+ + 4H2O
| +1,53
| MnO  + 1 ē; = MnO42- + 1 ē; = MnO42-
| +0,56
| | MnO2 + 4OH- + 2 ē; = Mn2+ + 2H2O
| +1,15
| MnO  + 2H2O + 2 ē; = MnO2 + 4OH- + 2H2O + 2 ē; = MnO2 + 4OH-
| +0,60
| MnO  + 4H+ + 3 ē; = MnO2 + 2H2O + 4H+ + 3 ē; = MnO2 + 2H2O
| +1,679
| MnO  + 2H2O + 3 ē; = MnO2 + 4OH- + 2H2O + 3 ē; = MnO2 + 4OH-
| +0,595
| | Mn(OH)2 + 2 ē; = Mn + 2OH-
| – 1,56
| | Mn(OH)3 + 1 ē; = Mn(OH)2 + OH-
| +0,15
| | Mn2O3 + 6H+ + 2 ē; = 2Mn2+ + 3H2O
| +1,485
| | N
| NO  + 2H+ + 1 ē; = NO2 + H2O + 2H+ + 1 ē; = NO2 + H2O
| +0,77
| | N2 + 2H2O + 6H+ + 6 ē; = 2NH4OH
| 0,092
| | 3N2 + 2H+ + 2 ē; = 2HN3
| – 3,09
| N2H  + 3H+ + 2 ē; = 2NH + 3H+ + 2 ē; = 2NH 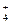
| +1,275
| | N2O + 2H+ + 2 ē; = N2 + H2O
| +1,766
| N2O4 + 2 ē; = 2NO 
| +0,867
| | N2O4 + 2H+ + 2 ē; = 2HNO2
| +1,065
| | N2O4 + 4H+ + 4 ē; = 2NO + 2H2O
| +1,035
| | 2NO + 2H+ + 2 ē; = N2O + H2O
| +1,591
| | 2NO + H2O + 2 ē; = N2O + 2OH-
| +0,76
| | HNO2 + H+ + 1 ē; = NO + H2O
| +0,983
| NO  + 3H+ + 2 ē; = HNO2 + H2O + 3H+ + 2 ē; = HNO2 + H2O
| +0,94
| NO  + 2H+ + 2 ē; = NO2- + H2O + 2H+ + 2 ē; = NO2- + H2O
| +0,84
| NO  + H2O + ē; = NO + 2OH- + H2O + ē; = NO + 2OH-
| – 0,46
| NO  + 4H+ + 3 ē = NO + 2H2O + 4H+ + 3 ē = NO + 2H2O
| +0,96
| 2NO  + 2H2O + 4 ē; = N2O + 2H2O + 4 ē; = N2O  + 4OH- + 4OH-
| – 0,18
| 2NO  + 3H2O + 4 ē; = N2O + 6OH- + 3H2O + 4 ē; = N2O + 6OH-
| +0,15
| 2NO  + 2H2O + 2 ē; = N2O4 + 4OH- + 2H2O + 2 ē; = N2O4 + 4OH-
| – 0,85
| 2NO  + 4H+ + 2 ē; = N2O4 + 2H2O + 4H+ + 2 ē; = N2O4 + 2H2O
| +0,803
| NO  + H2O + 2 ē; = NO + H2O + 2 ē; = NO  + 2OH- + 2OH-
| +0,01
| | О
| O2 + 2H+ + 4 ē; = 4OH-
| +0,40
| | O2 + 2H+ + 2 ē; = H2O2
| +0,69
| | O2 + 4H+ + 4 ē; = 2H2O
| +1,229
| | O2 + 2H2O + 2 ē; = H2O2 + 2OH-
| – 0,146
| | O3 + 2H+ + 2 ē; = H2O + O2
| +2,076
| | O2 + 2H2O + 4 ē; = 4OH-
| +0,40
| | O3 + 2H2O + 2 ē; = O2 + 2OH-
| +1,24
| | P
| H3PO4 + 5H+ + 5 ē; = P + 4H2O
| -0,41
| | H3PO4 + 2H+ + 2 ē; = H3PO3 + H2O
| -0,28
| | Pb
| [Pb(OH)4]2- + 2 ē; = Pb + 4OH-
| -0,52
| | PbO2 + 4H+ + 2 ē; = Pb2+ + 2H2O
| +1,46
| | PbO2 + 2 ē; = PbO22-
| +1,70
| | S
| S + 2 ē; = S2-
| -0,48
| | S + H2О + 2 ē; = HS- + ОН-
| - 0,478
| | SO42- + 10H+ + 8 ē = H2S + 4H2O
| +0,30
| | S + 2H+ + 2 ē; = H2S
| +0,142
| | SO2 + 4H+ + 4 ē; = S + 2H2O
| +0,45
| | SO42-+ 4H+ + 2 ē; = SO2 + 2H2O
| +0,16
| | SO42- + 8H+ + 6 ē; = S + 4H2O
| +0,35
| | SO42- + 8H+ + Cu2+ + 8 ē; = CuS + 4H2O
| +0,42
| | SO42- + 2H+ + 2 ē; = SO32- + H2O
| -0,10
| | Se
| SeO42- + 2H+ + 2 ē = SeO32- + H2O
| +1,15
|

Расчетные и графические задания Равновесный объем - это объем, определяемый равенством спроса и предложения...
|

Кардиналистский и ординалистский подходы Кардиналистский (количественный подход) к анализу полезности основан на представлении о возможности измерения различных благ в условных единицах полезности...
|

Обзор компонентов Multisim Компоненты – это основа любой схемы, это все элементы, из которых она состоит. Multisim оперирует с двумя категориями...
|

Композиция из абстрактных геометрических фигур Данная композиция состоит из линий, штриховки, абстрактных геометрических форм...
|
|
Педагогическая структура процесса социализации Характеризуя социализацию как педагогический процессе, следует рассмотреть ее основные компоненты: цель, содержание, средства, функции субъекта и объекта...
Типовые ситуационные задачи. Задача 1. Больной К., 38 лет, шахтер по профессии, во время планового медицинского осмотра предъявил жалобы на появление одышки при значительной физической
Задача 1. Больной К., 38 лет, шахтер по профессии, во время планового медицинского осмотра предъявил жалобы на появление одышки при значительной физической нагрузке. Из медицинской книжки установлено, что он страдает врожденным пороком сердца....
Типовые ситуационные задачи. Задача 1.У больного А., 20 лет, с детства отмечается повышенное АД, уровень которого в настоящее время составляет 180-200/110-120 мм рт Задача 1.У больного А., 20 лет, с детства отмечается повышенное АД, уровень которого в настоящее время составляет 180-200/110-120 мм рт. ст. Влияние психоэмоциональных факторов отсутствует. Колебаний АД практически нет. Головной боли нет. Нормализовать...
|
|
Плейотропное действие генов. Примеры. Плейотропное действие генов - это зависимость нескольких признаков от одного гена, то есть множественное действие одного гена...
Методика обучения письму и письменной речи на иностранном языке в средней школе. Различают письмо и письменную речь.
Письмо – объект овладения графической и орфографической системами иностранного языка для фиксации языкового и речевого материала...
Классификация холодных блюд и закусок. Урок №2 Тема: Холодные блюда и закуски. Значение холодных блюд и закусок. Классификация холодных блюд и закусок. Кулинарная обработка продуктов...
|
|