Титрування та його видиПроцес додавання одного розчину до іншого до досягнення точки еквівалентності з метою визначення концентрації одного з них називається титруванням. Розрізняють пряме і зворотне титрування. При прямому титруванні досліджуваний розчин безпосередньо титрують стандартним розчином. Зворотне титрування застосовують тоді, коли досліджувана речовина не реагує зі стандартним розчином або реагує повільно. В цьому випадку до розчину приливають надлишок третього компонента і відтитровують стандартним розчином. Момент закінчення реакції, коли реагуючі речовини повністю прореагують називаються точкою еквівалентності. Методом нейтралізації називається метод титриметричного аналізу, який ґрунтується на використанні реакції взаємодії йонів гідрогену і гідроксогрупи: Робочими розчинами в оксидиметрії є розчини окисників і відновників. Кількісною характеристикою інтенсивності окисно-відновного процесу є різниця окисно-відновних потенціалів реагуючих між собою систем.
57.Ацидиме́трія — метод об'ємного аналізу, що сводиться до визначення вмісту кислот у розчинах за відомою концентрацією лугу. Робочтй розчин-HCl, аналізований розчин-КОН (NaOH). Індикатор: метилоранж в точці еквівалентності змінюється з жовтого на рожевий. (HCl+KOH=NaCl+H20)… Результати обчислюємо на основі закону еквівалентів: N(HCl)*V(HCl)=N(KOH)*V(KOH)….Нормальность КОН визначаємо за формулою N(KOH)= 58. Комплексомитрія-грунтується на утворенні комплексних сполук. Комплексні сполуки утворюються між індикатором та аналізованою речовиною. В процесі титрування цей, комплекс руйнується і утворюється більш міцний безбарвний комплекс між аналізованою речовиною і титрованим розчином (робочим розчином). Визначення загальної твердості води (Н2О). Робочий розчин трилон Б. Аналізований розчин Н2О, що містить катіони 59.Перманганатометрія як метод об’ємного аналізу. Перманганатометрія визначення вмісту Fe в розчині солі Мора. (NH4)2SO4*Fe2SO4*6H20 (сіль Мора, подвійна сіль амонійсульфата і ферумсульфата на 6 молекул води). Індикатор змінює забарвлення в точці еквівалентності з блідо-рожевого, на малиновий. KMnO4+FeSO4+H2SO4=MnSO4+K2SO4+Fe2(SO4)3+H2O….. Cн(FeSO4)= 60. Йодометрія, як метод об’ємного аналізу. I2+2e=
|

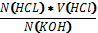 …Маса m(KOH)=N(KOH)*Meквіваленту(КОН)*V(KOH)… Використання в практиці СГ: Протолітометрія використовують з метою визначення кислотності молока та хліба, кислотності меду; Для встановлення карбонатної твердості води. Для визначення нітрогену в солях амонію; для визначення загальної кислотності плодів та овочів.
…Маса m(KOH)=N(KOH)*Meквіваленту(КОН)*V(KOH)… Використання в практиці СГ: Протолітометрія використовують з метою визначення кислотності молока та хліба, кислотності меду; Для встановлення карбонатної твердості води. Для визначення нітрогену в солях амонію; для визначення загальної кислотності плодів та овочів. . Індикатор: хромоген чорний, змінює своє забарвлення в точці еквівалентності з вино – червоного на синє. Трилон Б-є етилендіамін тетраацетатна кислота або натрієва силь. Рівняння реакції індикатором:
. Індикатор: хромоген чорний, змінює своє забарвлення в точці еквівалентності з вино – червоного на синє. Трилон Б-є етилендіамін тетраацетатна кислота або натрієва силь. Рівняння реакції індикатором: 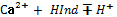 . Під час взаємодії Са з індикатором утв комплекс вино – червоного кольору Са
. Під час взаємодії Са з індикатором утв комплекс вино – червоного кольору Са  +Na2[H2I]→Na2[CaI]+HI+
+Na2[H2I]→Na2[CaI]+HI+  … Під час взаємодії Трилон Б з утвореним комплексом, звільняється індикатор синього кольору. T=
… Під час взаємодії Трилон Б з утвореним комплексом, звільняється індикатор синього кольору. T=  *1000
*1000 …. m(FeSO4)=Cн(FeSO4)*Mекв(FeSO4)*V(FeSO4)… Використання перманганатометрії для визначення вмісту оксалатної кислоти, для визначення вмісту N в азотних добривах.
…. m(FeSO4)=Cн(FeSO4)*Mекв(FeSO4)*V(FeSO4)… Використання перманганатометрії для визначення вмісту оксалатної кислоти, для визначення вмісту N в азотних добривах. … Визначення вмісту Сu в розчині за йодометрією. Na2S2O3- робочий розчин (натрій тіосульфат). CuSO4 –аналізований розчин. Індикатор: крохмаль змінює свій колір з синього на соломино-жовтий в точці еквівалентності. Данний метод представляє собою, метод заміщення. Тобто кількість еквівалентів Cu, дорівнює кількості еквівалентів виділеного I, а також кількості еквівалентів робочого розчину натрій тіосульфат. Основний процес титрування складається з двох реакцій: допоміжної та основної. 2CuSO4+4KI=2CuI+I2+2K2SO4 – допоміжна реакція. 2Na2S2O3+I2=2NaI+Na2S4O6 – основна реакція. Результати аналізу CuSO4- досліджуваний розчин. Сн=; m(CuSO4)=Cн(CuSO4)*Mекв(CuSO4)*V(CuSO4) Використання методу в практиці СГ: 1)Для визначення вмісту Cu в отрутохімікатах; 2) для визначення вмісту активного Cl в вапні (білильному); 3)) для визначення якості олійних культур.
… Визначення вмісту Сu в розчині за йодометрією. Na2S2O3- робочий розчин (натрій тіосульфат). CuSO4 –аналізований розчин. Індикатор: крохмаль змінює свій колір з синього на соломино-жовтий в точці еквівалентності. Данний метод представляє собою, метод заміщення. Тобто кількість еквівалентів Cu, дорівнює кількості еквівалентів виділеного I, а також кількості еквівалентів робочого розчину натрій тіосульфат. Основний процес титрування складається з двох реакцій: допоміжної та основної. 2CuSO4+4KI=2CuI+I2+2K2SO4 – допоміжна реакція. 2Na2S2O3+I2=2NaI+Na2S4O6 – основна реакція. Результати аналізу CuSO4- досліджуваний розчин. Сн=; m(CuSO4)=Cн(CuSO4)*Mекв(CuSO4)*V(CuSO4) Використання методу в практиці СГ: 1)Для визначення вмісту Cu в отрутохімікатах; 2) для визначення вмісту активного Cl в вапні (білильному); 3)) для визначення якості олійних культур.


