Материальный баланс колонны стабилизации К-2 на первой технологической нитке УСК до реконструкции колонны
Материальный баланс колонны стабилизации К-2 на первой технологической нитке УСК до реконструкции колонны Исходные данные для расчета: Состав сырья – Конденсата газового деэтанизированного, поступающего на питание колонны:
Расход сырья КГД,
Определение характеристик исходного сырья. Мольная масса сырья находится по формуле (1):
+ 0,035
Найдем расход сырья ВК, поступающего в колонну кг/ч:
где
Массовые доли компонента в сырье определяются по формуле (2):
х (С2Н6) = х (С3Н8) = х ( х ( х ( х( х ( ∑хi = 1,0.
Массовый расход компонентов рассчитывается по формуле (3):
GF (С2Н6) = 67399 GF (С3Н8) = 67399 GF (С4Н10) = 67399 GF (i-С4Н10) = 67399 GF (С5Н12)= 67399 GF (i-С5Н12)= 67399 GF (
Число молей компонентов в массовом расходе сырья определяется по формуле (4)
Состав и характеристики исходного сырья приведены в таблице 11. Таблица 11 – Состав и характеристики исходного сырья
Определение характеристик дистиллята. Массовый расход компонентов в дистилляте определяется по формуле (5):
D (С2Н6) =
D (С3Н8) =
D (i-С4Н10) =
D (С4Н10) =
D (i-С5Н12) =
D (С5Н12) =
D (∑
Массовый расход дистиллята находится по формуле (6):
D = 16179,52
Массовая доля компонента в дистилляте определяется по формуле (7):
xD (С2Н6) =
xD (С3Н8) =
xD (i-С4Н10) =
xD (С4Н10) =
xD (i-С5Н12) =
xD (С5Н12) =
xD (∑
∑хD = 1,0.
Число молей компонента в дистилляте рассчитывается по формуле (8):
ND (С2Н6) =
ND (С3Н8) =
ND (i-С4Н10) =
ND (С4Н10) =
ND (i-С5Н12) =
ND (С5Н12) =
ND (∑
Число молей в дистилляте определяется по формуле (9):
∑NDi = 191,725
Мольная доля компонента в дистилляте находится по формуле (10):
yD (С2Н6) =
yD (С3Н8) =
yD (i-С4Н10) =
yD (С4Н10) =
yD (i-С5Н12) =
yD (С5Н12) =
yD (∑
∑yi=1,0.
Состав и характеристики дистиллята приведены в таблице 12. Таблица 12 – Состав и характеристики дистиллята
Определение характеристик кубового остатка. Массовый расход компонента в остатке находится по формуле (11):
Wi (С2Н6) = 15,197 – 15,197 = 0
Wi (С3Н8) = 1145,161 – 1110,807 = 34,354
Wi (i-С4Н10) = 991,862 – 912,329 = 79,333
Wi (С4Н10) = 1799,684 – 1691,703 = 107,981
Wi (i-С5Н12) = 1641,372 – 1411,584 = 229,792
Wi (С5Н12) = 1595,779 – 1404,286 = 191,493
Wi (∑
С2Н6 – полностью поступает в дистиллят. Массовый расход кубового остатка определяется по формуле (12):
∑ Wi = 51219,457
Массовая доля компонентов в остатке рассчитывается по формуле (13):
xW (С3Н8) =
xW (i-С4Н10) =
xW (С4Н10) =
xW (i-С5Н12) =
xW (С5Н12) =
xW (∑
∑ xW =1,0.
Число молей компонента в кубовом остатке находится по формуле (14):
NW (С3Н8) =
NW (i-С4Н10) =
NW (С4Н10) =
NW (i-С5Н12) =
NW (С5Н12) =
NW (∑
Число молей в кубовом остатке рассчитывается по формуле (15):
∑NWi = 440,189
Мольная доля компонента в остатке находится по формуле (16):
x (С3Н8) =
x (i-С4Н10) =
x (С4Н10) =
x (i-С5Н12) =
x (С5Н12) =
x (∑
∑хi =1,0.
Состав и характеристики кубового остатка представлены в таблице 13. Таблица 13 – Состав и характеристики кубового остатка
Составим материальный баланс деэтанизатора в таблице 14, исходя из полученных результатов.
В соответствии с данными расчета материального баланса колонны К-2 расходы потоков составляют:
Мольная доля компонента в дистилляте находится по формуле
где Ki – константа фазового равновесия компонента дистиллята (определяем при Р = 2,7 МПа и toC = 28oC (температура дистиллята) [стр. 26,1].
x (СН4) =
х (∑С2) =
х (С3Н6) =
х (С3Н8) =
х (∑С4Н8) =
х (изо − С4Н10) =
х (норм − С4Н10) =
х (∑С5Н10) =
х (изо − С5Н12) =
х (норм − С5Н12) =
х (∑С6) =
∑хi=1.
Результаты расчета приведены в таблице 5.
Таблица 5 – Расчет необходимого давления из условий конденсации дистиллята
По уравнению изотермы конденсации методом подбора давления в верхней части колонны и температуры верха. Согласно расчёта, условие изотермы выполняется (yi = ∑ Определим мольный состав равновесных паров. Методом подбора при давлении 2,7 МПа, используя уравнение изотермы кипения, определим toCпитания
уi = Ki ∙ xi, (22)
у(СН4) = 8
у (∑С2) = 4
у (С3Н6) = 1,1
у (С3Н8) = 1,6
у (∑С4Н8) = 0,053
у (изо − С4Н10) = 2,1
у (норм − С4Н10) = 0,19
у (∑С5Н10) = 0,04
у (изо − С5Н12) = 0,048
у (норм − С5Н12) = 0,042
у (∑С6) = 0,001
Условие изотермы выполняется ∑уi = 1 при tокип = 112оС.
Результаты расчета приведены в таблице 6.
Таблица 6 – Результаты определения мольного состава равновесных паров
Для построения рабочей линии и линии равновесия заданная многокомпонентная смесь (сырье) сводится к псевдобинарной, состоящей из двух ключевых компонентов: ∑С2 и С3Н8. Определение концентрации С2Н6 в исходной бинарной системе находится по формуле
xF =
xF =
Определение концентрации ∑С2 в дистилляте производится по формуле
xD =
xD =
Определение концентрации ∑С2 в остатке по формуле
xW =
xW =
Построение кривой фазового равновесия. Для построения кривой фазового равновесия в координатах «х - у» используют уравнение равновесия концентрации бинарной системы
у =
где α – относительная летучесть псевдобинарной смеси при условии ввода сырья
α =
α =
Задаваясь рядом произвольных значений «х» по формуле (26) определим равновесные концентрации компонента в газовой фазе «у». По найденным значениям «х - у» строится кривая равновесия фаз.
Таблица 7 – Данные для построения кривой равновесия фаз
у1 =
у2 =
у3 =
у4 =
У5 = У6 =
У7 =
У8 =
Построение рабочей линии в координатах «х - у». Определение координат точки В при х = 0
B =
где R – флегмовое число
R = Rmin ∙ β, (29)
где β = 1,4, коэффициент избытка флегмы, Rmin – минимальное флегмовое число
Rmin =
где уР – равновесная концентрация этана в паровой фазе
уР =
уР =
Подставим данные в формулу (26) и получим результат
Rmin =
Подставим данные в формулу (24) и получим результат
B =
Число теоретических тарелок находится построением ступенчатой линии между линией равновесия и линией рабочей концентрации в пределах хW снизу вверх и от хD сверху вниз. В результате построения ступенчатой линии число теоретических контактов (тарелок) составило: - в концентрационной части – 28; − в отпарной части – 4. Действительное число контактов (тарелок)
ND =
ND =
Результаты, полученные при расчете материального баланса, сводим в таблицу 8.
В соответствии с данными расчета материального баланса колонны К-1 расходы потоков составляют:
|

 0,08;
0,08;  4,1;
4,1; 2,7;
2,7; 4,9;
4,9; 3,6;
3,6; 4,5;
4,5; 80,9;
80,9; 103;
103;
 = 0,0008
= 0,0008  30 + 0,041
30 + 0,041  58 + 0,049
58 + 0,049  .
.
 – расход сырья м3/ч;
– расход сырья м3/ч; – относительная плотность КГД,
– относительная плотность КГД, 

 = 0,0002,
= 0,0002, = 0,017,
= 0,017, ) =
) =  = 0,015
= 0,015 = 0,027,
= 0,027, ) =
) =  = 0,024,
= 0,024, = 0,024,
= 0,024, = 0,893,
= 0,893, 0,0002 = 15,197
0,0002 = 15,197  ,
,








 хi
хi
 ,
, 
 ,
, 

 = 15,197
= 15,197  = 1110,807
= 1110,807  = 912,329
= 912,329  = 1691,703
= 1691,703  = 1411,584
= 1411,584  = 1404,286
= 1404,286  = 9633,62
= 9633,62  = 0,0009,
= 0,0009, = 0,068,
= 0,068, = 0,056,
= 0,056, = 0,104,
= 0,104, = 0,087,
= 0,087, = 0,086,
= 0,086, = 0,595,
= 0,595, = 0,506
= 0,506  = 25,245
= 25,245  = 15,729
= 15,729  = 29,167
= 29,167  = 19,605
= 19,605  = 19,503
= 19,503 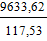 = 81,967
= 81,967  = 0,002,
= 0,002, = 0,131,
= 0,131, = 0,082,
= 0,082, = 0,152,
= 0,152, = 0,102,
= 0,102, = 0,101,
= 0,101, = 0,427,
= 0,427, = 0,00067,
= 0,00067, = 0,0015,
= 0,0015,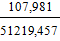 = 0,0021,
= 0,0021, = 0,0044,
= 0,0044, = 0,0037,
= 0,0037, = 0,987,
= 0,987, = 0,780
= 0,780  = 1,367
= 1,367  = 1,861
= 1,861  = 3,191
= 3,191  = 2,659
= 2,659  = 430,328
= 430,328  = 0,0017,
= 0,0017,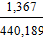 = 0,0031,
= 0,0031, = 0,0042,
= 0,0042, = 0,0072,
= 0,0072, = 0,0060,
= 0,0060, = 0,977,
= 0,977,





 – число молей в КГД
– число молей в КГД  ;
; – массовый расход ШФЛУ
– массовый расход ШФЛУ  – число молей в ШФЛУ
– число молей в ШФЛУ  – массовый расход КГС
– массовый расход КГС  – число молей в КГС
– число молей в КГС  , (21)
, (21) = 0,018,
= 0,018, = 0,118,
= 0,118, = 0,074,
= 0,074, = 0,165,
= 0,165, = 0,145,
= 0,145, = 0,067,
= 0,067, = 0,086,
= 0,086,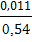 = 0,020,
= 0,020, = 0,049,
= 0,049, = 0,036,
= 0,036, = 0,219,
= 0,219, = 1). Значение давления в верхней части колонны 2,7 МПа принято правильно.
= 1). Значение давления в верхней части колонны 2,7 МПа принято правильно. 0,05 = 0,1,
0,05 = 0,1, 0,75 = 0,04,
0,75 = 0,04, , (23)
, (23) = 0,205.
= 0,205. , (24)
, (24) = 0,722.
= 0,722. , (25)
, (25) = 0,167.
= 0,167. , (26)
, (26) , (27)
, (27) = 2,5.
= 2,5. = 0,22,
= 0,22, = 0,38,
= 0,38, = 0,49,
= 0,49, = 0,56,
= 0,56, = 0,75,
= 0,75, = 0,84,
= 0,84,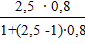 = 0,92,
= 0,92,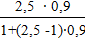 = 1.
= 1. , (28)
, (28) , (30)
, (30) , (31)
, (31) = 0,39.
= 0,39. = 1,79.
= 1,79.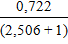 = 0,21.
= 0,21. , (32)
, (32) = 35.
= 35.





 ;
;


