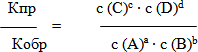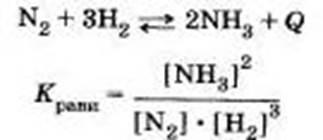Этап. Изучение нового материала.Химические реакции, протекающие в одном направлении, называют необратимыми. Большинство химических реакций являются обратимыми. Эта значит, что при одних и тех же условиях протекают и прямая, и обратная реакции (особенно если речь идет о замкнутых системах).
График показывает, что в какой то момент скорости прямой и обратной реакции становятся равными. Напишем это, используя кинетические уравнения для прямой и обратной реакций.
Vпр.= Кпр с (А)ª · с (В)b V обр. = Кобр с (С)c · с (D)d
Vпр. = Vобр. Кпр с (А)ª · с (В)b = Кобр с (С)c · с (D)d
Отсюда отношение константа скоростей прямой и обратной реакций.
Отношение констант скоростей прямой и обратной реакции называют константой равновесия. Константа равновесия обозначается буквой К и показывает, насколько полно протекает прямая реакция до момента наступления химического равновесия. Она показывает соотношение между концентрациями продуктов реакции (числитель) и исходных веществ (знаменатель) которое устанавливается при равновесии. Если константа равновесия больше единицы, это значит что на момент установления химического равновесия большая часть исходных веществ превратилась в продукты. А если меньше единицы- в продукты превратилась меньшая часть исходных веществ. Константы равновесия рассчитывают из опытных данных, определяя равновесные концентрации исходных веществ и продуктов реакции при определенной температуре. Значение константы равновесия характеризует выход продуктов реакции, полноту ее протекания.
Рассмотрим разные способы смещения равновесия на примере реакции взаимодействия азота и водорода с образованием аммиака:
Влияние изменения концентрации веществ Таким образом в реакционной смеси увеличится количество продукта реакции. Влияние изменения давления Предположим, что давление в замкнутой системе повысили, это значит, что концентрации всех газообразных веществ в рассматриваемой нами реакции возрастут в 2 раза. Изменение давления практически не сказывается на объеме жидких и твердых веществ, то есть не изменяет их концентрацию. Следовательно, состояние химического равновесия реакций, в которых не участвуют газы, не зависит от давления. Влияние изменения температуры Таким образом, скорость обратной реакции (в нашем примере эндотермической) увеличится сильнее, чем скорость прямой. Равновесие сместится в сторону процесса, сопровождающегося поглощением энергии. Значение константы равновесия характеризует выход продуктов реакции, полноту ее протекания. В случае гетерогенных реакций в выражение константы равновесия входят концентрации только тех веществ, которые находятся в газовой или жидкой фазе. Направление смещения равновесия можно предсказать, пользуясь принципом Ле Шателье (1884 г.): Если на систему, находящуюся в равновесии, оказывается внешнее воздействие (изменяется концентрация, давление, температура), то равновесие смешается в ту сторону, которая ослабляет данное воздействие. 4 этап. Закрепление нового материала 1.Структура СИМАЛТИНИУС РАУНД ТЕЙБЛ 2.Структура КУИЗ-КУИЗ-ТРЭЙД 2)Какие факторы влияют на смещение химического равновесия? (Температура, давление, концентрации исходных веществ и продуктов)
|