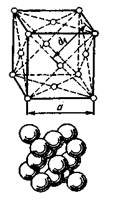
Кристаллическое строение металловВиды кристаллических решеток. Твердые вещества по взаимному расположению атомов делят на аморфные и кристаллические. Аморфными называют твердые вещества, атомы которых располагаются в пространстве хаотично. К таким веществам относят стекло, смолу, канифоль, клей и др. Кристаллическими называют твердые вещества, в которых атомы расположены в пространстве в строго определенном порядке. Все металлы являются кристаллическими веществами. Для описания кристаллической структуры металлов пользуются понятием кристаллической решетки. Кристаллическая решетка — это воображаемая пространственная сетка, в узлах которой расположены атомы. Наименьшая часть кристаллической решетки, определяющая структуру металла, называется элементарной кристаллической ячейкой. Элементарная ячейка повторяется во всех трех измерениях и полностью характеризует структуру кристалла. На рисунке изображены элементарные ячейки для наиболее распространенных кристаллических решеток: · объемно-центрированной кубической, · гранецентрированной кубической · гексагональной плотноупакованной. В элементарной ячейке кубической объемно-центрированной решетки девять атомов: восемь в вершинах решетки и один в центре. Такую решетку имеют железо при температурах до 911 и свыше 1392 °С, хром, вольфрам, ванадий и др. В элементарной ячейке кубической гранецентрированной решетки 14 атомов (8 в вершинах куба и по 1-му в центре каждой грани). Такую решетку имеют железо температуре от 911 до 1392 °С, медь, никель, алюминий и др. В элементарной ячейке гексагональной плотноупакованной решетки в виде шестигранной призмы 17 атомов (12 в вершинах призмы, 2 в центре оснований и 3 внутри призмы). Такая решетка у магния, цинка и др. Атомы в кристаллической решетке находятся на определенных расстояниях а, с и d1 друг от друга. Расстояние а и с между центрами атомов, находящихся в двух соседних узлах решетки называются параметрами или периодами решетки. Параметры решетки очень малы и измеряются в нанометрах (1 нм = 10 -9 м). Для большинства металлов они находятся в диапазоне 0,2-0,7 нм. Кубические решетки характеризуются только одним параметром — длиной ребра куба а. Гексагональные — двумя параметрами а и с, причем для гексагональной плотноупакованной отношение с/а = 1,633. (Золотое сечение связано с пространственным отношением природных объектов, человека, архитектурных сооружений, музыкальной гармонии, в геометрических фигурах, - их имеют многие цветы, морские звёзды, ежи, вирусы. У человека золотое сечение – это отношение его роста к расстоянию от пупка до подошв ног: при рождении оно равно 2, к 21 годам – 1,625, у женщин – 1,6. Многие женщины интуитивно пытаются приблизить это отношение к золотой пропорции, надевая туфли на каблуках. Атомы в кристаллической решетке можно условно рассматривать как соприкасающиеся между собой жесткие шары. При этом очевидно, что в решетке кроме атомов существует свободное пространство. Объем, который занимают атомы, т. е. плотность кристаллической решетки, характеризуют координационное число и коэффициент компактности.
Особенности кристаллического строения металлов определяют их свойства. Электроны, которые находятся на внешних атомных оболочках, теряют связь со своими атомами. Поэтому происходит образование свободных электронов, не принадлежащих отдельным атомам — электронного газа, а в узлах кристаллической решетки находятся положительно заряженные ионы. Между ионами и свободными электронами возникают силы притяжения, которые стягивают ионы. Такую связь называют металлической. Наличие металлической связи и объясняет характерные свойства металлов. В металлах расстояние между атомами значительно меньше, чем в неметаллах, поэтому металлы имеют большую плотность. Благодаря свободным электронам при пластической деформации связь между ионами не нарушается и разрушения не происходит, что объясняет высокую пластичность металлов. Наличие свободных электронов обусловливает высокую электро- и теплопроводность металлов. С понижением температуры ослабляются тепловые колебания ионов, что повышает электропроводность и в ряде случаев приводит к явлению сверхпроводимости при температурах, близких к абсолютному нулю. И напротив, с повышением температуры тепловые колебания ионов усиливаются и электропроводность снижается. Характерный металлический блеск объясняется взаимодействием световых волн со свободными электронами.
|