Методы получения азотной кислотыТехнология получения азотной кислоты Сырье для получения азотной кислоты Сырьем для получения азотной кислоты служат аммиак, воздух и вода. Синтетический аммиак в большей или меньшей степени загрязнен примесями. Такими примесями являются катализаторная пыль, смазочное масло (при сжатии поршневым компрессором). Для получения чистого газообразного аммиака служат испарительные станции и дистилляционные отделения жидкого аммиака [1]. Атмосферный воздух, применяемый в производстве азотной кислоты, забирается на территории завода или вблизи его. Этот воздух загрязнен газообразными примесями и пылью. Поэтому он подвергается тщательной очистке во избежание отравления катализатора окисления аммиака. Очистка воздуха осуществляется, как правило, в скруббере, а затем в двухступенчатом фильтре. Вода, применяемая для технологических нужд, подвергается специальной подготовке: отстою от механических примесей, фильтрованию и химической очистке от растворенных в ней солей. Для получения реактивной азотной кислоты требуется чистый паровой конденсат. Методы получения азотной кислоты Первый завод по производству HNO3 из аммиака коксохимического производства был пущен в России в 1916 г. В 1928 г. было освоено производство азотной кислоты из синтетического аммиака [1]. Различают производство слабой (разбавленной) азотной кислоты и производство концентрированной азотной кислоты. Процесс производства разбавленной азотной кислоты складывается из трех стадий: 1) конверсии аммиака с целью получения оксида азота 4NH3 + 5О2 → 4NO + 6Н2О; 2) окисления оксида азота до диоксида азота 2NO + О2 → 2NO2; 3) абсорбции оксидов азота водой 4NO2 + О2 + 2Н2О → 4HNO3; Суммарная реакция образования азотной кислоты выражается NH3 + 2О2 → HNO3 + Н2О. Производство азотной кислоты по схеме АК-72. В основу схемы АК-72, разработанной в СССР, положен замкнутый энерготехнологический цикл с двухступенчатой конверсией аммиака и охлаждением нитрозных газов под давлением 0,42–0,47 МПа и абсорбцией оксидов азота при давлении 1,1—1,26 МПа; продукция выпускается в виде 60%-ной HNO3. Первый агрегат АК-72 мощностью 380 тыс. т/год был пущен в 1976 г [1]. Принципиальная технологическая схема процесса приведена на рисунке 1.1. Воздух забирают из атмосферы через трубу 25, очищают от пыли в фильтре 24, сжимают воздушным компрессором 23 до 0,42 МПа и, разделив на два потока, подают в контактный аппарат и подогреватель аммиака. Жидкий аммиак (парожидкостная смесь) через ресивер 1 поступает в испаритель 2, где испаряется при 10–16 °С и давлении 0,6 МПа. После испарителя газообразный аммиак очищают от масла и механических примесей в фильтре 3 и направляют в подогреватель аммиака 4, где он нагревается до 80–120 °С воздухом. Очищенный воздух и аммиак поступают в смесительную камеру 22 контактного аппарата 20. Образующаяся аммиачно-воздушная смесь содержит 9,6–10,0% NH3. Пройдя тонкую очистку в фильтре, встроенном в контактный аппарат, аммиачно-воздушная смесь поступает на двухступенчатый катализатор, состоящий из трех платиноидных сетоь и слоя неплатинового катализатора. Нитрозные газы при температуре 840–860 °С поступают в котел-утилизатор 19, расположенный под контактным аппаратом, где за счет их охлаждения получают пар давлением 40 МПа с температурой 440 °С. Котел питают химически очищенной водой, деаэрированной в колонне 17. Деаэрированная вода проходит теплообменник 16, где нагревается нитрозными газами до 150 °С, экономайзер 18 и затем поступает в барабан котла-утилизатора 21.
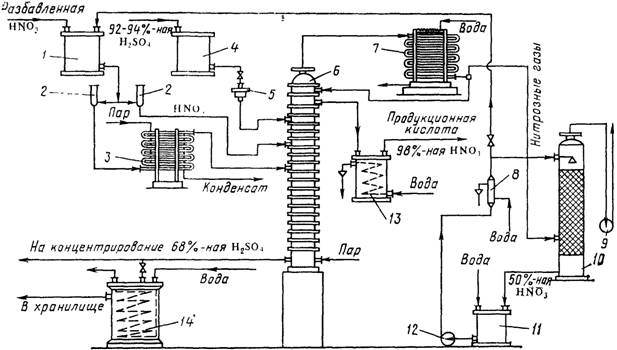
Рисунок 1.1 –Технологическая схема производства азотной кислоты АК-72: 1 – ресивер; 2 – испаритель; 3, 24 – фильтры; 4, 15 – подогреватели; 5 – рекуперационная турбина; 6 – реактор каталитической очистки; 7 – смеситель; 8 – топочное устройство; 9 – продувочная колонна; 10 – абсорбционная колонна, II, 14 – водяные холодильники; 12, 23 – компрессоры; 13 – газовый промыватель; 16, 18 – холодильники нитрозных газов; 17 – деаэрационная колонна; 19 – котел-утилизатор; 20 – контактный аппарат; 21 – барабан с сепарационным устройством; 22 – смесительная камера; 25 – труба для забора воздуха Нитрозные газы после котла-утилизатора охлаждаются в экономайзере 18, отдают свою теплоту в подогревателе 15 и затем поступают в водяной холодильник 14 для дальнейшего охлаждения до 55 СС. При охлаждении нитрозных газов происходит конденсация паров воды с образованием 40–45%-ной азотной кислоты, которая подается в газовый промыватель 13. Сюда же поступают нитрозные газы. В промывателе происходит одновременно с охлаждением промывка нитрозных газов от ндтрит-нитратных солей и дальнейшая конденсация азотной кислоты. Кислота из нижней части промывателя подается в абсорбционную колонну 10, а нитрозные газы сжимаются в компрессоре 12 до 11–12,6 МПа, нагреваясь при этом до 210–230 °С. После сжатия нитрозные газы охлаждают в холодильнике 16 до 155–165 °С. в холодильнике 11 второй ступени до 60–65 °С и подают в абсорбционную колонну 10. На тарелках колонны расположены земеевики для охлаждения кислоты. Сверху в колонну поступает паровой конденсат (Н2O) с температурой не выше 40 °С. Снизу колонны выводится 58–60%-ная азотная кислота; она поступает в продувочную колонну 9 для удаления растворенных в ней оксидов азота и далее направляется в хранилище. Отходящий газ из абсорбционной колонны нагревается в подогревателе (топочном устройстве) 8, смешивается в смесителе 7 с природным газом и подогретый до 480 °С направляется на каталитическую очистку от оксидов азота в реактор. Катализатором очистки служит алюмопалладиевый катализатор АПК-2. После каталитического разложения выхлопные газы, содержащие до 0,008% оксидов азота при температуре 750 °С, поступают в рекуперационную турбину 5, входящую в состав газотурбинного агрегата. Здесь тепловая энергия выхлопных газов преобразуется в механическую с одновременным снижением давления газа до 0,95–1,05МПа. Энергия, вырабатываемая в газовой турбине, используется для привода компрессоров 12 и 23 (нитрозного и воздушного). Производство слабой азотной кислоты под повышенным давлением. В 1960-х годах разработан агрегат по производству азотной кислоты мощностью 120 тыс. т год под давлением 0,716 МПа с использованием высокотемпературной каталитической очистки выхлопных газов, выпускающий продукцию в виде 53-58%-ной HNO3 [1]. При разработке этой схемы были пересмотрены вопросы экономической эффективности производства по схеме АК-72, в результате чего уменьшена мощность установки с 380 тыс. тонн до 120 тыс. тонн в год и снижено давление во всей схеме. В частности, абсорберы работают при давлении 0,5–0,7 МПа. Улучшена схема очистки хвостовых газов [1]. Производство концентрированной азотной кислоты прямым синтезом из оксидов азота. Прямой синтез HNО3основан на взаимодействии жидких оксидов азота с водой и газообразным кислородом под давлением до 5 МПа по уравнению 2N2O4 + O2 + 2H2O → 4HNO3. 100%-ный диоксид азота при атмосферном давлении и температуре 21,5 °С полностью переходит в жидкое состояние. При окислении аммиака полученный NO окисляется в NO2, содержание которого в газовой смеси составляет около 11%. Перевести диоксид азота такой концентрации в жидкое состояние при атмосферном давлении не представляется возможным, поэтому для сжижения оксидов азота применяют повышенное давление. Концентрирование азотной кислоты с помощью водоотнимающих веществ. Получить концентрированную азотную кислоту перегонкой разбавленной кислоты невозможно. При кипении и перегонке разбавленной азотной кислоты ее можно упарить лишь до содержания 68,4 % HNO3 (азеотропная смесь), после чего состав перегоняемой смеси не изменится [1]. В промышленности перегонку разбавленных водных растворов азотной кислоты осуществляют в присутствии водоотнимающих веществ (концентрированная серная кислота, фосфорная кислота, концентрированные растворы нитратов и др.). Применение водоотнимающих веществ дает возможность понизить содержание водяных паров над кипящей смесью и увеличить содержание паров азотной кислоты, при конденсации которых получается 98%-ная HNО3. Технологическая схема концентрирования азотной кислоты с применением серной кислоты показана на рисунке 1.2. Разбавленная азотная кислота из напорного бака 1 подается в колонну 6 через два расходомера 2, включенные параллельно. Один поток кислоты проходит в испаритель 3 и подается в виде смеси жидкости и пара на 10-ю тарелку колонны 6, другой поток без подогрева поступает на вышележащую тарелку [1]. Серная кислота из напорного бака 4 через регулятор 5 подается в верхнюю часть колонны 6 выше ввода холодного потока азотной кислоты. В нижнюю часть колонны вводится острый пар, при нагревании которым из тройной смеси начинает испаряться азотная кислота. Пары азотной кислоты при температуре 70–85 °С, поднимаясь вверх, выходят через штуцер в крышке колонны и поступают в холодильник-конденсатор 7. В этих парах имеются примеси оксидов азота и воды.
Рисунок 1.2 – Схема концентрирования разбавленной азотной кислоты в присутствии серной кислоты: 1, 4 – напорные баки для азотной и серной кислоты; 2 – контрольные фонари; 3 – испаритель разбавленной азотной кислоты; 5 – коробка для регулировании подачи кислоты,;6 – концентрационная колонна, 7 – холодильник конденсатор; 8 – холодильник кислоты, циркулирующей в башне; 9 –вентилятор: 10 – поглотительная башня; 11 – сборник; 12 – насос; 13 – холодильник концентрированной азотной кислоты, 14 – холодильник отработанной серной кислоты В холодильнике-конденсаторе пары азотной кислоты при температуре около 30 °С конденсируются с образованием 98–99%-ной HNО3, при этом оксиды азота частично поглощаются этой кислотой. Концентрированная азотная кислота, содержащая оксиды азота, направляется на две верхние тарелки и проходит их последовательно, причем оксиды выдуваются из раствора парами азотной кислоты, поступающими в конденсатор 7. Несконденсировавшиеся пары азотной кислоты и выделившиеся оксиды азота направляют на абсорбцию в башню 10, орошаемую водой. Полученная 50%-ная кислота поступает в сборник 11 и вновь направляется на концентрирование. Концентрированную азотную кислоту после охлаждения направляют на склад готовой продукции. Отработанная серная кислота, содержащая 65–85% H2SO4, поступает на концентрирование. При концентрировании азотной кислоты с применением 92–93%-ной серной кислоты расход последней значительно сокращается при подаче на концентрирование 59–60%-ной HNO3 вместо 48–50%-ной. Поэтому в некоторых случаях выгодно проводить предварительное концентрирование 50%-ной HNO3 до 60%-ной путем простого упаривания. Большим недостатком концентрирования азотной кислоты с помощью серной кислоты является высокое содержание паров и тумана H2SO4 в выхлопных газах после электрофильтров (0,3–0,8 г/м3 газа). Поэтому серную кислоту заменяют, например, нитратом магния или цинка. Концентрирование азотной кислоты с помощью нитрата магния. Этот способ концентрирования обеспечивает получение чистой концентрированной азотной кислоты без вредных выбросов в атмосферу. Однако у него есть ряд существенных недостатков, не позволяющих использовать такой способ повсеместно. В первую очередь это связано с повышенной по сравнению с другими способами себестоимостью получаемого продукта и проблемы утилизации трудно перерабатываемых твердых отходов [1]. С ростом давления наблюдается снижение выхода оксида азота (II). Поэтому проектирование и сооружение установок с использованием повышенного давления на стадии конверсии аммиака сдерживались. Вместе с тем использование высокого давления при окислении аммиака позволяет повысить производительность агрегата, уменьшить размеры аппаратов. Этот факт в связи со стремлением к увеличению единичной мощности агрегатов приобретает все большее значение. На современных крупных агрегатах производства азотной кислоты процесс окисления аммиака осуществляется под давлением 0,41— 0,73 МПа. Основным условием получения высоких выходов NO под давлением выше атмосферного являются повышение температуры и времени контактирования (увеличение числа сеток). На основании анализа принимаем к проектированию схему производства слабой азотной кислоты мощностью 120 тыс. тонн в год под давлением 0,7 МПа.
|