Политропный процесс. Адиабатным называется процесс, при котором отсутствует теплообмен между системой и окружающей средой Q = 0)
Адиабатным называется процесс, при котором отсутствует теплообмен между системой и окружающей средой
т. е. внешняя работа совершается за счет изменения внутренней энергии сис- темы. Используя выражения (52.1) и (53.4), для произвольной массы газа перепи- шем уравнение (55.1) в виде
Продифференцировав уравнение состояния для идеального газа р V =
Разделив переменные и учитывая, Рис. 85 что С — = [см. (53.8)], найдем
Полученное выражение есть урав- нение адиабатного процесса, называ- емое также уравнением Пуассона. Для перехода к переменным Т, V или р, Т исключим из (55.4) с помощью уравнения Клапейрона — Менделеева pV —- или объем:
(55.6) Выражения (55.4) — (55.6) представ- ляют собой уравнения адиабатного про- цесса. В этих уравнениях безразмерная величина [см. (53.8) и (53.2)] График зависимости между пара- метрами состояния идеального газа при Вычислим работу, совершаемую га- зом в адиабатном процессе. Запишем уравнение (55.1) в виде
(55.8)
Применяя те же приемы, что и при выводе формулы (55.5), выражение (55.8) для работы при адиабатном рас- ширении можно преобразовать к виду
_ М
Работа, совершаемая газом при адиабатном расширении 1 — 2 (опре- деляется тонированной площадью на рис. 85), меньше, чем при изотерми- ческом расширении. Это объясняется тем, что при адиабатном расширении происходит охлаждение газа, тогда как при изотермическом температура поддерживается постоянной за счет притока извне эквивалентного коли- чества теплоты.
Исходя из первого начала термоди- намики при условии постоянства теп- лоемкости
где п —
§56. Обратимые и необратимые процессы. Круговой процесс (цикл) Термодинамический процесс назы- вается обратимым, если он может про- исходить как в прямом, так и в обрат- ном направлении, причем если такой процесс происходит сначала в прямом, а затем в обратном направлении и сис- тема возвращается в исходное состоя- ние, то в окружающей среде и в этой си- стеме не происходит никаких измене- ний. Всякий процесс, не удовлетворя- ющий этим условиям, будет необрати- мым.
мом или обратном направлении. Реальные процессы сопровождают- ся диссипацией энергии (из-за трения, теплопроводности и т.д.), которая нами не обсуждается. Обратимые процес- сы — это идеализацияреальных процес- сов. Их рассмотрение важно по двум причинам: 1) многие процессы в при- роде и технике близки к обратимым; 2) для обратимых процессов термичес- кий коэффициент полезного действия максимален, что позволяет указать пути повышения КПД реальных тепловых двигателей.
Прямой цикл используется в теп- ловых двигателях — периодически действующих двигателях, совершаю- щих работу за счет полученной извне теплоты. Обратный цикл используется в холодильных машинах — периоди- чески действующих установках, в кото- рых за счет работы внешних сил тепло- та переносится к телу с более высокой температурой. В результате кругового процесса си- стема возвращается в исходное состоя- ние и, следовательно, полное изменение внутренней энергии газа равно нулю. Поэтому первое начало термодинами- ки (51.1) для кругового процесса
т. е. работа, совершаемая за цикл, равна количеству полученной извне теплоты. Однако в результате кругового процес- са система может теплоту как получать, так и отдавать, поэтому где Q1 — количество теплоты, получен- ное системой; Q2— количество тепло- ты, отданное системой. Поэтому термический коэффици- ент полезного действия для кругово- го процесса
|

 Q = 0). К адиабатным процессам мож- но отнести все быстропротекающие процессы. Адиабатным процессом, на- пример, можно считать процесс распро- странения звука в среде, так как ско- рость распространения звуковой волны настолько велика, что обмен энергией между волной и средой произойти не успевает. Адиабатные процессы приме- няются в двигателях внутреннего сго- рания (расширение и сжатие горючей смеси в цилиндрах), в холодильных ус- тановках и т.д. Из первого начала тер- модинамики
Q = 0). К адиабатным процессам мож- но отнести все быстропротекающие процессы. Адиабатным процессом, на- пример, можно считать процесс распро- странения звука в среде, так как ско- рость распространения звуковой волны настолько велика, что обмен энергией между волной и средой произойти не успевает. Адиабатные процессы приме- няются в двигателях внутреннего сго- рания (расширение и сжатие горючей смеси в цилиндрах), в холодильных ус- тановках и т.д. Из первого начала тер- модинамики  для адиа- батного процесса следует, что
для адиа- батного процесса следует, что (55.1)
(55.1)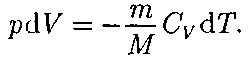 (55.2)
(55.2) получим
получим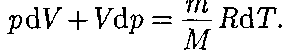 (55.3)
(55.3)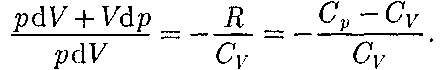 Исключим из (55.2) и (55.3) темпе- ратуру Т:
Исключим из (55.2) и (55.3) темпе- ратуру Т:



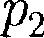 Интегрируя это уравнение в преде- лах от ДО и соответственно от
Интегрируя это уравнение в преде- лах от ДО и соответственно от 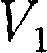 до
до  а затем потенцируя, придем к выра- жению
а затем потенцируя, придем к выра- жению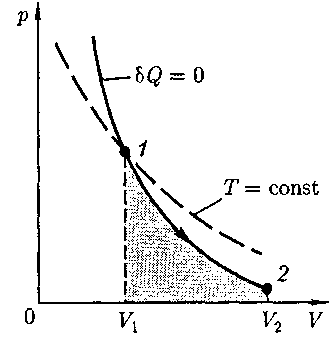 Так как состояния 1 и 2 выбраны произвольно, то можно записать
Так как состояния 1 и 2 выбраны произвольно, то можно записать (55.4)
(55.4)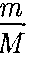 RT соответственно давление
RT соответственно давление (55.5)
(55.5) =.0 называется адиабатой. Адиаба- та в координатах р, V изображается ги- перболой (рис. 85). На рисунке видно, чтоадиабата (р
=.0 называется адиабатой. Адиаба- та в координатах р, V изображается ги- перболой (рис. 85). На рисунке видно, чтоадиабата (р  = const)болеекру-та, чем изотерма
= const)болеекру-та, чем изотерма 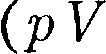 = const). Это объясняется тем, что при адиабатном сжатии увеличение давления газа обус- ловлено не только уменьшением его объема, как при изотермическом сжа- тии, но и повышением температуры.
= const). Это объясняется тем, что при адиабатном сжатии увеличение давления газа обус- ловлено не только уменьшением его объема, как при изотермическом сжа- тии, но и повышением температуры.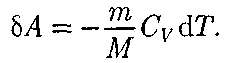
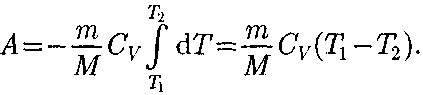
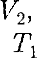
 Если газ адиабатно расширяется от объема
Если газ адиабатно расширяется от объема 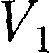 до температура уменьшается от до
до температура уменьшается от до  и работа рас- ширения идеального газа
и работа рас- ширения идеального газа (55.7)
(55.7)
 называется показателем адиабаты (или коэффициентом Пуассона). Для одноатомных газов (Ne,
называется показателем адиабаты (или коэффициентом Пуассона). Для одноатомных газов (Ne,  и др.), дос- таточно хорошо удовлетворяющих ус- ловию идеальности, г = 3, = 1,67. Для двухатомных газов и др.) 5,
и др.), дос- таточно хорошо удовлетворяющих ус- ловию идеальности, г = 3, = 1,67. Для двухатомных газов и др.) 5,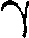
 = 1,4. Значения вычисленные по формуле (55.7), хорошо подтверждают- ся экспериментом.
= 1,4. Значения вычисленные по формуле (55.7), хорошо подтверждают- ся экспериментом.

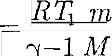
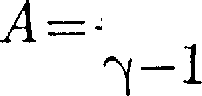
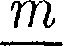
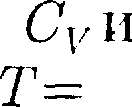 Рассмотренные изохорный, изобар- ный, изотермический и адиабатный процессы имеют общую
Рассмотренные изохорный, изобар- ный, изотермический и адиабатный процессы имеют общую 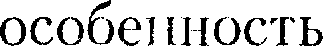 — они происходят при постоянной тепло- емкости. В первых двух процессах теп- лоемкости соответственно равны
— они происходят при постоянной тепло- емкости. В первых двух процессах теп- лоемкости соответственно равны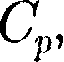 в изотермическом процессе (d 0) теплоемкость равна ±оо, в адиабатном
в изотермическом процессе (d 0) теплоемкость равна ±оо, в адиабатном теплоемкость равна нулю. Про- цесс, в котором теплоемкость остается постоянной, называется политроп- ным.
теплоемкость равна нулю. Про- цесс, в котором теплоемкость остается постоянной, называется политроп- ным.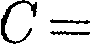 const), можно вывести уравнение политропы:
const), можно вывести уравнение политропы: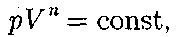 (55.9)
(55.9) — показатель политро-пы. График зависимости между пара- метрами состояния идеального газа при С= const называется политропой. Политропа в координатах р, V— гипер- бола, занимающая промежуточное по- ложение между изотермой и адиаба- той.
— показатель политро-пы. График зависимости между пара- метрами состояния идеального газа при С= const называется политропой. Политропа в координатах р, V— гипер- бола, занимающая промежуточное по- ложение между изотермой и адиаба- той.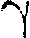
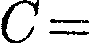
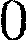
 Очевидно, что при С = 0, п — из (55.9) получается уравнение адиабаты; при
Очевидно, что при С = 0, п — из (55.9) получается уравнение адиабаты; при 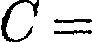 оо, п — 1 — уравнение изотер- мы; при
оо, п — 1 — уравнение изотер- мы; при 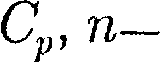 — уравнение изо- бары, при С= Су, п = ±оо — уравнение изохоры. Таким образом, все рассмот- ренные процессы являются частными случаями процесса.
— уравнение изо- бары, при С= Су, п = ±оо — уравнение изохоры. Таким образом, все рассмот- ренные процессы являются частными случаями процесса.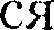 Любой обратимый процесс являет- равновесным. Обратимость равновес- ного процесса, происходящего в систе- ме, следует из того, что ее любое про- межуточное состояние есть состояние термодинамического равновесия; для него «безразлично», идет процесс в пря-
Любой обратимый процесс являет- равновесным. Обратимость равновес- ного процесса, происходящего в систе- ме, следует из того, что ее любое про- межуточное состояние есть состояние термодинамического равновесия; для него «безразлично», идет процесс в пря- Круговым процессом (или циклом) называется процесс, при котором сис- тема, пройдя через ряд состояний, воз- вращается в исходное. На диаграмме p—V равновесный круговой процесс изображается замкнутой кривой (рис. 86). Цикл, совершаемый идеальным га- зом, можно разбить на процессы расши- рения (1 — 2) сжатия (2— 1) газа.
Круговым процессом (или циклом) называется процесс, при котором сис- тема, пройдя через ряд состояний, воз- вращается в исходное. На диаграмме p—V равновесный круговой процесс изображается замкнутой кривой (рис. 86). Цикл, совершаемый идеальным га- зом, можно разбить на процессы расши- рения (1 — 2) сжатия (2— 1) газа.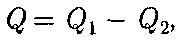
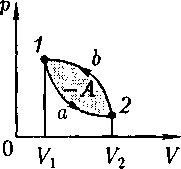
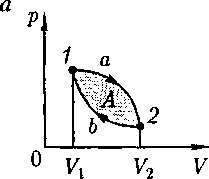 Рис.86
Рис.86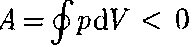 Работа расширения (определяется площадью фигуры
Работа расширения (определяется площадью фигуры  положи- тельна (dV > 0), работа сжатия (опре- деляется площадью фигуры
положи- тельна (dV > 0), работа сжатия (опре- деляется площадью фигуры  отрицательна (dV < 0). Следовательно, работа, совершаемая газом за цикл, опре- деляется площадью, охватываемой зам- кнутой кривой. Если за цикл совершает- ся положительная работа
отрицательна (dV < 0). Следовательно, работа, совершаемая газом за цикл, опре- деляется площадью, охватываемой зам- кнутой кривой. Если за цикл совершает- ся положительная работа  (цикл протекает по часовой стрелке), то он называется прямым (рис. 86, а), если за цикл совершается отрицательная ра- бота. (цикл протекает против часовой стрелки), то он называ- ется обратным (рис. 86, б).
(цикл протекает по часовой стрелке), то он называется прямым (рис. 86, а), если за цикл совершается отрицательная ра- бота. (цикл протекает против часовой стрелки), то он называ- ется обратным (рис. 86, б).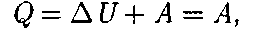 (56.1)
(56.1)



