Дифференциальные уравнения термодинамикиЗапишем внутреннюю энергию U и энтальпию H системы как функции переменных
где Частные производные при дифференциалах
Из равенства перекрестных производных для полного дифференциала получаем
Вычисление частных производных с учетом независимости порядка дифференцирования для непрерывных функций приводит к следующему результату:
Полные дифференциалы внутренней энергии, энтальпии и энтропии принимают вид
Используя полноту этих дифференциалов, т.е. равенство перекрестных производных, находим зависимость теплоемкостей
Функции, частные производные от которых пропорциональны теплоемкостям системы, называются калорическими функциями, а уравнения – калорическими уравнениями состояния. В частности, калорическими функциями являются внутренняя энергия U (T, V) и энтальпия H (T, p).
|

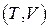 и
и 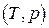 соответственно. Тогда полные дифференциалы этих функций запишутся в виде
соответственно. Тогда полные дифференциалы этих функций запишутся в виде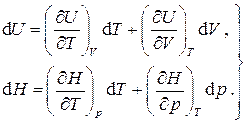 ,
,
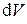 и
и  находятся из того факта, что дифференциал энтропии является полным. Имеем из уравнений Гиббса:
находятся из того факта, что дифференциал энтропии является полным. Имеем из уравнений Гиббса: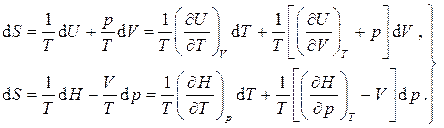
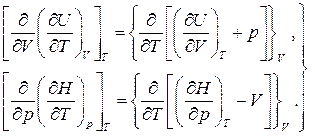
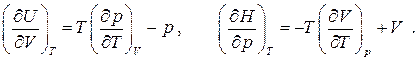
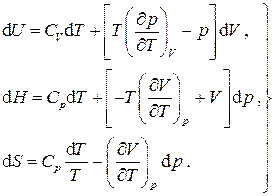
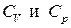 от объема и давления соответственно:
от объема и давления соответственно: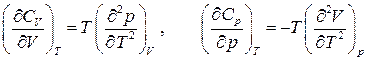 .
.


