Запишите уравнения процессов, идущих на аноде и катоде и уравнение токообразующей реакции (ТОР) при работе Вашего ГЭ.Уравнения процессов, протекающих на аноде и катоде в работающем Cu/Cl2 ГЭ и уравнение токообразующей реакции:
А: Cu → Cu2+ + 2е - окисление К: Cl2 + 2е → 2Cl- - восстановление ТОР: Cu + Cl2 → Cu2+ + 2Cl -
3. Рассчитайте ЭДС (Е0 Э) и максимальную электрическую работу (W) ГЭ при с.с. и 298 К. D f G 0Cu2 = 65,03 кДж/моль; D f G 0 Cl- = -131,17 кДж/моль; D f G 0 Cu= 0; D f G 0 Cl2 = 0 по закону Гесса, рассчитаем энергию Гиббса и ЭДС данного элемента при с.с. и 298 К: D G 0ТОР = D f G 0Cu2 + 2D f G 0 Cl- - D f G 0 Cu - D f G 0 Cl2 = = 65,03+ 2. (-131,17) - 0 - 0 = -197,31 кДж.
Е 0Э = - D G 0ТОР / nF = - (-197310)/ (2. 96500) = 1,022 B.
или Е 0Э= Е 0К - Е 0А = Е 0 Cl2 /Cl - - Е 0 Cu2+/Cu = 1,359- 0,337 = 1,022 В.
Максимальная электрическая работа гальванического элемента при с.с. и 298 К: W = - D G 0ТОР = 197,31 кДж.
4. Рассчитайте ЭДС (Е Э) и максимальную электрическую работу (W) Вашего ГЭ при уменьшении активности потенциалопределяющих ионов анода (a i) в 100 раз (активность ионов катода и парциальное давление газов считать стандартными, Т =298 К). Рассчитаем ЭДС гальванического элемента Cu/Cl2 по уравнению Нернста при 298 К; стандартном состоянии катода (Cl2 /Cl - - электрода,
при уменьшении активности потенциалопределяющих ионов анода (Cu2+/Cu - электрода) в 100 раз, т.е. а Cu2+ =0,01 моль/л: Е Э = 1,022 + Максимальная электрическая работа ГЭ при этих условиях: W = - D G ТОР = Е Э . nF = 1,14.2.96500=74112 Дж=220084 кДж.
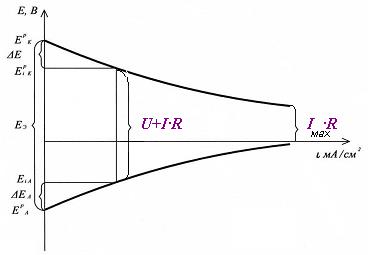
Покажите ход поляризационных кривых в гальваническом элементе. Объясните, почему меняется значение потенциалов анода и катода при работе гальванического элемента, почему напряжение ГЭ не равно ЭДС. Равновесные потенциалы электродов и ЭДС могут быть определены в условиях отсутствия тока в цепи. В работающем ГЭ при прохождении электрического тока уменьшается концентрация исходных реагентов и увеличивается концентрация продуктов реакции. Поэтому в соответствии с уравнением Нернста ЭДС элемента уменьшается. Кроме того возрастает поляризация электродов – потенциал анода становится менее отрицательным, потенциал катода – менее положительным. Помимо этого возникают омические потери. В результате напряжение гальванического элемента меньше ЭДС: U = Е Э - I . R - D Е А -D Е К, U - напряжение; Е Э - ЭДС; I - ток; R – сопротивление; D Е А ,D Е К - поляризация анода, катода. Изменение потенциалов электродов под действием тока отражают поляризационные кривые: ЭДС – максимально возможная разность потенциалов между катодом и анодом, в отсутствие тока в цепи. При протекании тока в ГЭ его напряжение всегда меньше ЭДС, потенциал анода становится более положительным, (поляризация анода D ЕА> 0) потенциал катода – более отрицательным вследствие поляризации, D ЕK< 0.
|

 Cl2= 105 Па/105 Па = 1, а Cl- = 1 моль/л);
Cl2= 105 Па/105 Па = 1, а Cl- = 1 моль/л);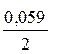 lg
lg  = 1,022+ 0,118 = 1,14В.
= 1,022+ 0,118 = 1,14В.