Детектор. Существует два варианта детектирования в ВЭЖХ: универсальное и селективное.Существует два варианта детектирования в ВЭЖХ: универсальное и селективное. При универсальном детектировании происходит измерение общей характеристики подвижной фазы, например, показателя преломления или электропроводности. В этом случае детектируемое вещество измеряется косвенно по изменению характеристик подвижной фазы. При селективном детектировании происходит измерение характеристик самого детектируемого вещества, например, его поглощение ультрафиолетового излучения, флуоресценции или диффузионного тока. В процессе развития жидкостной хроматографии было испытано более 20 типов различных детекторов, из которых в настоящее время наиболее широко применяются фотометрические, флуоресцентные, рефрактометрические и электрохимические детекторы (табл. 2).
Фотометрические детекторы используются наиболее часто (детектирование с их помощью составляет свыше 70% случаев). Принцип действия фотометрических детекторов основан на применении закона светопоглощения Бугера-Ламберта-Бера. Для измерения светопоглощения подвижной фазы на выходе из колонки используют проточные фотометрические ячейки Z-образной формы (рис. 3). Луч света проходит через проточную ячейку и частично поглощается раствором с анализируемым веществом, поступающим в проточную ячейку из колонки. Для уменьшения размывания хроматографических пиков объем ячейки стараются сделать как можно меньше – от 1 до 10 мкл. Длина оптического пути ячейки составляет 2 – 10 мм. При измерениях в УФ области оптические окна кюветы необходимо изготавливать из кварца. Большинство органических соединений (ароматические и гетероциклические соединения, вещества молекулы которых содержат функциональные группы С=О, С=S, N=O, N=N и сопряженные связи) имеют интенсивные полосы поглощения в диапазоне длин волн 200 – 800 нм, что и определяет широкое распространение фотометрических методов детектирования, в том числе и для анализа лекарственных препаратов. Фотометрические детекторы подразделяют следующим образом: · детекторы с фиксированной длиной волны (фотометры); · детекторы с дискретно изменяемой длиной волны с помощью оптических фильтров (фильтровые фотометры); · спектрофотометрические детекторы, регистрирующие поглощение в определенной области УФ спектра; · спектрофотометрические детекторы на фотодиодных матрицах. Фотометры являются наиболее простым вариантом фотометрических детекторов. Различают фотометры с фиксированной длиной волны и с дискретно изменяемой длиной волны (фильтровые фотометры). Детектирование проводят при фиксированной длине волны (обычно используют длину волны 254 нм, вблизи которой находятся максимумы поглощения всех ароматических и многих других органических веществ). Более удобными являются спектрофотометрические детекторы с плавно изменяемой длиной волны, которые позволяют регистрировать разделяемые вещества по поглощению света при любых длинах волн УФ и видимого диапазона. Для выделения спектральной полосы в этих детекторах используют дифракционные решетки или интерференционные фильтры с заданной шириной спектральной полосы. Спектрофотометрический детектор позволяет снять спектр анализируемого вещества, но только после остановки потока подвижной фазы, при этом сканирование спектра занимает несколько секунд или даже минут в зависимости от диапазона длин волн. Наиболее современными в настоящее время являются спектрофотометрические детекторы с фотодиодной матрицей – диодно-матричные детекторы (ДМД). В традиционных фотометрических детекторах полихроматическое излучение сперва попадает на входную щель монохроматора, а затем монохроматор селективно направляет узкие полосы монохроматического излучения на входную щель. В ДМД полихроматическое излучение сперва подается на проточную ячейку, через которую проходит элюат, а затем световой поток попадает на поверхность монохроматора и делится на монохроматические пучки света, каждый из которых попадает на фотодиодную матрицу, содержащую как правило 316 диодов. При использовании ДМД проба сканируется каждые несколько миллисекунд, т.е. спектральная информация подается практически непрерывно. Информация, полученная с помощью этого детектора, может быть представлена в виде трехмерной диаграммы (рис. 4), что позволяет проверить однородность пика (соответствует ли данный пик одному соединению).
Рис. 4 Трехмерная диаграмма, полученная с помощью ДМД, при определении фенантрена. При работе с ДМД можно зафиксировать спектр каждого компонента и установить максимальное поглощение в конкретной области длин волн. Кроме того, ДМД позволяют проводить количественный анализ, даже если хроматографические пики разрешены не полностью. К недостаткам фотометрических детекторов можно отнести невозможность определения оптически неактивных соединений. Также ограничивает их использование непрозрачность некоторых растворителей по отношению к УФ излучению в интересующей аналитика области длин волн. В основе работы рефрактометрического детектора лежит непрерывная регистрация изменения показателя преломления элюата на выходе из колонки по сравнению с чистым элюентом. В свою очередь, показатель преломления изменяется пропорционально концентрации определяемого вещества. Рефрактометрический детектор является универсальным, и совместим практически с любой подвижной фазой. Он является незаменимым в тех случаях, когда определяемые компоненты не поглощают электромагнитное излучение в УФ и видимой области спектра, не обладают электрохимической активностью и флуоресценцией. Основным недостатком рефрактометрического детектора является низкая чувствительность, которая может быть повышена за счет выбора максимально адекватной подвижной фазы: использованием элюента с очень высоким или очень низким показателем преломления. Кроме того, этот детектор требует термостатирования с точностью до ±0.001°С, не подходит для градиентного элюирования. Флуориметрический детектор использует способность определяемых соединений к люминесценции под различными воздействиями, из которых чаще всего используют облучение электромагнитным излучением. Для определения многих природных соединений, лекарственных препаратов и других физиологически активных веществ обычно используют собственную флуоресценцию. Для детектирования нефлуоресцирующих веществ следует получить их флуоресцирующие производные. Например, аминокислоты, не обладающие собственной флуоресценцией, превращают в флуоресцирующие производные по реакции с дансилхлоридом (5-N,N'-диметиламино-1-нафталинсульфохлоридом): Рис. 5 Дериватизация аминокислот с образование флуоресцирующих производных Чувствительность флуоресцентного детектора примерно в 100 раз превышает чувствительность фотометрических детекторов. Кроме того, флуориметрический детектор значительно селективнее, чем фотометрический, поскольку далеко не все соединения, поглощающие электромагнитное излучение, способны флуоресцировать. При работе с флуориметрическим детектором следует учитывать, что примеси, содержащиеся в элюенте, а также растворенный кислород способны вызывать тушение флуоресценции. Такое же действие оказывают кислородсодержащие растворители. Поэтому перед началом работы с флуориметрическим детектором необходимо убедиться в отсутствии фоновой флуоресценции элюента. Из группы электрохимических детекторов в ВЭЖХ наибольшее распространение получили кондуктометрический и амперометрический детекторы. Кондуктометрический детектор широко применяется в ионной хроматографии. Детектирование основано на измерении электропроводности элюата, которая пропорциональна концентрации ионов. Для подавления фоновой электропроводности элюента часто используют подавляющую колонку. Амперометрический детектор подходит для детектирования всех соединений, способных окисляться или восстанавливаться в диапазоне потенциала, установленного на рабочем электроде. В водном растворе этот диапазон составляет от -0.8 до +1.2 В. К рабочему электроду прикладывают постоянный потенциал, и измеряют предельный диффузионный ток при данном потенциале относительно электрода сравнения. Амперометрический детектор очень чувствительный и селективный. Он используется для определения фенолов, гормонов стресса (адреналина и норадреналина), пестицидов и нитрозоаминов. В настоящее время существуют и другие возможности детектирования в ВЭЖХ – это комбинация ВЭЖХ с масс-спектрометрией для идентификации органических соединений и с атомно-абсорбционной спектрометрией для определения элементов.
2.2. Сорбенты для жидкостной хроматографии 2.2.1 Общая характеристика В классическом варианте хроматографии, как правило, используются сорбенты с частицами диаметром 30 – 200 мкм. На основе таких материалов можно получать колонки эффективностью до нескольких тысяч теоретических тарелок на 1 м длины. Уже такой эффективности было бы достаточно для решения многих аналитических и препаративных задач. Однако существенным недостатком крупнозерновых сорбентов является большая длина пути диффузии внутри зерен, и как следствие, довольно большая продолжительность анализа. Становление ВЭЖХ в значительной мере связано с созданием новых поколений сорбентов с хорошими кинетическими свойствами. Основной путь улучшения кинетических характеристик сорбентов – уменьшение толщины активного слоя. Для достижения этой цели используют два пути: применение поверхностно-пористых сорбентов или уменьшение диаметра частиц обычных объемно-пористых сорбентов. Поверхностно-пористые или пелликулярные сорбенты имеют частицы диаметром около 30 мкм, состоящие из непористого ядра и пористого поверхностного слоя толщиной 1.5 – 2.5 мкм. Колонкам, заполненным поверхностно-пористыми сорбентами, присуще небольшое сопротивление потоку ПФ (в отличие от объемно-пористых сорбентов), однако у них имеется существенный недостаток – очень малая нагрузочная емкость, поскольку лишь небольшой пористый слой участвует в хроматографическом процессе. Поэтому в настоящее время пелликулярные сорбенты применяют лишь в ионной хроматографии или для заполнения предколонок. Объмно-пористые сорбенты для ВЭЖХ представляют собой сферические частицы размером 3 – 10 мкм, пронизанные порами на всю толщину. Благодаря большой удельной поверхности объемно-пористых сорбентов достигается высокая сорбционная емкость, вследствие чего они нашли широкое применение не только для аналитических, но и для препаративных целей.
2.2.2 Материалы для сорбентов В качестве материала для сорбентов в настоящее время в основном используется силикагель, который обладает таким преимуществами как высокая механическая прочность, возможность получения частиц заданного размера с различными размерами пор и разной удельной поверхностью. Его используют в режиме нормально-фазовой хроматографии для разделения полярных соединений, таких как фенолы, альдегиды, амины. Особое место занимают химически модифицированные силикагели (ХМС), которые содержат на своей поверхности различные химически привитые группы. ХМС получают силанизацией – обработкой поверхности силикагеля органическими хлорсиланами: Рис. 6 Схема получения химически модифицированных силикагелей В зависимости от природы радикала R можно получить ХМС различной полярности. В таблице 3 приведены примеры полярных функциональных групп, расположенных в порядке уменьшения полярности, которые наиболее часто применяются при синтезе ХМС.
Такие ХМС используют в качестве сорбентов в основном в варианте нормально-фазовой хроматографии. В качестве неполярных модифицированных сорбентов, применяемых в методе обращенно-фазовой хроматографии, чаще всего используют силикагель с привитыми н -октадецильными (С18) радикалами. Углеводородные радикалы располагаются параллельно друг другу и перпендикулярно поверхности частиц, образуя при этом поверхность в виде щетки:
При силанизации поверхность силикагеля может быть покрыта силанольными группами не более чем на половину (из-за стерических препятствий). Непрореагировавшие остаточные силанольные группы являются сильнополярными и могут адсорбировать из раствора полярные соединения. На хроматограмме это явление появляется в виде появления пиков с размытым задним фронтом. Поэтому остаточные силанольные группы необходимо как можно полнее дезактивировать. Для этого, как правило, используют повторную обработку поверхности силикагеля триметилхлорсиланом, в результате чего силанольные группы превращаются в силоксановые. С18 – силикагель используется в обращено-фазовой хроматографии и предназначен для разделения широкого круга веществ от умеренно- до высокополярных. Кроме того, он обладает высокой селективностью по отношению к гомологам. Также в ОФХ нашли применение сорбенты средней полярности, к которым относятся н -октилсиликагель (С8) и фенилсиликагель (С6Н5). В качестве радикала R могут выступать различные ионогенные группы, такие как –SO3H, -N+R3 и др. В результате модифицирования силикагеля такими группами получаются различные ионообменники. Новые возможности для разделения органических веществ открываются в результате привития к силикагелю оптически активных макроциклических соединений. Например, привитые краун-эфиры оказались эффективными хиральными фазами, позволяющие добиться полного разделения энантиомеров аминокислот и сложных эфиров. Основным недостатком сорбентов на основе силикагеля является их малая устойчивость в кислых и щелочных растворах. Так, ХМС устойчивы в полярных подвижных фазах в интервале рН от 2 до 8. При рН < 2 происходит гидролиз силоксановых связей, что приводит к потере привитой фазы. При рН > 8 силикагель растворяется, вследствие чего сорбент разрушается, и хроматографическая колонка выходит из строя. Для разделения веществ в сильнокислых или сильнощелочных растворах применяют сорбенты на основе различных полимеров, таких как полистирол, дивинилбензол, полиметилакрилат. Наибольшее распространение такие сорбенты получили в методе ионообменной хроматографии. 2.3. Растворители и подвижные фазы 2.3.1 Общая характеристика Прежде всего, необходимо определить два термина: растворитель и подвижная фаза. Термин «растворитель» используется всякий раз при рассмотрении физических или химических свойств чистых жидкостей. Термин «подвижная фаза» подчеркивает использование растворителей или их смесей в хроматографической системе. В отличие от газовой хроматографии, в которой подвижная фаза химически инертна и выполняет лишь роль переносчика, в жидкостной хроматографии она играет активную роль. Молекулы подвижной фазы участвуют в физико-химических взаимодействиях с другими компонентами системы: молекулами разделяемых веществ и частицами неподвижной фазы. Более того, во многих случаях компоненты подвижной фазы способны к прочной сорбции, что приводит к образованию на поверхности адсорбента слоя, существенно изменяющего свойства неподвижной фазы. Поэтому удерживание разделяемых веществ определяется характером подвижной фазы ничуть не менее чем характером сорбента. Нередко заменой одного растворителя другим можно изменить фактор удерживания в 1000 – 10000 раз. Кроме того, выбор подвижной фазы оказывает большое влияние на такие параметры, как селективность разделения, уровень давления в системе и фоновый сигнал детектора. Поэтому при выборе подвижной фазы важно учитывать как ее физические и химические свойства в целом, так и физико-химические свойства отдельных растворителей. Растворители, используемые для приготовления подвижной фазы, должны растворять анализируемую пробу; обладать небольшой вязкостью (до 1.5 сП), что обеспечивает высокие коэффициенты диффузии компонентов анализируемой пробы и небольшое падение давления в системе; обладать небольшой летучестью (в противном случае возможно изменение состава ПФ в ходе хроматографирования, что приводит к невоспроизводимости величин удерживания). Кроме того, растворители должны быть инертны по отношению ко всем частям хроматографа, безопасны и по возможности дешевы. Определенные требования к растворителям предъявляет используемый способ детектирования. Поскольку в большинстве случаев используются фотометрические детекторы, важное значение имеет такой параметр как УФ граница прозрачности растворителя, представляющий собой длину волны, при которой оптическая плотность растворителя в кювете длиной 10 мм (при использовании в качестве сравнения воздуха) равна единице. Примерные диапазоны прозрачности для разных классов растворителей приведены в таблице 4.
УФ граница прозрачности показывает, насколько растворитель пригоден для работы при выбранной длине волны. В целом, растворитель с УФ границей прозрачности большей, чем используемая в анализе длина волны, дает высокую фоновую оптическую плотность, что исключает его применение. Например, высокий объемный процент спирта в подвижной фазе не рекомендуется использовать при λ < 220 нм, и конечно, он совершенно недопустим при λ < 205 нм. Исключение составляет тот случай, когда растворитель используют в качестве не основного, а дополнительного компонента подвижной фазы, например, в количестве 10 об. % или менее. В таких случаях работа в области УФ границы прозрачности для 10% этого компонента приводит к фоновой оптической плотности, равной лишь 0.1. Часто это является допустимым, несмотря на увеличение уровня шумов, уменьшение линейного динамического диапазона и снижение чувствительности. Если в растворителе имеются примеси, общая оптическая плотность при данной длине волны представляет собой сумму вкладов каждого компонента:
Следовательно, даже небольшие концентрации примесей с большими значениями молярного коэффициента поглощения будут вносить свой вклад в значение оптической плотности. Поскольку содержание примесей часто не контролируется даже для растворителей квалификации «химически чистый», рекомендуется применять растворители специальных квалификаций – «для ВЭЖХ» или «для спектроскопии».
2.3.2 Характеристика элюирующей способности растворителя При разделении многокомпонентных смесей за приемлемое время одна подвижная фаза в качестве элюента не может разделить все компоненты пробы (особенно это касается смесей, содержащих соединения с резко различающейся полярностью). В этом случае применяют метод градиентного элюирования, в котором необходима подвижная фаза с возрастающей элюирующей способностью. На элюирующую способность растворителя влияют следующие основные факторы: · взаимодействие между молекулами подвижной фазы и хроматографируемого соединения; · взаимодействие между адсорбированными молекулами хроматографируемого соединения и молекулами подвижной фазы; · взаимодействие между адсорбированными молекулами подвижной фазы и неподвижной фазой. В адсорбционной хроматографии для характеристики элюирующей сопосбности растворителя используют понятие элюирующая сила εо. Данная величина показывает, во сколько раз энергия сорбции данного элюента на данном сорбенте больше, чем энергия сорбции элюента, выбранного в качестве стандарта (н -пентана). Для получения значений элюирующей силы для каждого растворителя, были найдены средние времена удерживания большого числа растворенных веществ на конкретных сорбентах (обычно силикагеле и оксиде алюминия). В табл. 5 приведены значения εо для некоторых растворителей на ряде неподвижных фаз.
Расположение растворителей в соответствии с возрастанием их элюирующей силы называют элюотропным рядом. Эти ряды являются одним из первых наборов данных, используемых для оценки силы растворителя по его влиянию на удерживание растворенных веществ. При сравнении элюирующей силы двух растворителей слабым называют растворитель, дающий большее время удерживания, тогда как сильным – растворитель, дающий меньшее время удерживания. Например, на силикагеле, для которого εо находится в диапазоне от 0 до 1, гексан с низким значением εо (0.01) является очень слабым растворителем, в то время как метанол с большим значением εо (0.95) – очень сильным растворителем. В целом, связь между εо и удерживанием такова, что с ростом величины элюирующей силы, удерживание растворенных веществ уменьшается. Более конкретно можно сказать, что увеличение εо на 0.05 уменьшает фактор удерживания k в 2 – 4 раза, и, наоборот, при уменьшении εо на 0.05 k увеличивается в 2 – 4 раза. В распределительной хроматографии силу растворителя обычно характеризуют величиной полярности Р'. В нормально-фазовом варианте хроматографии с увеличением полярности растворителя его сила растет, а в обращенно-фазовом варианте – убывает. Для расчета полярности смеси растворителей в первом приближении индексы полярности индивидуальных растворителей суммируются:
где φ – объемная доля растворителя. Например, для смеси, состоящей на 70% из воды и 30% СН3ОН, полярность будет равна
3. Характеристика отдельных видов колоночной жидкостной хроматографии Хроматографическое разделение в жидкостной хроматографии может быть обусловлено различными процессами: адсорбцией, распределением веществ между двумя несмешивающимися жидкими фазами, ионным обменом, распределением молекул в соответствии с их размерами и т.д. Выделить преобладающий процесс часто бывает сложно или невозможно, поскольку механизм удерживания в ЖХ часто бывает смешанным. что создает некоторые проблемы в изложении материала. В большей степени это утверждение относится к адсорбционной и распределительной хроматографии. Например, в отечественной литературе хроматографию на ХМС, как правило, относят к адсорбционному варианту, полагая, что разделение веществ происходит за счет различной адсорбируемости. В иностранной литературе данный вид хроматографии относят к распределительному варианту, полагая, что привитый слой способен удерживать за счет адсорбции слой жидкой фазы, обогащенной менее полярным растворителем из подвижной фазы, и разделение происходит за счет распределения компонентов между двумя несмешивающимися жидкостями. В нашей книге мы будем придерживаться второго варианта.
3.1. Адсорбционная хроматография В адсорбционном варианте жидкостной хроматографии удерживание веществ обусловлено процессом адсорбции на поверхности твердого адсорбента, которым обычно служит силикагель или оксид алюминия. Распределение веществ между подвижной и неподвижной фазами происходит за счет взаимодействий двух видов: неспецифических (дисперсионных, индукционных, ориентационных) и специфических (например, образование водородных связей с адсорбентом), вносящих основной вклад в величины удерживания. В качестве подвижных фаз используют органические растворители, такие как н -алканы, дихлорметан, изооктан, а также их смеси друг с другом. Поскольку подвижная фаза, как правило, обладает меньшей полярностью чем адсорбент, то адсорбционную хроматографию обычно рассматривают как вариант нормально-фазовой хроматографии. Процессы адсорбции локализованы на активных центрах поверхности адсорбента. Сильнополярные молекулы, такие как вода, необратимо адсорбируется на этих центрах и, таким образом, дезактивируют поверхность адсорбента. Поэтому в адсорбционной хроматографии следует тщательно контролировать содержание воды в используемых растворителях. Для облегчения выбора подвижной фазы установлены некоторые эмпирические правила, характеризующие адсорбцию веществ. Так, установлено, что сорбция, как правило, увеличивается с увеличением в молекуле числа кратных связей и ОН-групп, т.е. с увеличением полярности соединений. Например, для силикагеля или оксида алюминия адсорбция, а, следовательно, и времена удерживания для различных классов веществ в целом возрастают в ряду: алканы < алкены < ароматические УВ < галогенпроизводные УВ <; < простые эфиры < нитросоединения < сложные эфиры ≈ альдегиды ≈;
|

 Рис. 3Проточная фотометрическая ячейка для фотометрического детектирования в ВЭЖХ
Рис. 3Проточная фотометрическая ячейка для фотометрического детектирования в ВЭЖХ

 .
.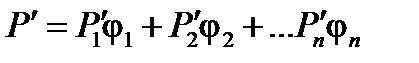 ,
, .
.


