Важнейшие даты до ВОВБСДК содержит сложный сфинктерный аппарат, состоящий из мощного циркулярного мышечного слоя, расположенного вокруг устья общего желчного протока, из менее мощного мышечного слоя вокруг устья главного панкреатического протока, а также из циркулярно и продольно идущих волокон вокруг ампулы. Функционирование мышечного образования в дистальном отделе общего желчного протока (ОЖП) на уровне БСДК - так называемого сфинктера Одди, регулирующего темп истечения панкреатического экскрета и желчи - имеет значение для поступления этих секретов в двенадцатиперстную кишку. БСДК работает по принципу отсасывающей помпы, ритмично открываясь каждые 6-12 с. Период расслабления ампулы зависит от объёма поступающего сока: он может удлиняться вдвое. Ритмичное функционирование сфинктерного аппарата БСДК предупреждает поступление дуоденального содержимого в протоки, а также желчи в проток поджелудочной железы. В 30% случаев на 3-4 см выше БСДК открывается дополнительный проток поджелудочной железы, называемый санториниевым. Он, как правило, связан анастомозом с протоком поджелудочной железы, чем и объясняется, наряду с анатомическими вариантами, что нет 100% вероятности развития острого панкреатита при блокаде БСДК камнем, рубцом или опухолью. Анатомически взаимоотношения конечных отделов общего желчного протока и протока поджелудочной железы могут быть различными. По данным A. Robson (1904), различают четыре типа взаимоотношений:
Поджелудочная железа и забрюшинные отделы двенадцатиперстной кишки залегают в ложе из фасций брюшинного происхождения. Заднюю стенку его составляют фасция Тольдта, а переднюю - наслоенная брыжейка (или её производные) толстой кишки. Соединительнотканная клетчатка в этом ложе рыхло соединяет фасциальные листки, что способствует быстрому распространению экссудата при деструктивном панкреатите в пределах самого ложа, а также в сообщающийся с ним правый и левый параколон. Форма затёков зависит от особенностей расположения фасциальных листков. При локализации очага деструкции в головке поджелудочной железы экссудат, задержавшись сначала в пределах панкреатодуоденального комплекса, затем может без особого препятствия опускаться в правый параколон, то есть в щель, расположенную между фасцией Тольдта сзади и восходящей ободочной кишкой с её брыжейкой спереди. При локализации очага деструкции в средней части тела поджелудочной железы экссудат может накапливаться в пределах средней части корня брыжейки поперечной ободочной кишки и начала брыжейки тонкой кишки. Распространению в правый параколон в этом случае препятствует забрюшинная связка двенадцатиперстной кишки (Бондарчук О.И., 1992). При локализации очага деструкции в левой части поджелудочной железы экссудат может распространяться в левый параколон. При поражении всей железы экссудат может занимать все эти пространства. Следует различать два слоя параколон: передний и задний. Они разделены фасцией Тольдта. Задний описан Стромбергом, носит его имя и содержит жировую клетчатку. Передний параколон описал О.И. Бондарчук (1992). Передний параколон ограничен сзади фасцией Тольдта, а спереди восходящей или нисходящей ободочной кишкой с их фиксированными брыжейками. Он заполнен рыхлой соединительнотканной клетчаткой и в отличие от заднего параколона сообщается с ложем, в котором залегает двенадцатиперстная кишка и поджелудочная железа. Именно поэтому имеется беспрепятственная возможность распространения экссудата в передний параколон. Если рассматривать фасциальные листки панкреатодуоденальной зоны, идя сзади наперёд, то можно определить следующий порядок их залегания:
Кроме описанных фасциальных образований, следует учитывать наличие нижней забрюшинной связки двенадцатиперстной кишки, натянутой между нижней поверхностью нижней горизонтальной части кишки и корнем брыжейки тонкой кишки. Эта треугольной формы связка со свободным правым краем заполняет угол между нижней частью двенадцатиперстной кишки и верхней частью тонкой кишки. М.И. Прудков и A.M. Шулутко (2001) из интересов хирургической тактики предлагают клетчаточное пространство делить на несколько зон: перипанкреатическая клетчатка, непосредственно контактирующая с поджелудочной железой, и ретроперитонеальное клетчаточное пространство, условно разделённое позвоночником и брыжейкой ободочной кишки на левый верхний квадрант, левый нижний квадрант, правый верхний квадрант, правый нижний квадрант и их комбинации. Наиболее сложный по форме - правый верхний квадрант, включающий в себя клетчатку, расположенную вокруг головки поджелудочной железы, по ходу печёночно-дуоденальной связки, а также узкое забрюшинное пространство под малым сальником между левой долей печени и позвоночником. А.Г. Кригер (2004) предлагает делить забрюшинную клетчатку на 6 зон:
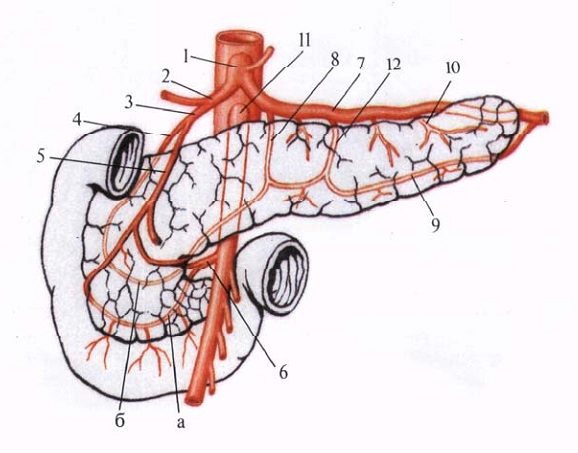
Поджелудочная железа не имеет собственных крупных артериальных сосудов. Она кровоснабжается многочисленными ветвями от печёночной, селезёночной и верхней брыжеечной артерий. Источники кровоснабжения разные для головки, тела и хвоста. От печёночной артерии у левого края печёночно-дуоденальной связки отходит желудочно-двенадцатиперстная артерия (a. gastroduodenalis), которая делится на правую желудочно-сальниковую артерию (a. gastroepiploica dextra) и верхнюю панкреатодуоденальную артерию (a. pancreaticoduodenalis superior), которая уже в свою очередь делится на две ветви и образует полную дугу по передней и задней поверхности поджелудочной железы. Нижняя панкреатодуоденальная артерия отходит от верхней брыжеечной артерии (a. mesenterica superior) и также имеет переднюю и заднюю ветви. Эти артерии окружают головку поджелудочной железы. Тело и хвост кровоснабжаются веточками от селезёночной артерии. Кровь оттекает по венам в систему воротной вены. Вены впадают или непосредственно в воротную вену, или в селезёночную и верхнюю брыжеечную вены, идущие параллельно одноимённым артериям. Расположение поджелудочной железы, тесная связь её протоковой системы с желчевыводящей системой, прилегание к желудку и двенадцатиперстной кишке, крупным ветвям чревного ствола и воротной вены создают условия для вовлечения этих образований в патологические процессы, происходящие в органе. И наоборот, расстройства кровообращения, возникающие в прилежащих сосудистых регионах, неизбежно сказываются на структуре и функции поджелудочной железы.
Кровоснабжение поджелудочной железы (полусхематично). Лимфатические сосуды поджелудочной железы анастомозируют с лимфатическими сосудами двенадцатиперстной кишки, желчного пузыря и общего желчного протока, что играет роль в переходе инфекции с одного органа на другой. Обширная сеть лимфатических сосудов, дренирующих интерстиций поджелудочной железы непосредственно в систему грудного протока, создаёт значительное поле резорбции. Из него продукты распада тканей, биологически активные вещества и несекретированные в кишку ферменты поджелудочной железы быстро попадают в циркулирующую кровь, повреждая лёгкие и воздействуя на микроциркуляцию малого и большого круга кровообращения. Другой путь резорбции - через систему воротной вены. Именно эти особенности обеспечивают быстрое развитие тяжёлой эндогенной интоксикации, которая определяет приоритетные органные повреждения (лёгкие, печень, миокард) и общие реакции организма в ответ на поступление факторов панкреатической агрессии. Иннервация поджелудочной железы осуществляется парасимпатической и симпатической нервной системой, обеспечивая непосредственное участие нервных влияний на функции этого органа. Симпатические волокна участвуют преимущественно в регуляции тонуса кровеносных сосудов поджелудочной железы, а парасимпатические - в её экзокринной деятельности, прежде всего в выделении ферментов. В поджелудочной железе не проявляется антагонистического влияния симпатической и парасимпатической нервной систем. Обилие нервных образований, объединяемых в так называемое чревное, или солнечное, сплетение (plexus coeliacus), расположенное сразу за железой, создаёт возможность интенсивной ноцицептивной импульсации, нейровегетативных и гемодинамических расстройств, моторно-эвакуаторных нарушений желудка и кишечника. Внешнесекреторная, или экзокринная, деятельность поджелудочной железы сводится к секреции панкреатического сока, богатого ферментами и бикарбонатами, что обеспечивает расщепление пищи до частиц, способных всасываться в кишечнике. Секрецию разделяют на экболическую (секреция ферментов и аминокислот) и гидрокинетическую (секреция воды, бикарбонатов, хлоридов и других электролитов). В целом экзокринная деятельность проявляется выделением в двенадцатиперстную кишку до 1,5-2 л панкреатического сока, имеющего основную реакцию рН 8,4-8,8 и содержащего 15 ферментов, которые могут обеспечить переваривание всех питательных веществ, поступающих с пищей: протеолитические (эндопептидазы: трипсин, химотрипсин, эластаза, коллагеназа, промежуточная эндопептидаза; экзопептидазы: карбоксипептидаза А и Б, аминопептидаза; нуклеазы: рибонуклеаза, дезоксирибонуклеаза), липолитические (липаза, фосфолипаза А и В, холестеролэстераза, липопротеинлипаза, эстеразы), гликолитические (а-амилаза). Секреция воды, бикарбонатов и основных ферментов поджелудочной железы (амилазы, липазы, трипсина) регулируется либо нейровегетативным путём - через парасимпатическую иннервацию (система блуждающего нерва), либо гуморальным - под действием энтерогормонов. Поступление желудочного сока, содержащего соляную кислоту, в двенадцатиперстную кишку резко возбуждает выделение панкреатического сока, что объясняется образованием в слизистой оболочке двенадцатиперстной кишки секретина, который вызывает выделение жидкой части поджелудочного сока и бикарбонатов и потенцирует действие другого энтерогормона - холецистокинина (панкреозимина), который в свою очередь стимулирует секрецию и выделение ферментов. Алиментарная активация секреции холецистокинин-панкреозимина под влиянием белков и жиров происходит также через слизистую оболочку двенадцатиперстной кишки. Действие этого энтерогормона осуществляется его прямым влиянием на ацинарные клетки и трофическим воздействием на поджелудочную железу. Наконец, на поджелудочную железу оказывает стимулирующее влияние пептидный гормон гастрин, который вырабатывается в норме в светлых клетках антрального отдела желудка. Действие гастрина осуществляется в основном опосредованно через стимуляцию секреции соляной кислоты, он, подобно холецистокинин-панкреозимину, улучшает трофику поджелудочной железы. Ферменты образуются в ацинарных клетках, жидкая часть сока и электролиты вырабатываются клетками протоков, а мукоидная жидкость - слизистыми клетками протока поджелудочной железы. Из клеток ферменты поступают в межклеточные пространства дольки, в систему протоков, а также в кровь. Активность ферментов, поступающих в кровь, в нормальных условиях имеет постоянное значение. Поджелудочная железа вырабатывает и антиферменты (ингибиторы ферментов), принимающие участие в регуляции активности панкреатического сока. В двенадцатиперстную кишку протеолитические ферменты поступают в неактивной фазе. Трипсиноген активизируется энтерокиназой, выделяемой слизистой оболочкой двенадцатиперстной кишки и переходит в активный трипсин. Активизируют трипсин также соли кальция, бактерии и цитокиназа, выделяемая погибшими и повреждёнными клетками. Химотрипсиноген и карбоксипептидаза активизируется только в присутствии трипсина. Липаза выделяется тоже в неактивном состоянии. Под влиянием желчи и желчных кислот она становится активной и расщепляет нейтральные жиры на жирные кислоты и глицерин. Амилаза выделяется в активном состоянии. Она участвует в переваривании углеводов. Амилаза вырабатывается не только поджелудочной железой, но также слюнными и потовыми железами, печенью и лёгочными альвеолами. Протеолитические ферменты (протеазы) не только участвуют в пищеварении, но и обладают кининогеназным действием, вызывая образование вазоактивных полипептидов (кининов) из плазменных и тканевых кининогенов. Кининовая система осуществляет гуморальную регуляцию гемодинамики, свёртывания крови, фибринолиза, секреторного процесса и функции почек. Функция ферментов строго специфична. Панкреатический сок начинает интенсивно выделяться в двенадцатиперстную кишку примерно через 2-5 мин после еды. Наибольшее напряжение секреторной деятельности железы возникает в период пищеварения, примерно через 1-3 ч после приёма пищи, чему предшествует увеличение кровенаполнения поджелудочной железы. Эти обстоятельства имеют большое значение в патогенезе острого панкреатита. Голодание приводит к снижению объёма сока и концентрации в нём ферментов. Работами академика И.П. Павлова и его учениками было установлено, что различная по составу пища вызывает выделение разнообразного по объёму и содержанию ферментов панкреатического сока. Наиболее сильным возбудителем панкреатической секреции служит соляная кислота, а также другие кислоты, причём отделение сока тем больше, чем выше концентрация кислоты. Желудочное содержимое с высокой кислотностью, поступая в двенадцатиперстную кишку, будет давать более обильную панкреатическую секрецию, чем желудочное содержимое с пониженной кислотностью. С учётом этой закономерности при развитии ОП для создания функционального покоя поджелудочной железы используется активная антацидная терапия блокаторами Н2-рецепторов и/или ингибиторами Н+-, К+-АТФазы. Эндокринная деятельность поджелудочной железы в основном реализуется в островках Лангерханса, расположенных большей частью в её хвосте. Форма островков чаще шаровидная. У взрослого человека их поперечник составляет 120-600 мкм, количество - в среднем около 1,5 млн, суммарная масса - 1-3,5% всей массы поджелудочной железы. Островки состоят из нескольких вариантов клеток, окружены соединительно-тканной оболочкой, обильно снабжены кровеносными капиллярами и нервными волокнами. Бета-клетки островков выделяют гормон инсулин, альфа-клетки - глюкагон, D-клетки вырабатывают соматостатин, РР-клетки - панкреатический полипептид. Вырабатываются также липокаин и калликреин. Инсулин снижает концентрацию глюкозы в крови, способствует отложению гликогена в печени, поглощению его тканями. Глюкагон - антагонист инсулина, он вызывает распад гликогена в печени и выделение глюкозы в кровь. Секреция их определяется концентрацией глюкозы в крови. Липокаин регулирует жировой обмен и отложение жира в печени; калликреин - сосудистый гормон, который принимает участие в регуляции кровообращения: расширяет сосуды, снижает артериальное давление, увеличивает минутный объём сердца. Некоторые авторы относят калликреин к ферментам протеазам и называют его фермент-гормоном. Природа и место выработки, а также роль липокаина и калликреина ещё окончательно не расшифрованы, но связь их с функцией поджелудочной железы очевидна. Регуляция секреторной функции поджелудочной железы осуществляется тремя взаимосвязанными механизмами: интрацеллюлярным, нервным и гормональным. Нервные и гормональные механизмы реализуются в три фазы секреции панкреатического сока: сложнорефлекторную, желудочную и кишечную. Условнорефлекторными раздражителями секреции служат вид и запах пищи, безусловнорефлекторными - процесс жевания и глотания. Желудочная фаза секреции связана с попаданием пищи в желудок. Раздражение и растяжение его, особенно пилорической части, способствует выделению поджелудочной железой воды и ферментов. Связано это с действием гастрина, секретируемого слизистой оболочкой желудка. Кишечная фаза обеспечивается гуморальными факторами: секретином и холецистокинином (панкреозимином). Они выделяются слизистой оболочкой проксимальных отделов тонкой кишки. Сложные взаимоотношения между выделяемыми поджелудочной железой ферментами, проферментами, ингибиторами и стимуляторами при развитии острого панкреатита создают сложную, ещё недостаточно изученную реакцию («метаболический кошмар»), что приводит не только к глубоким нарушениям процессов пищеварения и обмена веществ, но и к самоперевариванию ткани железы и окружающих тканей и органов, вызывающих необратимые, трудно поддающиеся коррекции изменения.
Важнейшие даты до ВОВ 1939 год 10–21 марта — В Москве состоялся XVIII съезд ВКП(б).
|