Уравнения Лайнуивера–Бэрка
10. Механизмы ингибирования. Специфическое регулирование ферм. активности достигается использованием в клетке м-л эффекторов, ускоряющих либо ингибирующих ферм. катализ. Неспецифическое регулирование происходит путем изменения физ-хим условий среды. Регуляция ферм. активности может достигатся также путем 1)экспрессии генов 2)фосфорилирования и дефосфорилирования. Типы ингибиторов:1) конкурентный тип - конкурирует за связывание с субстратом 2) неконкурентный - не конкурирует с субстратом, не изменяет Кm 3) бесконкурентный - в одинаковой степени уменьшает Км и Vmax Аллостерические регуляторы - это регуляторы взаимод. с ферментом в центре отличном от активного. Энергия активации -это энергия необхадимая для достижения активированного состояния.(тот избыток энергии которым они должны обладать чтобы вступить в реакцию. Фермент снижает Еа увеличивая число активирующих м-л,становящихся реакционно способными на более низком энергетическом уровне (характерно наличие 2 переходных состояний ES и EP) E+S↔ES→EX→EP→E+P
11 Ст-ра и ф-ция гемоглобина В 1968 г Перутц впервые получил рентгеноструктурные изображения молекулы гемоглобина. Молекула Нb состоит из 4-х субъединиц (2-х альфа и 2-х бетта), между которыми нах. полость, в которой связываются молекулы эффектора(2,3 ДФГ - дифосфоглицерат).Каждая субъединица содержит 4 ферропротопорфирина. Нb заключен в эритроциты для защиты белка от окисления, предотвращения вымывания белка почками, повышения концентрации эффектора. М-лы Hb могут состоять в неск. состояниях:1)оксигемоглобин 2)дезоксигемоглобин 3)метгемоглобин 4)карбоксигемоглобин 5)нитрозогемоглобин. В организме взаимодействие с кислородом регулируется на нескольких уровнях: 1. На атомарном (специфическое лигандирование иона Fe ll молекулой О2). 2. На молекулярном (конформация молекулы Нb контролирует связывание молекулы О2). 3. На клеточном (эритроцит обеспечивает циркулирование Нb в русле крови, повышает концентрацию регуляторов и эритроцит предотвращает необратимое окисление Нb). 4. На тканевом (изменяя скорость кровотока). Ион Fe ll в молекуле Нb образует 6 координационных связей, из которых 4 – с атомами азота перрольных колец гемо, 1- с атомом азота гистидина (под плоскостью гемо), а 6-е положение занимает координационная связь с молекулой О2.
Свойство Нb – высокое сродство к О2. 1г Нb присоединяет 1,34 – 1,36 мл О2. Функция белковой глобулы Нb сводится к передачи информации об обеспеченности ор-ма О2 к центрам связвания О2, а ткже к защите порфириновых циклов. Взаимодействие Hb с О2 протекает кооперативно. Степень кооперативности процесса определяется взаимодействием активных центров в м-ле белка и может быть рассчитано по ур-нию Хилла: lgY/1-Y=n lgPo2/P50
12 Ст-ра НК Структура и функции НК были выделены в конце 19 века Фридриком Мишером НК явл. полимерами нуклеотидов связанных фосфодиэфирной связью. Нуклеотид явл монофосфоридным эфиром нуклеотидов. Первичная структура нуклеиновых кислот – это последовательность нуклеотидов в молекуле НК. Нуклеотид – это фосфолированный нуклеозид. Нуклеотид = сахар + остаток фосфорной кислоты + азотистое основание. (Нуклеотид = нуклеозид монофосфат) Состав нуклеиновых кислот: - Нуклеиновые кислоты - полимеры, построенные из нуклеотидов, соединенных между собой фосфодиэфирными связями. - Нуклеотиды состоят из остатков азотистого основания, пентозы и фосфорной кислоты. -Различают пиримидиновые (пиримидины) и пуриновые (пурины) основания. -В состав ДНК входят тимин, цитозин, аденин и гуанин -В состав РНК - урацил цитозин, аденин и гуанин -НК содержат пентозы Азотистые основания представляют 2 класса: пиримидины (Т, Ц, У); пурины (А, Г). В перв. структуре мол. ДНК нуклеотиды связываются между собой фосфодиэфирными мостиками, которые связывают 5/ гидроксильную группу одного нуклеотида и 3/ гидроксильную группу другого нуклеотида, т.о. остов молекулы ДНК представляет сахар остаток фосфорной кислоты. Сравнительный анализ стр-ра белка и НК
Исследования Э.Чаргаффа и других ученых, сделавших следующие выводы:1)нуклеотидный состав ДНК разных тканей одного и того же вида одинаков;2)нуклеотидный состав ДНК у разных видов различен;3)нуклеотидный состав не зависит от возраста и питания;4)в составе ДНК число остатков аденина всегда равно числу остатков тимина, а число остатков гуанина равно числу остатков цитозина: А + Г = Т + С
13. Вторичная структура ДНК. В1944 г Эвери, МакЛеод, Маккарти доказали что ДНК – носители генетической информации. 1953 – Уотсон и Крик предложили теорию двойной спирали, которая позволяла объяснить механизмы хранения, трансформации и реализации генетической информации. Нуклеотиды связаны в молекулы ДНК фосфорноэфирной связью. Взаимодействие двух полинуклеотидных цепочек молекулы ДНК обеспечивается комплементарностью (соответствие азотистых основании в одной цепочке азотистым основаниям в другой Т=А, Г≡ Ц). Основную роль в этом играет водородные связи. же важную роль играют гидрофобн взаимод-я, стэкинг взаим-я дипольные взаимодействия p–связей. Молекула ДНК п редставляет двойную правозакрученную спираль. При этом плоскости азотистых оснований лежат перпендикулярно оси спирали.На внешней стороне двойной спирали расположены остатки дезоксирибозы и фосфорной кислоты. Полиморфизм стр-ра молек ДНК. Полиморфизм – это разнообразие формы молек ДНК. Стандартн конформация мол-лы ДНК – это В конформация (Уотсон-Криковская двойная спираль – на один виток спирали приходится 10 пар основании). Основание распологается перпендикулярно оси спирали на растоян 0,36 нм. А-конформация получ из В-конформац при ее дегидротации (11пар оснований приходится на 1 виток). Z-конформац – это левозакрученная спираль (12 пар оснований).Одна из важнейших задач – анал-з нуклеотид последоват. мол-ле ДНК. С-тип (на виток 9,33 пар оснований). Стр-ра ДНК 2-ая спираль объесняет 3 основн. способа реализации информации: репликация (копирование, удвоение мол. ДНК) транскрипция (переписывание), трансляция. Денатурация (потеря нативной третичной структуры, связанной с нарушением связей) происходит при действии химических факторов (мочевина, кислота, щелочь) и физических факторов (температура). Денатурированный белок приобретает свою нативную структуру - ренатурация. Денатурация при действии температуры – плавление ДНК. Важной физико-химич хар-кой мол-лы ДНК явл температура плавления ДНК. Тпл завис от нуклеотидного состава. Гиперхромный эффект – увеличение оптической плотности ДНК при плавлении ДНК. Максимальное повышение оптической плотности раствора ДНК при длине волны 260 нм приблизительно равно 80 %, при полном распаде ее до мононуклеотидов Хроматин состоит из многих витков ДНК, присоединенных к гистонам – белкам основной природы. В период между делениями (интерфаза), хромосомы практически неразличимы в световом микроскопе как обособленные структуры, хотя материал, из которого они состоят, окрашивается некоторыми основными красителями и потому назван хроматином. На этой стадии хромосомы представляют клубок длинных тонких нитей.
14. Нуклеосомы. Гистоны. Нуклеосомы – ДНК и гистоны объедины в структуру, по виду напоминающие бусины. ДНК (около 160 п.н.) делает два ветка вокруг нуклеосомы (кора). Нуклеосома содержит по две молекулы каждого из гистонов Н2А, Н2В, Н3 и Н4, т.е. состоит из восьми молекул. Размер ДНК между нуклеосомами (линкерная ДНК) составляет около 60 п.н.Гистоны – белки основной природы, заряжены положительно.
Природные РНК можно разделить на 2 группы: одноцепочечные и двухцепочечные РНК. Двухцепочечные РНК состоят из двух нитей РНК, комплементарных друг другу. По своей организации двухцепочные РНК сходны с ДНК: 1. они закручены в двойную правую спираль 2. цепи РНК в них антипаралельны 3. между комплементарными основаниями образованы водородные связи 4. углеводнофосфатный скелет расположен снаружи спирали
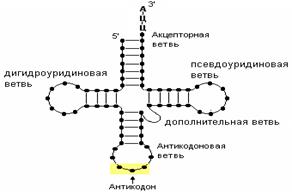
1. иРНК (или матричные РНК) - несет информацию о первичной структуре белка служат матрицами для биосинтеза полипептидных цепей. Они содержат линейную последовательность кодонов, которые и определяют первичную структура белка. иРНК –одноцепочечные молекулы. Одна молекула иРНК может кодировать одну или несколько полипептидных цепей. Если иРНК несет информацию об одной полипептидной цепи, то ее называют моноцистронной (эукариот), если о двух или более – полицистронной (прокариот). 2. рРНК - входит всостав рибосом. Рибосомы представляют собой - крупный рибонуклеопротеидный комплекс с молекулярной массой около 2,5 мДа, состоящий из белков и молекул рРНК. У эукариот они представлены 80S частицами, у прокариот – 70S. Рибосомы всех известных организмов построены из большой и малой субчастиц: прокариотические – 30S и 50S, а эукариотические – 40S и 60S. рРНК играют важную роль в структуре и биосинтетической функции рибосом. 3. тРНК - обеспечивает расшифровку ген. инф., записанной в иРНК и доставку АК к месту синтеза белка. На 3’-конце всех тРНК находится тринуклеотидная последовательность Ц-Ц-А. Более половины оснований тРНК образуют внутрицепочечные пары по принципу комплементарности. Т.о., формируется вторичная структура- клеверный листок.
В ней выделяют:1)дигидроуридиловую ветвь;2)псевдоуридиловую ветвь, содержащую минорные азотистые основапния псевдоуридина;3)антикодоновую ветвь, в центре которой находится антикодон (комплементарен кодону);4)дополнительную ветвь;5)акцепторную ветвь с универсальной 3'-концевой последовательностью ЦЦА, служащей акцептором остатка аминокислоты.
|