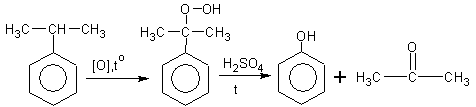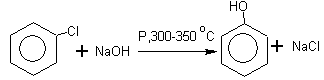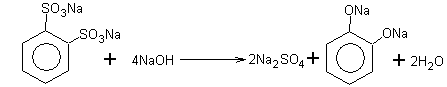Фенолы.На предметне скло нанести 2 краплі насиченого розчину біосульфату натрію, додати 1 краплю ацетону, розмішати скляною палочкою. Через 3-5 хв предметне скло перенести під мікроскоп. Що видно? Якої форми кристали біосульфітного похідного ацетону? Написати схему реакції. Самоокислення водних розчинів формальдегіду. В пробірку додати 3 краплі розчину формаліну та додати 1 краплю індикатора метилового червоного. Що спостерігається? Обгрунтувати відповідь винекнення кислого середовища у водних розчинах формальдегіду.
Вправи для самостійної роботи: 1.Напишіть структурні формули альдегідів, молекули яких містять від одного до шести вуглецевих атомів. 2.Написати структурні формули всіх ізомерів альдегідів і кетонів складу С5Н10О, назвати їх за ІЮПАК номенклатури. 3.Напишіть схему окислення бутаналю. 4.200 мл ацетилену (н,у.) пропустили при нагріванні через воду, яка містила невелику кількість сульфату ртуті. Яка речовина і в якій кількості утворилася при цьому? 5.Яким чином можна виявити ацетон у воді? Напишіть схему реакції. 6.Про що свідчить наявність ацетону у сечі людини? Як його виявити в сечі? 7.Здійсніть перетворення: 8.Напишіть схему окислення метилпропілкетону. 9.Окисленням вторинного спирту добувають ацетон. Обчислити, скільки спирту потрібно для добування 1 кг 5%-го водного розчину ацетону? Домашнє завдання: 1. Вивчити контрольні питання теми. 2. Підготуватися до теми: “Односновні карбонові кислоти” Література: 1.Тюкавкина Н.А. Органическая химия.– М.:Медицина, 1989. С.135-152. 2.Боєчко Ф.Ф., Найдан В.М., Захарик Д.М. і ін. Органічна хімія.-1986., С142. 3.Конспект лекцій з теми: “Альдегіди та кетони”.
План лекции. 1. Классификация, номенклатура, способы получения и химические свойства одноатомных фенолов в сопоставлении со спиртами. 2. Кислотные свойства. Реакции нуклеофильного замещения (взаимодействие с галогенопроизводными). Качественные реакции на фенолы. Фенолы. Фенолы – органические соединения, содержащие в молекулах гидроксильную группу, связанную непосредственно с бензольным кольцом.
Номенклатура и изомерия . 1. Тривиальная (фенол, резорцин, гидрохинон, пирокатехин) 2. Систематическая (гидроксибензол, 1,3-дигидроксибензол, 1,4-дигидроксибензол, 1,2-дигидроксибензол) Примеры:
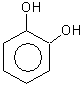
гидроксибензол(фенол) 1,2-дигидроксибензол 1,3-дигидроксибензол (бензендиол-1,2) (бензендиол-1,3) (пирокатехин) резорцин
(бензендиол-1,4) гидрохинон. Изомерия в многоатомных фенолах обусловлена положением ОН-групп.
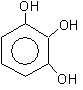
1,2,3-тригидроксибензол 1,2,4-тригидроксибзл 1,3,5-тригидроксибзл (бензентриол-1,2,3) (бензентриол-1,2,4) (бензентриол-1,3,5) пирогаллол оксигидрохинон флороглюцин
Способы получения . 1.Фенол получают из каменноугольной смолы. 2.Синтетический путь получения фенола - кумольный метод из изопропилбензола:
(кумол) гидроперекись фенол ацетон изопропилбензол кумола 3.Гидролиз хлорбензола (SN):
Условия протекания реакции: а) давление, температура 300-350оС, автоклав; б) катализатор - соль Сu +8% p-p NaOH 4. Получение двухатомных и трехатомных спиртов синтетическим путём сложнее, чем одноатомных. В природе источником их является сланец. Резорцин получают окислением м-диизопропилбензола, пирокатехин – окислением о-диизопропилбензола, гидрохинон – окислением п-диизопропилбензола:
Бензолдисульфокислоты дифенолят динатриевая соль После кислотной обработки дифенолят легко превращается в пирокатехин. Физические свойства . Фенол – кристаллическое бесцветное вещество, трудно растворимое в Н2О. С увеличением количества ОН-групп растворимость фенолов в Н2О увеличивается. Ядовит, Является антисептиком, при попадании на кожу вызывает ожоги. Имеет tплав = 43оС. С Н2О образует гидрат, называемый карболовой кислотой. Пирокатехин ( 1,2-бензендиол) имеет tплав = 104оС. При хранении темнеет. С FeCl3 дает зелёное окрашивание, которое переходит в красное при добавлении NaHCO3. Резорцин (1,3-бензендиол) имеет tплав = 118оС.С FeCl3 дает фиолетовое окрашивание.
|

 В зависимости от числа ОН-груп в бензольном кольце бывают: одно-, двух и трёхатомные.
В зависимости от числа ОН-груп в бензольном кольце бывают: одно-, двух и трёхатомные.
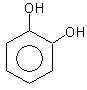

 1,4-дигидрокибензол
1,4-дигидрокибензол