| Название этапа
| Описание деятельности
| Цель деятельности
| время
|
| 1. Теоретические аспекты теории строения и свойств вещества.
| Задание № 1.
1.Характеристика кристаллических веществ?
2.Типы кристаллических решёток?
3. Что такое смесь?
4. Что такое изотопы?
5.Осадок: аморфный, кристаллический. Характеристика?
6.Что такое химическая связь? Виды? Характеристика?
7.Органические и неорганические вещества. Характеристика? Пример?
| формирование новых знаний
| 30мин
|
| 2. Классификация химических связей..
| Задание № 2
Даны вещества NH3(Аммиак); Cl2. 1) по формуле определите вид химической связи. Приведите аргументы. 2)опишите последовательно особенности строения и свойств атомов, химической связи, кристаллической решетки для каждого из веществ.3)опишите физические свойства веществ, основываясь на их строении.
| формирование умения решать задачи и отвечать на вопросы
|
мин
|
| 3. Задания на знание химических элементов
| В настоящее время известно 13 кристаллических модификаций простых веществ обладающих полупроводниковыми свойствами. Назовите данные химические элементы: 3-я группа – В; 6-я группа – S, Se, Te; 4-я группа – S, Si, Ge, Sn; 7-я группа – I. 5-я группа – P, As, Sb, Bi;
Дайте им характеристику?
| формирование умения находить отличия
|
мин
|
| 4. Структура кристаллов и типы химических связей
| Задание № 4
1) Какие связи имеются в кристаллах, образованных элементами с порядковым номером 40, 2, 82? Какие свойства характерны для этих кристаллов? 2) Чем отличается структура кристаллов As и Zn от структуры кристалла Zn3As2? Какие свойства характерны для этих веществ в кристаллическом состоянии? 3) Охарактеризовать полупроводниковые свойства кристалла Вт. Как изменятся эти свойства, если кристалл содержит примеси: Zn; Sb.
| закрепление знаний, полученных на теоретических занятиях
| 35 мин
|
| 5.Подведение итогов работы
| Сделать вывод о проделанной работе, отметить, что удалось и вызвало трудности. Записать вывод в дневник.
| рефлексия
|
мин
|
| 6. Контроль выполнения работы
| Сдать дневник преподавателю, отчитаться о проделанной работе
| контроль полученных знаний
| 5 мин
|
| 7.Уборка рабочего места
| Убрать рабочее место, сдать раздаточный материал по проведению работы преподавателю.
| организованное завершение работы
| 1мин
|
Методическая разработка для студентов
к практическому занятию № 4
по дисциплине «Неорганическая химия»
тема: «Классы неорганических соединений»
Цели занятия:
Студент должен знать:
- теоретические основы неорганической химии
- методы качественного и количественного анализа
- качественные реакции, применяемые в фармацевтическом анализе
Студент должен уметь:
-периодического закона и характеристики элементов периодической системы Д.И. Менделеева;
- основы теории протекания химических процессов
-строения и реакционных способностей неорганических соединений
-способов получения неорганических соединений
-теории растворов и способов выражения концентрации растворов
Знания формул лекарственных средств неорганической природы
Оснащение: методические указания по выполнению работы с приложениями
Ориентировочная карта № 1 (задание на самоподготовку)
| № п/п
| Учебные элементы
| Истоки
| Цель деятельности
| Вопросы самоконтроля
|
|
| Теоретические аспекты классификации соединений.
| конспект лекции
| Знать основные характеристики
| 1.Что такое химическое соединение?
2.Что такое металлы?
3. Неметаллы. Характеристика?
4. Соли. Характеристика?
5.Оксиды. Характеристика?
6.Осннования. Характеристика?
|
|
| Классификация химических соединений.
| конспект лекции
| Знать основные характеристики химических соединений
| Начертите схему классификация неорганических соединений.
|
|
| Задания на знание кислот и солей
| конспект лекции
|
| Название кислоты Формула Пример соли Название соли
Серная H2SO4
K2SO4 сульфат К
сернистая H2SO3
Na2SO3 сульфит Na
соляная HCl
Ca(Cl)2 хлорид Са
иодоводородная HI KI
иодид К
сероводородная H2S
Na2S cульфид
Na
азотная HNO3
KNO3 нитрат К
азотистая HNO2
NaNO2 нитрит Na
ортофосфорная H3РO4 K3РO4 ортофосфат К хлорная НСlO4 NaСlO4 перхлорат Na хлорноватая НClO3 NaСlO3 хлорат Na хлористая НClO2 NaСlO2 хлорит Na хлорноватистая НСlO NaСlO4 гипохлорит Na кремниевая H2SiO3 CaSiO3 силикат Сa Название кислоты Формула Пример соли Название соли алюминиевая H3AlO3 K3AlO3 алюминат К ортоборная H3BO3 K3BO3 ортоборат К мышьяковая HAsO4 KAsO4 арсенат К мышьяковистая HAsO3 KAsO3 арсениты К двуфосфорная H4P2O7 K4P2O7 дифосфат К угольная H2CO3 K2CO3 карбонат К фосфористая H3PO3 K3PO3 фосфит К фтороводород HF KF фторид К хромовая Н2СrO4 K2СrO4 хромат К синильная НCN KCN цианид К
|
|
| Вычисление эквивалента элемента
| конспект лекции
| Знать химический структуру.
| Под эквивалентом элемента понимают такое его количество, которое соединяется с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях. Масса 1 эквивалента элемента называется его эквивалентной массой. Эквивалент водорода ЭН всегда равен 1, а эквивалент кислорода ЭО=8. Эквивалент элемента равен:  , где: М – мольная масса элемента; СО – степень окисления элемента (валентность) в соединении. Эквивалент кислоты равен: , где: М – мольная масса элемента; СО – степень окисления элемента (валентность) в соединении. Эквивалент кислоты равен:  , где: М – мольная масса кислоты; х – основность кислоты. Эквивалент основания равен: , где: М – мольная масса кислоты; х – основность кислоты. Эквивалент основания равен:  , где: М – мольная масса основания; у – кислотность основания.
Эквивалент соли равен: , где: М – мольная масса основания; у – кислотность основания.
Эквивалент соли равен: 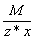 , где: М – мольная масса соли; z – валентность катиона; х – количество атомов катиона в соединении. Вычислите эквивалент кислорода , где: М – мольная масса соли; z – валентность катиона; х – количество атомов катиона в соединении. Вычислите эквивалент кислорода  , едкого натра , едкого натра 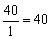 и угольной кислоты и угольной кислоты  . .
|

 , где: М – мольная масса элемента; СО – степень окисления элемента (валентность) в соединении. Эквивалент кислоты равен:
, где: М – мольная масса элемента; СО – степень окисления элемента (валентность) в соединении. Эквивалент кислоты равен:  , где: М – мольная масса кислоты; х – основность кислоты. Эквивалент основания равен:
, где: М – мольная масса кислоты; х – основность кислоты. Эквивалент основания равен:  , где: М – мольная масса основания; у – кислотность основания.
Эквивалент соли равен:
, где: М – мольная масса основания; у – кислотность основания.
Эквивалент соли равен: 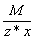 , где: М – мольная масса соли; z – валентность катиона; х – количество атомов катиона в соединении. Вычислите эквивалент кислорода
, где: М – мольная масса соли; z – валентность катиона; х – количество атомов катиона в соединении. Вычислите эквивалент кислорода  , едкого натра
, едкого натра 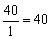 и угольной кислоты
и угольной кислоты  .
.



