Контрольная работа. по предмету «Материаловедение» МИНИСТЕРСТВО ТРАНСПОРТА РОССИЙСКОЙ ФЕДИРАЦИИ
Федеральное агентство воздушного транспорта
Рыльский авиационный технический колледж – филиал
федерального государственного бюджетного образовательного
учреждения высшего профессионального образования
«МОСКОВСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ
УНИВЕРСИТЕТ ГРАЖДАНСКОЙ АВИАЦИИ»
по предмету «Материаловедение»
студента заочного отделения
Колодий Евгения Евгеньевича
Вариант 11 1)Каковы основные виды химической связи в материалах и чем они характеризуются? При сближении атомов до расстояния нескольких долей нанометра (1нм=10-9 м), между ними появляются силы взаимодействия. Если эти силы являются силами притяжения, то атомы могут соединяться с выделением энергии, образуя устойчивые химические соединения. При этом электроны внутренних и внешних оболочек атомов ведут себя по-разному. Электроны внутренних, полностью заполненных оболочек прочно связаны с ядром и не участвуют в образовании химических связей. Строение внешней, не полностью заполненной электронами оболочки определяет химические свойства атомов в образовавшемся соединении. Электроны, находящиеся на внешних оболочках, являются валентными. Валентность атома определяется числом этих электронов. Все многообразие существующих в природе материалов характеризуется несколькими видами химической связи. Ковалентная (гомеополярная) связь. При наличии такой связи объединение атомов в молекулу достигается за счет электронов, которые становятся общими для пар атомов (рис. 1.1). Плотность отрицательно заряженного электронного облака между положительно заряженными ионами получается наибольшей. Появление состояния с повышенной плотностью электронного заряда в межионном пространстве приводит к возникновению сил притяжения между атомами.
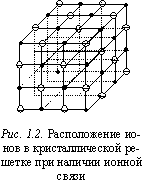
Ковалентная связь характерна как для органических так и для неорганических соединений. К неорганическим веществам с ковалентной связью относятся алмаз, кремний, германий, арсенид галлия (GaAs), карбид кремния (SiC) и другие, являющиеся полупроводниками. Многие полупроводники кристаллизуются в структуре алмаза, в которой каждый атом образует четыре связи со своими ближайшими соседями. Ковалентная связь в неорганических материалах характеризуется высокой прочностью. Подтверждением этому является высокие твердость и температура плавления алмаза, кремния и др. Ионная (гетерополярная) связь. Наблюдается в химических соединениях атомов металла с металлоидными атомами (типа NaCl). Ионная связь возникает вследствие перехода валентных электронов от металлического атома к металлоидному и, как результат, возникновению электростатического притяжения разноименно заряженных атомов друг к другу. На рис. 1.2 схематически представлена трехмерная решетка гипотетического ионного кристалла, где атомы металла изображены в виде точек (положительно заряженные ионы - катионы), а атомы металлоида - в виде кружочков (отрицательные ионы - анионы). В решетке ионного кристалла чередуются ионы различного сорта. Способность атома захватывать электрон при образовании ионной химической связи называется электроотрицательностью. Чем больше разность электроотрицательностей атомов, участвующих в образовании химической связи, тем больше степень ионности соединения
Металлическая связь. Существует в системах, построенных из положительных атомных остовов, находящихся в среде свободных коллективизированных электронов (рис. 1.3). Притяжение между положительными ионами и электронами обуславливает существование металлов как химических соединений. Металлическую связь можно рассматривать до некоторой степени как ковалентную связь, поскольку в ее основе лежит обобществление внешних валентных электронов. Специфика металлической связи состоит в том, что обобществленные электроны свободно перемещаются внутри всей решетки, образуя "электронный газ". Поэтому металлическим материалам свойственны пластичность, высокая электро- и теплопроводность. Молекулярная связь (связь Ван-дер-Ваальса). Этот вид химической связи наблюдается у ряда веществ (парафин, жидкие кристаллы) между молекулами с ковалентным характером внутримолекулярного взаимодействия. Вещества с молекулярной связью характеризуются сравнительно низкой температурой плавления и невысокой механической прочностью.
|