Материальный балансПроизводство водорода Расчет материального и теплового балансов трубчатой печи для конверсии природного газа.
Составить материальный и тепловой балансы трубчатой печи для конверсии природного газа. Состав природного газа (в объемных %): w (СН4)=97,8; w (С3Н8)=0,2; w (N2)=1,4. w (С2Н6)=0,5; w (С4Н10)=0,1; Отношение объемов пар: газ в исходной смеси η=2,5. Степень конверсии газа по углероду хг=0,67. Гомологи метана разлагаются нацело. Соотношение между СО и СО2 в конвертированном газе соответствует равновесию реакции при 700°С. СО + Н2О ó CО2 + Н2, ΔН=-40,9 кДж/моль (а) Температура: - паро-газовой смеси на входе в печь t0=380°C; на выходе из печи tк=700°C; - дымовых газов на выходе tдым=800°С; - природного газа (для обогрева печи) tп=18°С Теплопотери в окружающую среду – 4% от прихода тепла; Давление в конверторе р=1·105 Па (1 атм).
Расчет вести на 100 м3 природного газа (при н.у.) (Vг=100 м3). Материальный баланс При конверсии метана и его гомологов протекают следующие эндотермические реакции: СН4 + Н2О = СО + 3Н2 (б) С2Н6 + 2Н2О = 2СО + 5Н2 (в) С3Н8 + 3Н2О = 3СО + 7Н2 (г) С4Н10 + 4Н2О = 4СО + 9Н2 (д) Образующаяся окись углерода СО конвертируется водяным паром по экзотермической реакции (а).
Обозначим содержание, в м3: · компонентов в конвертированном газе СО2 – а; СО – b; Н2 – с; · водяного пара, вступившего в реакцию с углеводородами и СО через d.
Объем углеводородов в пересчете на СН4 в конечном газе Vк(СН4):
Vк(СН4) = (V(СН4) + V(С2Н6)·2 + V(С3Н8)·3 + V(С4Н10)·4)·(1-хг)= = (97,8 + 0,5·2 + 0,2·3 + 0,1·4)·(1-0.67)=32,9 м3,
где: 2, 3, 4 – количество атомов углерода в молекулах С2Н6, С3Н8 и С4Н10 соответственно.
Составим балансовое уравнение по содержанию каждого элемента в исходном и конвертированном газах, в м3: · по углероду V(СН4) + V(С2Н6)·2 + V(С3Н8)·3 + V(С4Н10)·4 = = Vк(СО2) + Vк(СО) + Vк(СН4); 97,8 + 0,5·2 + 0,2·3 + 0,1·4 = a + b + 32,9; а = 66,9 – b; (1) · по кислороду: в исходной паро-газовой смеси содержится V(Н2О) = Vг·η = 100·2,5=250 (м3) V(Н2О)·0,5 = Vк(СО2) + Vк(СО)·0,5 + Vк(Н2О)·0,5; 250·0,5 = a + 0,5b + 0,5(250-d) a + 0,5b – 0,5d = 0; (2) · по водороду: V(СН4)·2 + V(С2Н6)·3 + V(С3Н8)·4 + V(С4Н10)·5 + V(Н2О) = = V(Н2) + Vк(СН4)·2 + Vк(Н2О); 97,8·2 + 0,5·3 + 0,2·4 + 0,1·5 + 250 = с + 32,9·2 + (250-d) с = d + 132,6 (3)
Соотношение между СО и СО2 в конечном газе по условию определяется равновесием реакции конверсии СО (а). Для определения значения константы равновесия воспользуемся следующим уравнением:
Константа равновесия при температуре 700°C равна 1,54 (табл.): К= Подставляя значение а из уравнения (1) в уравнение (2), получаем: b = 133,8 – d (5) Подставляя в уравнение (1) значение b из (5), находим: a = d – 66,9 (6) Подставляя в уравнение (4) значения a, b, c, выражения через d получаем:
Откуда находим d=100м3, а = 100 – 66,9 = 33,1 м3; b = 133,8 – 100 = 33,8 м3; с = 100 + 132,6 = 232,6 м3. Объем водяного пара, вступившего в реакцию: · с СО V1 = Vк(СО2) = a = 33,1 м3 (в соответствии с уравнением1) · с углеводородами V2 = d – V1 = 100 – 33,1 = 66,9 м3. Осталось в газе водяного пара Vк(Н2О)=V(Н2О)–d=250-100= = 150 м3. Занесем состав влажного и сухого газа в таблицу 1. Таблица 1 Состав конвертированного газа
Для составления материального баланса выразим состав газа до и после конверсии в кг по общей формуле:
где: У – компонент газа; V(У) – его объем, м3; М(У) – молярная масса У, кг/кмоль; 22,4 – молярный объем газа при н.у., дм3/моль. Результаты расчета материального баланса представим в табл.2 Таблица 2
Материальный баланс трубчатой печи.
|

 (4)
(4) (7)
(7)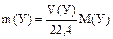 ,
,


