ЭЛЕМЕНТЫ У1 ГРУППЫ ПОБОЧНОЙ ПОДГРУППЫВ подгруппу входят хром, молибден, вольфрам и рений.
 Характерная степень окисления +6, наряду с этим хром дает устойчивые соединения со степенью окисления +3, молибден +4. В других степенях окисления (+2, +4, +5) хром и его аналоги образуют неустойчивые соединения и имеют несколько степеней окисления. На свойства вольфрама оказывает влияние лантаноидное сжатие. Радиусы вольфрама и молибдена близки, по свойствам они менее отличаются друг от друга, чем от хрома. От хрома к вольфраму химическая активность элементов уменьшается. Характерная степень окисления +6, наряду с этим хром дает устойчивые соединения со степенью окисления +3, молибден +4. В других степенях окисления (+2, +4, +5) хром и его аналоги образуют неустойчивые соединения и имеют несколько степеней окисления. На свойства вольфрама оказывает влияние лантаноидное сжатие. Радиусы вольфрама и молибдена близки, по свойствам они менее отличаются друг от друга, чем от хрома. От хрома к вольфраму химическая активность элементов уменьшается.
Природные ресурсы. В земной коре содержится: Cr -3,5 · 10-2 %, Mo – 1,1 · 10-4 % и W – 10-4 %. Основные минералы: Fe(CrO2)2 – хромистый железняк, PdCrO4 - крокоит, MoS2 - молибденит, CaWO4 – шеелит, WO3 – вольфрамовая охра, (Fe, Mn) WO4 – вольфрамит. Получение. Хром, молибден и вольфрам получают из природных соединений в виде металлов и в виде ферросплавов, которые непосредственно используются для легирования сталей. Феррохром: Fe(CrO2)2 + 4C = Feº +2Crº + 4CO; tº Cr2O3 + 2Al = Al2O3 + 2Cr; tº 2Cr2O3 + 3 Si + CaO = 4Cr + 3CaSiO3.
Физические свойства. В свободном состоянии элементы подгруппы хрома – серебристо – белые блестящие парамагнитные металлы с очень высокой температурой плавления, которая растет от хрома к вольфраму, W – самый тугоплавкий из всех известных металлов. Плотность металлов увеличиваетсяот хрома к вольфраму,в этом же ряду снижается способность металлов переходить в пассивное состояние за счет образования на поверхности металла оксидной пленки. Химические свойства. В ряду напряжений хром, молибден и вольфрам расположены до водорода, однако в обычных условиях они малоактивны. Хром взаимодействует с разбавленными НС1О4 и H2SO4, молибден к ним устойчив. Концентрированные H2SO4 и HNO3 и царская водка на холоде пассивируют хром; горячие окисляют хром до солей хрома (111), а молибден до молибденовой кислоты. Вольфрам устойчив ко всем кислотам за исключением царской водки и смеси HNO3 + НF, например: Cr + H2SO4 + 6H2O = [Cr(H2O)6] SO4 + H2↑ 2Cr + 6 H2SO4 (конц.) = Cr2(SO4)3 + 3SO2 +6H2O Mo + 2HNO3 + 2 H2O = H2MO4 +2NO W + 2НNO3 + 8 HF = H2[WF8] + 2 NO + 4 H2O Хром, молибден и вольфрам могут быть переведены в раствор методом окислительного щелочного сплавления с образованием, соответственно, хроматов, молибдатов и вольфраматов, например:
1 Э +_ 8ОН - - 6 е = _ ЭO42- + 4 H2O 3 NО3 + H2O +2е = NО2 + 2ОН - Э + 8ОН - + 3NО3 + 3 H2O = ЭO42- + 4 H2O + 3NО2 + 6ОН - Растворы щелочей на данные металлы практически не действуют. Соединения хрома в степени окисления +2. Для хрома известно лишь небольшое число бинарных соединений в степени окисления +2, которые получают восстановлением соединений Cr3+. Оксид хрома (11) получить очень трудно. Бинарные соединения хрома проявляют основные свойства. Соединения хрома в степени окисления +2 обладают большой востановительной способностью. В при отсутствии окислителя восстанавливают воду, постепенно разлагая ее с выделением водорода: 2CrCI2+2H2О= 2Cr ОНCI2+ H2.
Соединения хрома в степени окисления +3. Для хрома степень окисления +3 является наиболее устойчивой. Координационное число хрома (111) равно шести, его комплексы имеют структуру октаэдра. Оксид хрома (III) –химически устойчивый, нерастворимый в воде и кислотах зеленый порошок. Он тугоплавок, твердоссть его кристаллов соизмерима с твердостью корунда. Оксид хрома (111) можно получить по следующим реакциям:
Амфотерная природа Сr2О3 проявляется при сплавлении со щелочами и пи-росульфатом калия: tº
Оксиду Cr2O3 соответствует гидроксид хрома (111) [Cr(OH)3] n – это много-ядерный слоистый полимер серо-зеленого цвета, в котором роль лигандов играют ионы гидроксила и молекулы воды, а роль мостиков - группы ОН-. Его состав и структура зависят от условий получения. При старении и особенно при нагревании, гидроксид хрома. Свежеосажденный гидроксид хрома хорошо растворяется в кислотах и щелочах, которые вызывают разрыв связей в слоистом полимере: Cr(OH)3 + 3HCl + 3 H2O = [Cr(H2O)6]Cl3 Cr(OH)3 + 3NaOH = Na3[Cr(OH)6]
Для солей хрома характерна гидратная изомерия, в зависимости от числа моль воды во внутренней сфере они окрашены в разные цвета, например, [Cr(H2O)5Cl]Cl2-светло-зеленый [Cr(H2O)4Cl2]Cl·2H2O – темно – зеленый, Соли хрома легко подвергаются гидролизу:
2 CrCl3 + 3Na2СO3 +3H2O = 2Cr (OH)3 + 3CO2 + 6NaCl Хром (III) весьма склонен к образованию комплексов как анионного, так и катионного типа, координационное число равно шести, что соответствует d2sp3 – гибридизации.
2 Cr 3+ + 8 ОН- -3е = CrO4 2- + 4Н2О 3 Н2О2 –2е = 2ОН- 2Cr 3+ + 16ОН- + 3Н2О2 = 2CrO4 2- + 8Н2О – 6ОН- 2 Na [Cr(OH)6] 3- +6Br2 +4NaОН = Na2CrO4 +6NaBr +8Н2О 2 [Cr(OH)6] 3- +2ОН- -3е = CrO4 2- + 4Н2О 3 Br2 +2e = 2Br - 2 [Cr(OH)6] 3- +4ОН- + 3Br2= 2CrO4 2- + 8Н2О + 6Br- -
Соединения хрома степени окисления +6. Соединения хрома в степени окисления +6 многочисленны. Соединения с низкими степенями окисления длямолибдена и вольфрама неустойчивы и мало изучены. Оксид CrO3 получают по реакции: K2Cr2O7 (тверд.) + H2SO4 (КОНЦ) = K2 SO4 + 2 СrО3 + H2O. CrO3 – оксид темно-красного цвета, имеет цепочечную структуру, образованную тетраэдрами CrO4. При нагревании CrO3 довольно легко разлагается с выделением кислорода:
Со многими окисляющимися веществами CrO3 взаимодействует со взрывом.
|


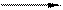 Э+ 3NаNО3 + 2NаОН СПЛАВ Na2ЭO4 + 3 NaNO2 + Н2О
Э+ 3NаNО3 + 2NаОН СПЛАВ Na2ЭO4 + 3 NaNO2 + Н2О K2S2O3 K2SO4 + SO3
K2S2O3 K2SO4 + SO3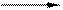 Cr2O3 + 3SO3 tº Cr2 (SO4)3
Cr2O3 + 3SO3 tº Cr2 (SO4)3 [Cr(H2O)6]Cl3 –фиолетовый,
[Cr(H2O)6]Cl3 –фиолетовый,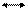

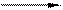 4CrO3 2Cr2O3 + 3O2↑,
4CrO3 2Cr2O3 + 3O2↑,


