Порядок выполнения работы. Изучение скорости разложения пероксида водорода газометрическим методом: гомогенный иМИНИСТЕРСТВО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ ЮГОРСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ИНСТИТУТ ГЕОЛОГИИ НЕФТИ И ГАЗА КАФЕДРА ХИМИИ
Лабораторная работа
Изучение скорости разложения пероксида водорода газометрическим методом: гомогенный и Гетерогенный катализ
Лабораторные работы по физической химии для студентов института геологии нефти и газа обучающихся по специальности 020100 «Химия» Курс III, семестр 6 Ханты-Мансийск·2009 Лабораторная работа №5 Изучение скорости разложения пероксида водорода газометрическим методом: гомогенный и гетерогенный катализ Цель работы: определить несколькими методами порядок реакции, аналитически и графически определить среднюю константу скорости при различных концентрациях катализатора.
Общие положения Пероксид водорода в водных растворах самопроизвольно медленно разлагается по уравнению: 2Н2О2 ® 2H2O + O2. В присутствии катионов и анионов некоторых органических веществ, а также ряда твердых веществ разложение перексида водорода (H2O2) значительно ускоряется. Следовательно, эта реакция в водных растворах может быть гомогенной и гетерогенной каталитической реакцией в зависимости от взятого катализатора. Механизм реакции включает следующие стадии:
Катализ разложения H2O2 хлоридом железа (III) происходит по общей схеме: А + К—[АК] (первая стадия), [АК] — В + К (вторая стадия), где А – перексид водорода, К – катализатор. Равновесие устанавливается быстро, и скоростьопределяющей стадией является распад [AK]. Аналитический способ определения порядка реакции Порядок реакции по концентрации H2O2– первый (или близкий к первому) и для расчета константы скорости используют уравнение:
Подставляя в это уравнение опытные значения концентрации исследуемого вещества в разные моменты времени протекания реакции, вычисляем k. Если расчетные k остаются постоянными, то это означает, что порядок реакции по этому веществу равен единице. Начальная и текущая концентрации H2O2 пропорциональны объемам кислорода, выделившегося к концу реакции V ¥ и разности между V ¥ и текущим объемом кислорода Vt. В соответствии с этим, уравнение для расчета константы скорости в данном случае примет следующий вид:
Графический способ определения порядка реакции
Как видно из этих уравнений, график, построенный по опытным данным для концентраций рассматриваемого исходного вещества в разные моменты времени протекания реакции, будет выражаться прямой линией в разных координатах в зависимости от порядка данной реакции по веществу. А именно, при n = 1 – в координатах ln с – t; при n = 2 – в координатах К реакциям первого порядка относятся реакции, в которых концентрация одного из реагирующих веществ остается постоянной. Для реакции типа
Разделив переменные,
Если t = 0, то с = с о. Тогда const = ln с o и можно записать:
где с о= V ∞, с =(V ∞– V t). Следовательно
то есть график в координатах ln с – t будет линейным; по углу наклона этого графика можно оценить k. Для проверки порядка реакции графическим способом (только для гомогенного катализа) строят график ln(w ¢)= f [ln(V¥ – Vt)]. На этом графике должна получиться прямая линия, угловой коэффициент которой в соответствии с уравнением lg w =lg k + n lg c должен быть равен порядку реакции, поскольку коэффициент пропорциональности между w ¢ и w тот же, что и между (V¥ – Vt) и c (Н2О2). Свободный член полученной зависимости равен ln k только в том случае, если получился порядок равный единице, в ином случае значение свободного члена зависит от порядка реакции и коэффициента пропорциональности между (V¥ – Vt) и c (Н2О2).

Рис. 1. График зависимости логарифма концентрации от времени Для нахождения значений w’ необходимо построить график (V¥ – Vt) = f (t), т.е. кинетическую кривую, причем следует иметь в виду, что по оси ординат отложена не концентрация, а пропорциональная ей величина. Не менее чем для трех произвольно выбранных значений времени на этом графике найти значения производной
проведя касательные к выбранным точкам и определив их тангенс наклона. Полученные таким образом значения производной w ¢ не равны, но пропорциональны значениям скорости w в выбранные моменты времени. Касательные на кинетической кривой проводятся не к экспериментально определенным точкам (производная к точке и, соответственно, касательная к точке – бессмысленные понятия), а к сглаженной линии, наилучшим образом проходящей через экспериментальные точки.
Реактивы и оборудование: 3%-ный раствор хлорида железа (III); 3%-ный раствор пероксида водорода; оксид алюминия (III); оксид марганца (IV); 3%-ный раствор иодида калия; водяная баня – 1 шт.; термометр до 100°С – 1 шт.; установка для газометрических измерений – 1 шт.; градуированная пипетка на 10 мл – 2 шт.; секундомер – 1 шт.
Порядок выполнения работы Для изучения скорости разложения пероксида водорода используют установку, показанную на рисунке 2, которая позволяет измерять объем выделяющегося кислорода. В одно колено реактора 1 с помощью пипетки помещают 10 мл 3%-ного раствора пероксида водорода, а во второе – 0,5 мл раствора хлорида железа (III) и с помощью пробки соединяют реакционный сосуд с мерной бюреткой. Перед началом эксперимента проверяют герметичность системы. Для этого с помощью трехходового крана 3 соединяют измерительный сосуд 4 одновременно с реакционным сосудом 1 и с атмосферой. Поднимают уравнительный сосуд 5, чтобы заполнить бюретку жидкостью до нулевой отметки, после чего соединяют бюретку 4 только с реакционным сосудом 1 и опускают сосуд 5 примерно на четверть высоты бюретки. Если обеспечена герметичность, то уровень затворной жидкости в бюретке 4, опустившись на небольшую величину, должен остановиться, не достигнув уровня жидкости в уравнительном сосуде и должен оставаться неизменным в течение 2-3 минут. После этого при поднимании уравнительного сосуда до уровня жидкости в бюретке, последний должен вновь вернуться к нулевой отметке.
Рис. 2. Схема установки для изучения скорости разложения пероксида водорода: 1 – реакционный сосуд; 2 – пробка, соединяющая реакционный сосуд с мерной бюреткой;
После проверки герметичности приступают к выполнению эксперимента. Для этого пероксид водорода переливают в колено с катализатором, реакционный сосуд 1 встряхивают несколько раз для более полного перемешивания. Время смешения принимают за время начала реакции. Кислород, выделяющийся в ходе реакции, будет вытеснять жидкость из мерной бюретки. Фиксируют объем выделившегося кислорода в зависимости от времени протекания реакции. Измерения проводят через 1, 2, 4, 6, 10, 15, 20 … минут от начала реакции. При измерениях уровень жидкости в уравнительном сосуде 5 поддерживают на уровне жидкости в мерной бюретке 4. Измерения заканчивают, если в течение 10 мин объем кислорода не увеличивается. Если в ходе реакции возникает риск, что объем мерной бюретки окажется недостаточным, следует произвести последний замер объема и по возможности быстро с помощью крана 3 соединяют бюретку 4 с атмосферой. С помощью сосуда 5 устанавливают уровень жидкости в бюретке на нулевой отметке и вновь краном 3 соединяют реакционный сосуд 1 только с бюреткой 4. Продолжают измерения, прибавляя объем кислорода, выпущенного в атмосферу (значение последнего измерения перед соединением бюретки с атмосферой). По окончанию процесса выделения пузырьков кислорода приступают к определению V¥. Для этого реакционный сосуд 1 помещают в водяную баню с температурой воды 70-80°С и выдерживают его при этой температуре до тех пор, пока объем выделившегося кислорода не будет оставаться постоянным в течение 5-10 минут. В этот момент можно считать, что реакция полностью завершилась, однако измерение значения V¥ следует производить только после извлечения реакционного сосуда водяной бани и приведения его к прежней температуре. Опыты повторяют, увеличивая объем раствора катализатора до 1,0 и 1,5 мл. Результаты опытов и расчетов оформляют в виде таблиц, предваряя их следующими данными. Температура опыта…………………………………………°С Объем пероксида водорода..………………………………мл Концентрация пероксида водорода..………………………% Объем раствора катализатора……………………………..мл Концентрация катализатора………………………………..% Объем кислорода по окончанию реакции V¥………….…мл Таблица 1 Выделение кислорода во времени и определение константы скорости разложения пероксида водорода
Аналогичный опыт проделывают с твердым катализатором, в качестве которого используют 0,5 г оксида алюминия (III) или оксида марганца (IV) (по указанию преподавателя).
|

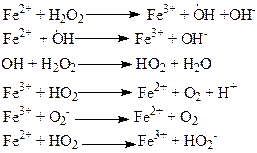

 .
.
 при n = 1,
при n = 1,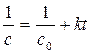 при n = 2,
при n = 2,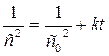 при n = 3.
при n = 3.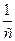 – t; при n = 3 – в координатах
– t; при n = 3 – в координатах 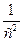 – t. Если, например, график, построенный по опытным данным, оказался прямолинейным на графике в координатах
– t. Если, например, график, построенный по опытным данным, оказался прямолинейным на графике в координатах 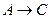 скорость выражается уравнением
скорость выражается уравнением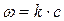 или
или 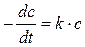 .
.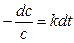 , после интегрирования получим:
, после интегрирования получим: .
.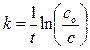 ,
, ,
,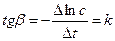
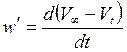 ,
,



