УРОВЕНЬ В. 1. На 2 г смеси, состоящей из Fe, FeO, Fe2O3 подействовали хлороводородной кислотой1. На 2 г смеси, состоящей из Fe, FeO, Fe2O3 подействовали хлороводородной кислотой. При этом выделилось 224 см3 (при н.у.) водорода, а при восстановлении 2 г исходной смеси до металла водородом получено 0, 45 г воды. Определить состав исходной смеси (% масс.).
Cоставляем пропорцию для реакции (12.6):
где
При восстановлении смеси FeO и Fe2O3 водородом протекают реакции FeO + H2 = Fe + H2O (12.7) Fe2O3 + 3H2 = 2Fe + 3H2O (12.8) Составляем пропорцию для уравнения (12.7)
Откуда Составляем пропорцию для уравнения (12.8)
Откуда По условию задачи
Составляем систему уравнений
0, 25 Выражаем из первого уравнения
0, 25·(1, 44 - 0, 09 = 0, 087 Откуда Определяем состав исходной смеси:
Ответ: состав смеси: 28% - Fe, 20, 5% - FeO, 51, 5% - Fe2O3
2. Составить схему получения металлического кадмия из 10 г смеси оксидов CdO и ZnO. В качестве растворителя оксидов использовать разбавленную серную кислоту. Определить состав смеси (% мас.) и массу полученного кадмия, если в качестве восстановителя CdO использовали СО, а объем образовавшегося СО2 составляет 300 см3 (н.у.)
2. Осаждение гидроксидов кадмия и цинка гидроксидом натрия при стехиометрическом соотношении солей и гидроксида натрия: CdSO4 + 2NaOH = Cd(OH)2↓ + Na2SO4 (12.11) ZnSO4 + 2NaOH = Zn(OH)2↓ + Na2SO4 (12.12) 3. Растворение амфотерного гидроксида цинка в избытке щелочи: Zn(OH)2 + 2NaOH = Na2[Zn(OH)4] (12.13) избыток растворимая соль Так как Na2[Zn(OH)4] - растворимая соль, то в осадке остается только гидроксид кадмия. 4. Отделение осадка Cd(OH)2 от раствора фильтрацией, промывка, сушка. 5. Разложение осадка Cd(OH)2 при нагревании: Cd(OH)2 6. Восстановление CdO оксидом углерода (II) при нагревании: CdO + CO М m откуда m где М Определяем содержание СdO в смеси по уравнению (12.16) M m 128, 4г ― 112, 4 г m где M откуда m Определяем ω ω Ответ: состав смеси ZnO - 82, 9%, CdO - 17, 1%, m 3. При растворении 0, 5 г алюминиевой бронзы, состоящей из меди и алюминия, в хлороводородной кислоте выделилось 43, 56 см3 водорода, собранного над водой и измеренного при 300К и 740 мм рт. ст. Давление паров воды при 300К равно 26, 74 мм рт. ст. Определить состав сплава (% мас.)
РЕШЕНИЕ: В соответствии со следствием из ряда стандартных электродных потенциалов металлов в хлороводородной кислоте могут растворяться только те металлы, у которых
Определяем стандартные электродные потенциалы:
Следовательно, в хлороводородной кислоте из сплава будет растворяться только алюминий. Уравнение реакции имеет вид: Alo + HCl = Al+3Cl3 + H
Alo - 3e = Al+3 1 2 ДМ удваиваем, т.к. 3 после реакции образуется H+ + e = H о 3 6 четное число атомов водорода 2Al + 6H+ = 2Al3+ + 6Hо 2Al + 6HCl = 2AlCl3 + 3H2↑ (12.18) Массу алюминия в сплаве можно рассчитываем по уравнению реакции (12.18): 2
Откуда
где Объем водорода при н.у. (
Откуда: = где Подставляя величину
Рассчитываем содержание металлов в сплаве:
Ответ: состав сплава Al – 6%, Cu – 94%.
|



 -? ω
-? ω  -?
ω
-?
ω  -?
-?
 вытесняет 22, 4 л H2 56 г Fe вытесняет 22, 4 л Н2
вытесняет 22, 4 л H2 56 г Fe вытесняет 22, 4 л Н2 - 0, 224 л H2
- 0, 224 л H2  +
+  = 2 – 0, 56 = 1, 44 г
= 2 – 0, 56 = 1, 44 г -
-  72 г/моль - 18 г/моль
72 г/моль - 18 г/моль

 = 0, 25
= 0, 25  -
-  160 г/моль - 3·18 г/моль
160 г/моль - 3·18 г/моль
 = 0, 337
= 0, 337 
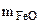
 =
= 
 =
= 
 =
= 
 = 10 г
V
= 10 г
V  = 300 см3
= 300 см3
 -? ω
-? ω  -?
m
-?
m  -?
-?
 СdO + H2O↑ (12.14)
СdO + H2O↑ (12.14) =
=  = 1, 5 г
= 1, 5 г =
=  = 1, 71 г
= 1, 71 г =
=  ·100 = 17, 1%
·100 = 17, 1% = 0, 5 г
HCl - растворитель
V
= 0, 5 г
HCl - растворитель
V 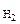 = 43, 56 см3
Т = 300 К
Р = 740 мм рт.ст.
Р
= 43, 56 см3
Т = 300 К
Р = 740 мм рт.ст.
Р  = 26, 74 мм рт.ст.
= 26, 74 мм рт.ст.


 < 0.
< 0. = + 0, 34В,
= + 0, 34В, = -1, 67В
= -1, 67В ↑ (12.17)
↑ (12.17)


 - 3·22400 см3 Н2
- 3·22400 см3 Н2 -
- 
 (12.19)
(12.19)
 =
=







