Получение электрохимическим методом металлического покрытия, как одного из способов защиты металлов от коррозии.Цель работы:Освоить методику электрохимического метода металлических покрытий. Задание по работе:Собрать схему установки для гальванического покрытия, приготовить растворы заданной концентрации, определить выход по току, тип и толщину покрытия и написать уравнения реакции для данного процесса. Методические указания по выполнению работы 1. Сборка установки Собрать установку по схеме, приведенной на рис. В качестве катода – пластина из малоуглеродистой стали; анода – пластина из меди, никеля или цинка в зависимости от типа покрытия. Необходимо взять два анода, чтобы одновременно шло покрытие обоих сторон пластины (катода). 2. Приготовление электролита для гальванической ванны · Электролит омеднения. Состав электролита: 80 г медного купороса, 22 мл 20%раствора серной кислоты. Медный купорос растворить в 400 мл воды и в него добавить раствор серной кислоты. Приготовленный раствор вылить в гальваническую ванну (химический стакан). · Электролит никелирования. Состав электролита: 40г сульфата никеля, 7 г поваренной соли и 7 г борной кислоты растворить в 400 мл воды. Приготовленный раствор вылить в гальваническую ванну (химический стакан). В раствор никелирования вводят поваренную соль, чтобы не происходила пассивация анода, так как в этом случае поступление ионов никеля в раствор замедлится, или совсем прекратится; борную кислоту вводят для поддержания постоянной кислотности. · Электролит оцинкования Состав электролита: 80 г сульфата цинка, 12-15 г глауберовой соли, 12-15 г сульфата аммония растворить в 400 мл воды. Приготовленный раствор вылить в гальваническую ванну (химический стакан). Сульфат аммония вводят для поддержания постоянной кислотности. 3. Обработка поверхности катода. · Процесс омеднения. Пластину из малоуглеродистой стали поместить на 3-5 мин в 5% раствор серной или соляной кислоты и промыть в воде. Затем надо пластину обезжирить. Для обезжиривания пластину помещают в 2М раствор гидроксида натрия на 3-5 мин и затем промывают в воде. Обсушить фильтровальной бумагой и взвесить на весах. · Процесс никелирования Пластину из малоуглеродистой стали поместить на 3-5 мин в 5% раствор серной или соляной кислоты и промыть в воде. Затем надо пластину обезжирить. Для обезжиривания пластину помещают в горячий 10% раствор соды и затем промывают в воде. Обсушить фильтровальной бумагой и взвесить на весах. · Процесс оцинкования Пластину из малоуглеродистой стали поместить на 3-5 мин в 5% раствор серной или соляной кислоты и промыть в воде. Затем надо пластину обезжирить. Для обезжиривания пластину помещают в горячий 10% раствор соды и затем промывают в воде. Обсушить фильтровальной бумагой и взвесить на весах. 4. Расчет силы тока · Для процесса омеднения При омеднении изделий плотность тока не должна превышать 3-5А на 1дм2покрываемого изделия (катода). Для этого можно провести следующие простые расчеты: на площади в 100 см2 катода сила тока должна быть 5 А, а на S(площади пластинки) сила тока ровна Χ. Отсюда Χ= Χ - сила тока; S – поверхность катода, см2 · Для процесса никелирования При никелировании изделий плотность тока должна быть 1А на 1 дм2 покрываемой поверхности, т.е. Χ= Χ - сила тока S – поверхность катода, см2 · Для процесса оцинкования При оцинковании изделий плотность тока рассчитывают исходя из того, на 1 дм2 покрываемой поверхности необходима сила тока в 2А. Отсюда, Χ= Χ - сила тока S – поверхность катода, см2
|

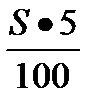 ,где
,где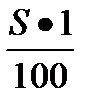 ,где
,где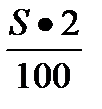 ,где
,где


