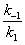Михаэлиса константа, один из важнейших параметров кинетики ферментативных реакций, введенный немецкими учеными Л. Михаэлисом (L. Michaelis) и М. Ментен в 1913; характеризует зависимость скорости ферментативного процесса от концентрации субстрата. Согласно теории Михаэлиса — Ментен, первым этапом любого ферментативного процесса является обратимая реакция между ферментом (Е) и субстратом (), приводящая к образованию промежуточного фермент-субстратного комплекса (ES), который затем подвергается практически необратимому расщеплению на продукт реакции (Р) и исходный фермент:


Реакции образования и распада комплекса ES характеризуются константами скорости k 1, k -1, k 2. Если концентрация субстрата значительно превышает концентрацию фермента (S) >> (E)) и, следовательно, концентрация ES становится постоянной, скорость ферментативной реакции (u) выражается уравнением:2
где — максимальная скорость реакции, достигаемая при полном насыщении фермента субстратом. Соотношение констант скорости
где — максимальная скорость реакции, достигаемая при полном насыщении фермента субстратом. Соотношение констант скорости

также является константой (Кm), получившей название Михаэлиса константа Подставляя в уравнение (2) Михаэлиса константа, получаем уравнение Михаэлиса — Ментен:

Из уравнения (3) следует, что Михаэлиса константа численно равна концентрации субстрата, при которой скорость реакции составляет половину максимально возможной (см. рис.). В ряде случаев, когда величина k 1 мала и ею можно пренебречь, Михаэлиса константа становится равной
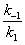
и может служить мерой сродства субстрата к ферменту. Михаэлиса константа имеет размерность концентрации. Практически величину Михаэлиса константа находят различными графическими методами, исследуя зависимость скорости ферментативной реакции от концентрации субстрата.