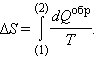править]Закон о растворимости компонентов газовой смесиПри постоянной температуре растворимость в данной жидкости каждого из компонентов газовой смеси, находящейся над жидкостью, пропорциональна их парциальному давлению.
7. определение работы при изменений объема A = P·(V2- V1) = P·∆V. 8. первое начало термодинамики для бесконечно-малых приращений
Для конечных приращений хз) 9)выражение для внутренней энергии идеального газа U=3/2VRT
V(ню)-молярная масса,можно заменить как m/M R=8.31ДЖ Т-температура в кельвинах(к температуре в градусах прибавляешь 273) 10) Теплоемкость тела это физическая величина, равная количеству теплоты, которое необходимо сообщить телу, чтобы изменить его температуру на 10К. Удельная теплоёмкость - физическая величина, численно равная количеству теплоты, которое необходимо передать телу массой 1 кг для того, чтобы его температура изменилась на 1 Кельвин. Удельная теплоемкость обозначается буквой c и измеряется в Дж/кг*Кельвин. молярная теплоёмкость — это теплоёмкость одного моля вещества. 11)соотношение майера для идеального газа Сp-Cv=R R-универсальная газовая постоянная, Cp-молярная теплоёмкость при постоянном давлении Cv-молярная теплоёмкость при постоянном объёме. 12. P-V
T-V
13)закон равнораспределения РАВНОРАСПРЕДЕЛЕНИЯ ЗАКОН - теорема классической статистической физики, согласно которой на каждую степень свободы системы в равновесном состоянии приходится средняя энергия kT/2, где k - Больцмана постоянная, T - абсолютная температура
15)ФОРМУЛИРОВКА второе начало термодинамики При перемещении какого-либо тела на какое-либо расстояние под действием определенной силы совершается работа, и различные формы энергии как раз и выражают способность системы произвести определенную работу. Поскольку теплота, отражающая кинетическую энергию молекул, представляет собой одну из форм энергии, она тоже может быть преобразована в работу. Но опять мы имеем дело с направленным процессом. Перевести работу в теплоту можно со стопроцентной эффективностью — вы делаете это каждый раз, когда нажимаете на педаль тормоза в своем автомобиле: вся кинетическая энергия движения вашего автомобиля плюс затраченная вами энергия силы нажатия на педаль через работу вашей ноги и гидравлической системы тормозов полностью превращается в теплоту, выделяющуюся в процессе трения колодок о тормозные диски 16.
Показатель адиабаты (
Таким образом, для одноатомного идеального газа (три степени свободы) показатель адиабаты равен:
в то время как для двуатомного идеального газа (пять степеней свободы) (при комнатной температуре):
17)цикл Карно в п-в Полная работа за цикл A = A1 + A2 на диаграмме (p, V) равна площади цикла. Работа A положительна, если цикл обходится по часовой стрелке, и A отрицательна, если цикл обходится в противоположном направлении. 18. неравенство клаузиуса в общем случае
19.Энтропия систем
20 изолированная
т.е. для любого процесса в изолированной системе энтропия конечного состояния не может быть меньше энтрпии начального состояния. Это – закон возрастания энтропии. Не изолированная
|

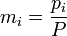
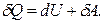
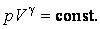
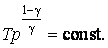
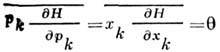 (чертой сверху обозначено усреднение с помощью классич. канонического распределения Гиббса
(чертой сверху обозначено усреднение с помощью классич. канонического распределения Гиббса
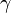 ) для идеального газа может быть выражен через количество степеней свободы (
) для идеального газа может быть выражен через количество степеней свободы (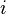 ) молекул газа:
) молекул газа: или
или 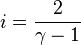
 ,
,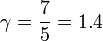 .
.
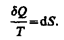 Функция состояния, дифференциалом которой является dQ/T, называется энтропией и обозначается S.
Функция состояния, дифференциалом которой является dQ/T, называется энтропией и обозначается S.