Анализ карбонатного сырьяОпределение влажности карбонатного сырья. На аналитических весах в бюксе взвешивают 2-3 г тонкоизмельченного исходного материала (задается преподавателем) и помещают его в сушильный шкаф при температуре 105-110°С на 1,5-2 ч. Затем бюкс вынимают из шкафа, охлаждают до комнатной температуры и взвешивают. Для проверки постоянства массы навеску снова высушивают в течение 30 мин. Удаление влаги считают полным, если при двух последовательных взвешиваниях пробы ее вес не изменяется. Влажность материала W, %, рассчитывается из соотношения
где т 1 - масса бюкса с навеской до высушивания, г; т 2 - масса бюкса с навеской после высушивания, г; т - масса навески, г. Определение потерь при прокаливании. Навеску исходного материала (задается преподавателем) около 1 г, высушенную при 105-110°С до постоянной массы, в фарфоровом тигле помещают в муфельную печь при температуре 950-1000°С и выдерживают при этой температуре не менее 1 ч. Затем тигель с навеской охлаждают до комнатной температуры, взвешивают и повторяют прокаливание в течение 30 мин. Если при двух последовательных взвешиваниях пробы ее вес не изменился, испытания считают завершенными. Потери при прокаливании ппп, %, вычисляют по формуле
где т 1 - масса фарфорового тигля с навеской до прокаливания, г; т 2 - масса фарфорового тигля с навеской после прокаливания, г; т - масса навески, высушенной при температуре 105-110°С, г. Определение нерастворимого в HCl остатка. Навеску карбонатной породы 1 г, взвешенную на аналитических весах, помещают в стакан объемом 200 мл, приливают 50-60 мл воды и, прикрывая часовым стеклом, постепенно прибавляют 30 мл 10%-ной соляной кислоты. После прекращения выделения пузырьков углекислого газа раствор нагревают до кипения и фильтруют через беззольный фильтр. Осадок на фильтре промывают горячей водой до отрицательной реакции промывных вод на ион хлора (отсутствие помутнения фильтрата при добавлении к нему 1%-го раствора азотнокислого серебра), помещают во взвешенный фарфоровый тигель, осторожно подсушивают и озоляют, не допуская воспламенения фильтра, затем прокаливают до постоянной массы при температуре 900-1000°С, охлаждают до комнатной температуры и взвешивают. Содержание нерастворимого в соляной кислоте остатка Н. О. в процентах вычисляют по формуле
где т 1 - масса прокаленного остатка, г; т - сухая навеска карбонатной породы, г. Определение оксида кремния. Навеску карбонатной породы около 0,5 г сплавляют в тигле с 3 г углекислого натрия. Сплав обрабатывают горячей водой, переносят в фарфоровую чашку, осторожно добавляют соляную кислоту до прекращения выделения пузырьков углекислого газа. Затем раствор выпаривают на песчаной бане, по каплям добавляют 5-8 мл соляной кислоты (r = 1,19 г/см3), выдерживают 10 мин под часовым стеклом, прибавляют 30 мл горячей дистиллированной воды и фильтруют через беззольный фильтр. Осадок вместе с фильтром переносят во взвешенный тигель, высушивают, озоляют и прокаливают в печи при температуре 900-1000°С в течение 20 мин. Затем тигель охлаждают и взвешивают. Для проверки постоянства массы прокаливание повторяют в течение 15 мин. Содержание SiO2, %, определяют по формуле
где т 1 - масса остатка, г; т - масса сухой навески карбонатной породы, г. Определение суммарного содержания оксида кремния и нерастворимого в HCl остатка. Один грамм навески карбонатной породы переносят количественно в фарфоровую чашку и осторожно добавляют, прикрывая часовым стеклом, 10-15 мл концентрированной соляной кислоты (r = 1,19 г/см3). Часовое стекло после окончания реакции обмывают дистиллированной водой, после чего фарфоровую чашку ставят на песчаную баню для выпаривания раствора досуха. В охлажденную чашку с осадком добавляют 5-7 мл концентрированной соляной кислоты (r = 1,19 г/см3). После растворения осадка раствор выпаривают досуха на песчаной бане. К осадку добавляют 5 мл концентрированной соляной кислоты, разведенной водой в отношении 1: 1, и 25-30 мл горячей дистиллированной воды. Раствор затем фильтруется через беззольный фильтр на воронке Бюхнера. Промывка осадка на фильтре производится горячей дистиллированной водой до исчезновения реакции на ион хлора. Фильтр вместе с осадком переносят в тигель, осторожно сжигают в муфельной печи и затем прокаливают при температуре 900-1000°С до постоянной массы. Суммарное содержание SiO2 + Н. О., % рассчитывается из уравнения
где т 1 - масса тигля с осадком, г; т 2 - масса пустого тигля, г; т - масса исходной навески, г. Определение суммы полуторных оксидов R2O3. Для определения R2O3 фильтрат, оставшийся после определения SiO2 и нерастворимого в HCl остатка, выпаривают на водной бане до объема порядка 100-150 мл, после чего к нему добавляют несколько капель концентрированной HNO3 (r = 1,64 г/см3). Раствор доводят до кипения и к нему осторожно добавляют 10%-ный раствор NH4OH до появления слабого запаха аммиака. Образовавшийся осадок отфильтровывают через беззольный фильтр и промывают горячей дистиллированной водой до исчезновения реакции на хлорид-ион. Фильтр с осадком переносят в тигель, осторожно сжигают и прокаливают. Содержание R2O3, %, рассчитывают по уравнению
где т 1 - масса прокаленного тигля с осадком, г; т 2 - масса пустого тигля, г; т - масса исходной навески, г. Определение содержания Ca2+ и Mg2+(CaCO3 и MgCO3). Содержание карбонатов кальция и магния определяют комплексонометрическим методом согласно ГОСТ 10398-76. Ион кальция определяют титрованием пробы трилона Б в щелочной среде (рН = 12) в присутствии индикатора мурексида (до перехода розовой окраски в сиреневую). Определение суммарного содержания ионов Ca2+ и Mg2+ производится титрованием пробы раствором трилона Б в среде аммиачного буферного раствора в присутствии индикатора хромоген черный или хром темно-синий. Окраска раствора изменяется при этом от малиново-красной до синей. Содержание в растворе ионов магния определяется по разности между показаниями первого и второго титрований. Фильтрат после определения R2O3 количественно переносят в мерную колбу емкостью 250 мл и доводят объем раствора до метки дистиллированной водой. Из мерной колбы отбирают 25 мл раствора в коническую колбу, добавляют к нему 50-100 мл дистиллированной воды, 5-10 мл 1 н раствора NaOH для создания щелочной среды, 5-6 капель индикатора мурексида и титруют 0,05-0,1 н раствором трилона Б до перехода розовой окраски в сиреневую. Содержание Ca2+ в пересчете на СаСО3, %, рассчитывают по формуле
где V - количество трилона Б, пошедшее на титрование пробы, мл; K - поправочный коэффициент к нормальности трилона Б; H - нормальность раствора трилона Б; Титрованием раствором трилона Б пробы с индикатором хром темно-синий получают суммарное содержание ионов Са2+ и Mg2+ в растворе. Титруя параллельную пробу трилоном Б с мурексидом получают содержание в растворе ионов Са2+. Расчет содержания MgCO3, %, производится по формуле
где V 1 - количество трилона Б, пошедшее на титрование пробы с индикатором хром темно-синий, мл; V 2 - количество трилона Б, пошедшее на титрование пробы с индикатором мурексид, мл; K - поправочный коэффициент к нормальности раствора трилона Б; H - нормальность раствора трилона Б; Определение общего содержания карбонатов кальция и магния. Этот метод пригоден при анализе высокосортного, стабильного по составу карбонатного сырья. Для определения общего количества карбонатов кальция и магния (в пересчете на СаСО3) берут навеску карбонатной породы около 0,5 г (но не более 0,55 г) и обрабатывают 25 мл дистиллированной воды. Добавив затем точно 25 мл 0,5 н HCl, коническую колбу накрывают часовым стеклом и при перемешивании доводят раствор до кипения. Кипятят 1-2 мин. При этом все крупные частицы сырья должны прореагировать с соляной кислотой до полного разложения карбонатов. Помогает этому легкое разминание частиц стеклянной палочкой. Обмыв стекло, стенки конической колбы и палочку струей воды из промывалки, избыток раствора HCl оттитровывают по метиловому оранжевому 0,5 н NaOH. Общее содержание СаСО3 + MgСО3 в пересчете на СаСО3, %, определяют по формуле
где V 1 - количество 0,5 н раствора HCl, взятое для перевода карбонатов кальция и магния в хлориды, мл (V 1 = 25 мл); K 1 - коэффициент нормальности раствора HCl по отношению к строго 0,5 н раствору HCl; V 2 - количество 0,5 н раствора NaOH, затраченное на титрование избытка 0,5 н раствора HCl, мл; K 2 - коэффициент нормальности рабочего 0,5 н раствора NaOH по отношению к строго 0,5 н раствору HCl; Т - титр строго 0,5 н HCl, выраженный в СаСО3 (Т = 0,025023); g - навеска карбонатной породы, г.
|

 ,
,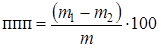 ,
,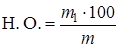 ,
,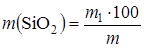 ,
,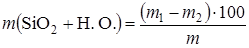 ,
,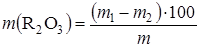 ,
,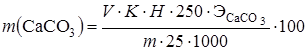 ,
,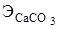 - масса 1 г·экв СаСО3 (
- масса 1 г·экв СаСО3 (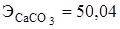 ); т - навеска исходного материала, г.
); т - навеска исходного материала, г. ,
,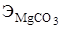 - масса 1 г·экв MgСО3 (
- масса 1 г·экв MgСО3 (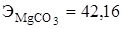 ); т - навеска исходного материала, г.
); т - навеска исходного материала, г.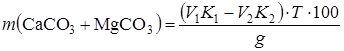 ,
,


