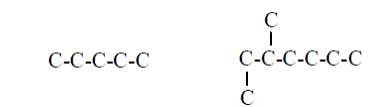Классификация органических соединений
I Классификация по природе углеводородного скелета
Все органические соединения в зависимости от строения углеродной цепи - скелета – делят на следующие большие группы: 1. Ациклические соединения ( алифатические соединения или соединения жирного ряда) – соединения с открытой (незамкнутой) цепью углеродных атомов. 1.1 Парафиновые соединения (соединения предельного ряда, насыщенные).
1.2 Непредельные жирные соединения (ненасыщенные), содержащие двойные, тройные углерод -углеродные связи.
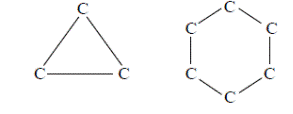
2 Циклические соединения – соединения, в которых углеродные атомы образуют цикл. 2.1 Карбоциклические соединения содержат в молекуле кольца углеродные атомы: 2.1.1 Алициклические соединения – все изоциклические соединения, за исключением бензола и его производных: насыщенные или циклопарафины; ненасыщенные, содержащие в цикле или в боковой цепи двойные или тройные углерод – углеродные связи.
2.1.2 Ароматические соединения – молекулы циклической группировки из шести атомов углерода, находящихся во втором валентном состоянии.
2.2 Гетероциклические соединения – циклы, в состав которых кроме атомов углерода входят и другие атомы – гетероатомы (атомы азота, серы, кислорода).
II. Классификация по природе функциональной группы. Органические соединения по вышеуказанному признаку могут делиться на углеводороды и их производные. Углеводороды (УВ)– органические соединения, в молекулы которых входят атомы лишь двух элементов: углерода и водорода (R- H, R- углеводородный радикал) .
В зависимости от характера функциональной группы все органические вещества делят на многочисленные классы (при замене атомов водорода в углеводородах на другие атомы или группы атомов – функциональные группы):
Таблица 1 Функциональные группы и классы органических соединений (R- углеводородный радикал)
Из этого ряда видно, что функциональная группа, связанная с радикалом, определяет класс соединения. Каждый из этих классов делится в зависимости от характера связи между углеродными атомами на две группы: предельные и непредельные. Полифункциональными называют соединения, содержащие несколько одинаковых функциональных групп. Гетерофункциональными называют органические соединения, характеризующиеся присутствием в молекуле нескольких различных функциональных групп. Для каждого класса органических соединений характерно существование гомологического ряда. Такие ряды являются подтверждением основного закона природы – перехода количественных изменений в качественные. Гомологический ряд (от греч. homos – «последовательный») – ряд соединений с близкими химическими и закономерно изменяющимися физическими свойствами, в котором каждый член отличается от предыдущего на одну группу СН2. 3 Алканы Алканы ( парафины) - алифатические предельные углеводороды, в молекулах которых атомы углерода связаны между собой простой (одинарной связью) s - связью. Общая формула гомологического ряда предельных углеводородов имеет вид СnH2n+2. Простейшим представителем предельных углеводородов является метан СН4. Структурная формула метана имеет вид
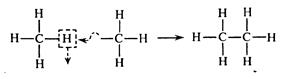
При последовательном замещении в углеводородах атомов водорода на одновалентный остаток, или радикал –СН3, называемый метилом, получается гомологический ряд углеводородов, начинающийся от метана, причем каждый последующий член этого ряда по составу отличается от предыдущего на одну группу СН2. Отдельные члены этого ряда называются гомологами.
Если углеводород лишается одного атома водорода, то образуется частица, называемая углеводородным радикалом или углеводородным остатком. Одновалентные углеводородные радикалы называются алкилами. Сокращенно радикалы обозначаются R или Alk. Общая формула одновалентных радикалов СnH2n+1. Таблица 2 Алканы
|