Теплоемкость. Запишем уравнение первого закона термодинамики для бесконечно малого изменения состояния системыЗапишем уравнение первого закона термодинамики для бесконечно малого изменения состояния системы dQ = dU + dА (4.9) dU является функцией состояния, а dQ и dА не являются функциями состояния системы. Они являются характеристиками процесса. Если нет процесса, то работа и теплота равны нулю. В термодинамике большую роль играют круговые процессы - циклы. В двигателе внутреннего сгорания, в паровой машине совершаются такие циклы, позволяющие получить работу в тепловом процессе сжигания топлива. Если единственной работой является работа расширения идеального газа, вычисляемая по уравнению dA = p dV, (4.10) то уравнение первого закона термодинамики примет вид dQ = dU + рdV. (4.11) Введем понятие истинная теплоемкость при постоянном объеме и постоянном давлении. При постоянном объеме (V = const) dV =0 и dQV = dU, (4.12) и мы получим выражение теплоемкости при постоянном объеме
Запишем уравнение первого закона термодинамики при р = const dQp = dU + рdV (4.14) dQp = d(U + рV) dQp = dН, (4.15) где H – энтальпия химической реакции H = (U +pV). Из уравнения (4.15) выражение теплоемкости при постоянном давлении
Отметим, что единственный случай, когда теплота физико-химического процесса является функцией состояния, то есть определяется начальным и конечным состояниями системы, отражена в уравнениях (4.12) и (4.15). Величины удельной и мольной теплоемкости индивидуальных соединений имеют размерности [Дж/г× К] и [Дж/моль× К] соответственно. Между мольными теплоемкостями идеального газа при постоянном давлении и объеме существует связь. Её можно получить из уравнения (4.16):
Поскольку внутренняя энергия идеального газа не зависит от давления и объема,
Используя уравнение состояния идеального газа, найдем, что Ср = СV + R. (4.17) Газовая постоянная R = 8.314 Дж/моль К имеет ту же размерность, что и мольная теплоемкость.
Пример. Вычислим количество энергии, которое необходимо для нагревания 1 г воды (Ср = 4.18 Дж/г К) и 1 г железа (Ср = 0.448 Дж/г К) – от 25 до 100 0С.
|

 . (4.13)
. (4.13) . (4.16)
. (4.16)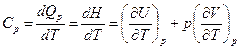 .
. и
и  .
. , тогда
, тогда


