Определение кинетических параметров реакции
Основными кинетическими параметрами формально простой химической реакции являются порядок по компонентам, константа скорости и энергия активации реакции. Они определяются из экспериментальных зависимостей концентрации реагирующих веществ (или величин пропорциональных концентрации) от времени и температуры. Для экспериментального определения порядка реакции (x и y в кинетическом уравнении) и константы скорости при конкретной температуре (k) обычно используют способ избыточных концентраций. Добавление в реакционную смесь в большом избытке всех реагирующих веществ, кроме одного, позволяет считать, что их концентрация в ходе реакции не меняется. Рассмотрим, например, реакцию n AA + n BB =n DD + n EE. Зависимость ее скорости от концентрации реагентов определяется уравнением
Если С 0 B > > C 0 A , то можно считать, что в ходе реакции концентрация вещества В не меняется(СB = С 0 B – const). Тогда
Это позволяет определить порядок реакции по компоненту А (x) дифференциальным или интегральным методами. Дифференциальный метод. Порядок реакции по компоненту А (x) и константу скорости рассчитывают по экспериментально определенной зависимости скорости реакции от концентрации вещества, не находящегося в избытке (v = f (CA)). Поскольку
Рис. 2.6. Дифференциальный метод определения порядка реакции по компоненту
Порядок реакции x может быть как целым, так и дробным. Экспериментальные точки должны ложиться на прямую в пределах ошибки измерений. Если это условие не выполняется, то реакция не является формально простой, и уравнение закона действующих масс для ее описания неприменимо. Интегральный метод. Порядок реакции по компоненту А (x) определяют по виду экспериментальной зависимости концентрации этого вещества от времени протекания реакции (CA = f (t)). Эта зависимость является линейной в координатах С – t для реакций нулевого порядка (рис. 2.7, а), ln C – t – первого (рис.2.7, б),
Рис. 2.7. Изменение концентрации вещества А (CA) во времени t, если кинетическое уравнение имеет вид 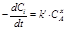 : а – x =0; б – x =1; в – x =2 : а – x =0; б – x =1; в – x =2
Энергия активации химической реакции определяется из экспериментальной зависимости константы скорости (скорости реакции) от температуры. Поскольку  , то очевидно, что в координатах ln k –1/ T зависимость константы скорости от температуры представляет собой прямую линию. Тангенс угла наклона прямой равен E ак/ R (рис. 2.8). , то очевидно, что в координатах ln k –1/ T зависимость константы скорости от температуры представляет собой прямую линию. Тангенс угла наклона прямой равен E ак/ R (рис. 2.8).
Рис. 2.8. Зависимость логарифма константы скорости реакции (ln k) от обратной температуры (1/ Т, К)
|

 , x¹ n A; y¹ n B.
, x¹ n A; y¹ n B. ;
;  .
. , то в координатах ln v –ln CA зависимость скорости реакции от концентрации вещества А будет представлять собой прямую линию (рис. 2.6). Причем тангенс угла наклона этой прямой равен x, а отрезок, отсекаемый на оси ln v, равен ln k ¢.
, то в координатах ln v –ln CA зависимость скорости реакции от концентрации вещества А будет представлять собой прямую линию (рис. 2.6). Причем тангенс угла наклона этой прямой равен x, а отрезок, отсекаемый на оси ln v, равен ln k ¢.
 – t – второго порядка (рис.2.7, в). Тангенс угла наклона прямой в соответствующих координатах равен k ¢. Если экспериментальные точки в соответствующих координатах не ложатся на прямую линию в пределах ошибки измерений, то порядок реакции не равен 0, 1, 2 и должен определяться другим способом.
– t – второго порядка (рис.2.7, в). Тангенс угла наклона прямой в соответствующих координатах равен k ¢. Если экспериментальные точки в соответствующих координатах не ложатся на прямую линию в пределах ошибки измерений, то порядок реакции не равен 0, 1, 2 и должен определяться другим способом.




