Определение содержания кислот в нефтепродуктах путем титрования.Титрование – процесс постепенно прибавления титрованного рабочего раствора к определяемому веществу. Титрование продолжают до тех пор, пока количество титранта не станет эквивалентным количеству реагирующего с ним определяемого вещества. Метод кислотно-основного титрования основан на реакциях взаимодействия между кислотами и основаниями, то есть на реакции нейтрализации. Рабочими растворами метода являются растворы сильных кислот (HCl, H2S, НNОз и др.) или сильных оснований (NaOH, КОН, Ва (ОН) 2 и др.). В зависимости от титранта метод кислотно-основного титрования подразделяют на ацидиметрию, если титрантом является раствор кислоты, и алкалиметрию, если титрантом является раствор основания. Рабочие растворы в основном готовят как вторичные стандартные растворы, поскольку исходные для их приготовления вещества не являются стандaртными, а затем их стандартизуют по стандартным веществам или стандартным растворам. Точка эквивалентности и конечная точка титрования. Согласно правилу эквивалентности титрование необходимо продолжать до тех пор, пока количество прибавленного реагента не станет эквивалентным содержанию определяемого вещества. Наступающий в процессе титрования момент, когда количecтвo стандартного раствора реагента (титранта) становится теоретически строго эквивалентным количеству определяемого вещества согласно определенному уравнению химической реакции, называют точкой эквивалентности. Точку эквивалентности устанавливают различными способами, например по изменению окраски индикатора, прибавляемого в титруемый раствор. Момент, при котором происходит наблюдаемое изменение цвета индикатора, называют конечной точкой титрования. Очень часто конечная точка титрования не совсем совпадает с точкой эквивалентности. Как правило, они отличаются друг от друга не более чем на 0,02-0,04 мл (1-2 капли) титранта. Это то количество титранта, которое необходимо для взаимодейcтвия с индикатором.
29. Определить массовую долю (%) компонентов газовой смеси по следующим данным:
ωi = ωпропан = ωбутан = ωпентан =
30.Для определения олефиновых углеводородов в бензине в пробу объемом 4 мл добавили 1 г йода. После взаимодействия на титрование остатка йода пошло 26 мл 0,1 нормального раствора тиосульфата натрия. Каково содержание олефиновых углеводородов в бензине и соответствует ли он требованиям ГОСТ Р 51866-2002?
31, 40!! ГЖХ-анализ бензина дал следующие значения площадей пиков… Дано: Бутан S=10; Пентан S=20, Средние и тяжелые фракции S=170. Методом внутренней нормализации рассчитать содержание бутана и пентана в образце бензина,калибровочный коэффициент f=1. Решение:
32. Для определения полной динамической емкости (ПДОЕ) катионита через колонку с 5 г катионита в Н+- форме пропустили 350,0 мл 0,05 н раствора СаСl2. При определении Са(2+) в элюате в порциях по 50,00 мл были получены следующие значения концентраций: 0,0030; 0,0080; 0,0150; 0,0250; 0,0400; 0,0500 и 0,0500 моль экв/л. Определить ПДОЕ катионита по кальцию. H+- mкатионита = 5 г V = 350 мл Cн = 0,05 Н раствора СаСl2 Са(2+) V=50 мл Cн = 0,0030; 0,0080; 0,0150; 0,0250; 0,0400; 0,0500; 0,0500 моль экв/л. n1 =(Cн*V)Са2+ = 350*0,05 = 17,5 (мэкв) n2 = n3 = n1 – n2 = 17,5 – 13,4 = 4,1 (мэкв) ПДОЕ =
Ширина основания хроматографического пика (m) метанола составляет 16 мм. Расстояние на хроматограмме от момента введения пробы до середины пика метанола (l) составляет 8 см. Вычислить число теоретических тарелок данной колонки. n =16*(l/m)2 = 16*(80/16)2 = 400
34 Ежедневный анализ НП в сточных водах дал следующие результаты в мг/л: 0,38; 0,32; 0,31; 0,32; 0,33; 0,29; 0,32; 0,32; 0,33;0,39
|

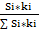 *100%
*100%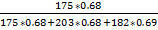 *100% = 31.1 %
*100% = 31.1 %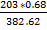 *100% =36.08 %
*100% =36.08 %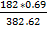 *100% =32.82 %
*100% =32.82 %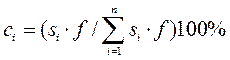 ;
;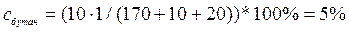
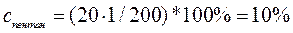 , где с-концентрация определяемого компонента в весовых процентах.
, где с-концентрация определяемого компонента в весовых процентах.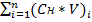 = 0,003*50+0,008*50+0,015*50+0,025*50+0,04*50+0,05*50+0,05*50 = 13,4 (мэкв)
= 0,003*50+0,008*50+0,015*50+0,025*50+0,04*50+0,05*50+0,05*50 = 13,4 (мэкв)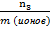 = 4,1/5 = 0,82 мэкв/г
= 4,1/5 = 0,82 мэкв/г


