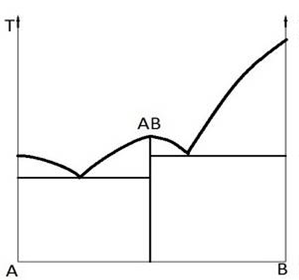
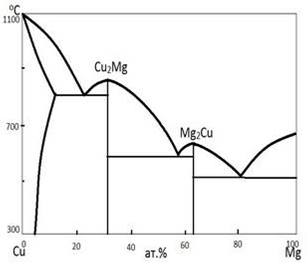
Диаграммы состояния двойных равновесных систем.в общей случае представляет собой пространственную фигуру, имеющую три координатные оси: концентраций одного из компонентов, температур и давлений. Если система конденсирована, то ее равновесное состояние можно изобразить более простой плоской диаграммой, являющейся изобарным сечением пространственной фигуры (например, при атмосферном давлении). Такую диаграмму называет изобарной диаграммой равновесного состояния конденсированной системы. Однако, в литературе вместо этого слишком длинного термина обычно применяют более краткие названия: диаграмма состояния, фазовая диаграмма, диаграмма плавкости и др. Ограничимся рассмотрением конденсированных двойных систем с образованием химических соединений. Диаграмма состояния системы, где компоненты А и В образуют соединение АВ, приведена на рис. 2.1. В этом случае диаграмма состояния разбивается ординатой соединения на две самостоятельные системы эвтектического типа: А−АВ и АВ−В. Соединений может быть и больше. В соответствии с их числом диаграмма состояния в целом разбивается на (n+1) простых двойных систем, где n − число образующихся химических соединений. В системе Cu−Mg, например, кристаллизуются два соединения Cu2Mg и Mg2Cu, которым отвечают две дистектики на диаграмме состояния (рис. 2.2).
Рис. 2.1. Диаграмма состояния двойной конденсированной системы с образованием прочного химического соединения и в отсутствие твердых растворов
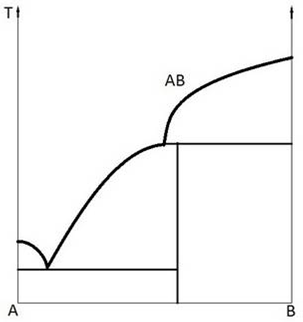
Рис. 2.2. Диаграмма состояния системы Сu – Mg Химическое соединение (рис. 2.1), плавящееся без разложения, называют конгруэнтно плавящимся. Возможно образование химического соединения по перитектической реакции между твердой и жидкими фазами (рис. 2.3) В + ж ↔АВ.
Рис. 2.3. Диаграмма состояния двойной конденсированной системы с образованием инконгруэнтно плавящегося (растворяющегося) химического соединения и в отсутствие твердых растворов
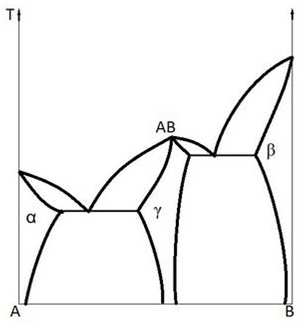
Рис. 2.4. Диаграмма состояния двойной конденсированной системы с образованием химического соединения и твердых растворов: α и β-поля твердых растворов на основе компонентов А и В соответственно, γ -поле твердого раствора на основе химического соединения АВ Такое соединение называют инконгруэнтно плавящимся (плавящимся с разложением). В системе с образованием химического соединения нередко происходит образование эвтектик между твердыми растворами на основе чистых компонентов и твердым раствором на основе химического соединения (рис. 2.4). Образование твердых растворов изменяет характер равновесия в системе и оказывает решающее влияние на эффективность синтетических реакций − на выход и чистоту получаемых соединений. Диаграммы состояния двойных систем в настоящее время изучены достаточно хорошо. Вряд ли найдется сочетание двух элементов периодической системы, для которых не была бы известна диаграмма состояния. Изучено много систем с неорганическими солями в качестве компонентов, диаграмм растворимости с применением органических и неорганических растворителей. Термин "диаграмма растворимости" применяется для систем, у которых основная фаза при обычных условиях является жидкой. В неорганическом синтезе особенно часто пользуются диаграммами растворимости при переработке водных растворов солей, связанной с их растворением и кристаллизацией. Анализ фазовых превращений с помощью этих диаграмм позволяет установить и закономерности образования природных солевых залежей, а в некоторых случаях предвидеть не только их состав, но и условия залегания. Реакции соединения − разложения и диспропорционирования, протекающие в двойной системе, могут протекать и по бинарному сечению тройной или какой-либо другой многокомпонентной системы. В последнем случае равновесие не отличается по характеру протекания от равновесия в двойной системе при условии, что выделяемое соединение достаточно прочно.
|