Мутность.Мутность воды определяют фотометрически - путем сравнения пробы воды со стандартными суспензиями. Мутность (в мг/л) определяют по калибровочному графику. Согласно требованиям ГОСТа мутность питьевой воды не должна превышать 1,5 мг/л. Калибровочный график строят по стандартным рабочим суспензиям. Для этого готовят рабочие суспензии с концентрацией каолина 0,5; 1,0; 1,5; 2,0; 3,0; 4,0; 5,0 мг/л. На спектрофотометре «ЮНИКО 1201» измеряют оптические плотности этих суспензий при длине волны 530 нм. Получают следующие значения оптических плотностей и соответствующие им значения мутности: Мутность, мг/л 5 10 15 20 30 40 50 Оптическая ОД 0,2 0,3 0,4 0,6 0,8 1,0 плотность По полученным данным постройте калибровочный график зависимости оптической плотности от мутности. Измерение мутности проводится в неотфильтрованной пробе воды. В качестве раствора сравнения используется отфильтрованная вода исследуемой пробы. Проведите определение оптической плотности исследуемой воды на спектрофотометре «ЮНИКО 1201» при длине волны 530 нм. По полученному значению оптической плотности определите на калибровочном графике соответствующее значение мутности для исследуемого образца. Результат запишите в табл. 1, после чего сделайте вывод о соответствии исследуемой воды нормативу ГОСТ.
Литература: 1. Андруз Дж., Бримблекумб П., Джикелс Т., Лисс П. Введение в химию окружающей среды. Пер. с англ. – М.: Мир, 1999. – 271 с. 12. Голдовская Л.Н. Химия окружающей среды. М. БИНОМ. ЛЗ 2008г. – 295 с. 13. Маршал В. Основные опасности химических производств. М.: Мир. 1989. 14. Скурлатов Ю.И. и др. Введение в экологическую химию: Учеб. пособие для хим. и хим.-технолог. спец. вузов/ Ю.И. Скурлатов, Г.Г. Дука, А. Мизити. – М.: Высшая школа, 1994. -400 с. 15. Тинсли И. Поведение химических загрязнителей в окружающей среде. М.: Мир, 1982. 16. Химия окружающей среды. Под ред. Дж. Бокриса. Перевод с англ. - М. Химия 1982г. 672 с. Занятие № 7 Тема: Основные направления и методы снижения экологического риска загрязнения окружающей среды. Исходный уровень: загрязнитель, вредное вещество, окружающая среда . Учебно-целевые вопросы: 1. Методы очистки производственных выбросов в атмосферу от газообразных и аэрозольных загрязняющих веществ. 2. Пути предотвращения выбросов загрязняющих веществ в атмосферу. Разработка и реализация новых технологий, направленных на снижение выбросов "парниковых" газов. 3. Методы предотвращения загрязнения гидросферы, очистка сточных вод. Система оборотного водоснабжения. Озонирование. Опреснение воды. Переработка отходов (химическая и биохимическая обработка отходов). Термические способы обезвреживания. 4. Методы предотвращения и ликвидации вредных последствий в результате применения удобрений и ядохимикатов. Принципы создания комплексных малоотходных технологий. 5. Разработка замкнутых циклов использования природных ресурсов. Научные основы эффективного использования энергоресурсов. Научные предпосылки реализации концепции устойчивого развития общества. Литература: 1. Андруз Дж., Бримблекумб П., Джикелс Т., Лисс П. Введение в химию окружающей среды. Пер. с англ. – М.: Мир, 1999. – 271 с. 17. Голдовская Л.Н. Химия окружающей среды. М. БИНОМ. ЛЗ 2008г. – 295 с. 18. Маршал В. Основные опасности химических производств. М.: Мир. 1989. 19. Скурлатов Ю.И. и др. Введение в экологическую химию: Учеб. пособие для хим. и хим.-технолог. спец. вузов/ Ю.И. Скурлатов, Г.Г. Дука, А. Мизити. – М.: Высшая школа, 1994. -400 с. 20. Тинсли И. Поведение химических загрязнителей в окружающей среде. М.: Мир, 1982. 21. Химия окружающей среды. Под ред. Дж. Бокриса. Перевод с англ. - М. Химия 1982г. 672 с. План лабораторно-практического занятия № 8 Тема: Зачетное занятие.
24. Токсиканты окружающей среды, экологический кризис. 25. Состав и структура атмосферы. 26. Фотохимические реакции в атмосфере. Фотосенсибилизаторы. 27. Химия соединений азота в атмосфере: азот – простое вещество, оксиды азота: химическое строение, реакционная способность. Реакции с участием соединений азота.
ВОПРОСЫ К ЗАЧЕТУ ПО ЭКОЛОГИЧЕСКОЙ ХИМИИ
1. Предмет и задачи экологической химии, ее связь с другими дисциплинами. Основные понятия экологической химии. 2. Структура и функции биосферы, современные представления о ее происхождении и химической эволюции. 3. Экосистемы и их классификация. Законы, лежащие в основе функционирования биосферы. Понятие об экологических факторах, классификация экологических факторов. 4. Круговорот энергии и вещества в биосфере. Энергетический и материальный баланс в биосфере. Природные ресурсы. 5. Токсиканты окружающей среды: определение, классификация. Основные вещества - загрязнители различных природных сред (вода, почва, воздух). Основные каналы загрязнения атмосферы, гидросферы, почв и биоты. 6. Основные экологические проблемы: сдвиг климатического равновесия вследствие накопления различных газов в атмосфере, разрушение озонового слоя, загрязнение природных вод и т.д. Глобальный экологический кризис и его последствия. 7. Состав атмосферы. Основные химические реакции, протекающие в атмосфере. Взаимодействие ионизирующего излучения с компонентами атмосферы. Фотохимические реакции. Свободные радикалы. 8. Азот, оксиды азота: химическое строение, реакционная способность. Атмосферные реакции с участием азота и его соединений. 9. Кислород, озон: химическое строение, реакционная способность. Активные формы кислорода. Вода в атмосфере. Фотолиз воды. Снеговой покров. Токсическое действие кислорода и его активных форм. Повреждение клеточных мембран посредством перекисного окисления. Понятие об антиоксидантах. 10. Углеводороды в атмосфере и продукты их превращений (формальдегид, металлорганические соединения). Токсичность органических веществ в атмосфере. Реакции свободно-радикального окисления органических веществ в атмосфере. 11. Галогенопроизводные углеводородов. Озоновый слой. 12. Оксиды углерода. Загрязнение атмосферы на региональном и глобальном уровне. Парниковые газы и парниковый эффект. 13. Кислотные дожди. Механизмы образования кислотных дождей. Смог лондонского и лос-анджелесского типа. 14. Металлы в атмосфере: основные источники поступление в атмосферу и токсическое действие этих веществ. 15. Источники поступления загрязняющих веществ в атмосферу. Способы очистки выбрасываемых газов. 16. Состав природных вод (морских, речных, грунтовых). Лигандный состав и формы существования основных ионов в природных водоемах. Круговорот основных ионов гидросферы. 17. Кислород и оксид углерода (IV) в гидросфере. Абсорбция газов водной поверхностью. 18. Азот-, фосфор- и серусодержащие соединения в природных водах. 19. Фотохимические реакции в гидросфере. Действие ионизирующего излучения на компоненты гидросферы. 20. Буферные свойства природных водоемов. рН водоемов и его влияние на жизнедеятельность организмов. 21. Классификация типов загрязнений природных вод по фазово-дисперсному состоянию. Оценка степени загрязненности воды. Качество питьевой воды. 22. Формы существования природных металлов в гидросфере. Миграция тяжелых металлов. 23. Загрязнение гидросферы органическими веществами. 24. Процессы самоочищения водоемов. Методы водоочистки и водоподготовки. Ионообменные смолы. 25. Состав литосферы. Состав и функции почв. Плодородие почвы. Почвенные ресурсы. Эрозия почв. 26. Соединения азота и фосфора в почвах, их влияние на живые организмы. Роль азотфиксирующих бактерий в круговороте азота. 27. Основные загрязнители почв: органические соединения (производные фталевой кислоты, диоксины, галогенуглеводороды, полициклические ароматические углеводороды). 28. Основные загрязнители почв: тяжелые металлы. Ртуть, кадмий и свинец, механизм их токсического действия. 29. Минеральные и органические удобрения. Пестициды. 30. Отходы производства и потребления, твердые бытовые отходы. Проблема утилизации твердых бытовых отходов. 31. Круговорот элементов как средство обеспечения взаимосвязи между географическими оболочками Земли.Круговорот кислорода, азота, серы, фосфора, углерода, воды. Транспорт химических веществ в окружающей среде. 32. Критерии оценки качества питьевой воды, атмосферного воздуха, почв, снегового покрова. Понятие о предельно-допустимых концентрациях. Взаимосвязь между токсичностью химического соединения и его предельно-допустимой концентрацией. 33. Предельно допустимые концентрации. Токсикологическое нормирование химических веществ. 34. Экологический мониторинг: ступени, объекты, показатели. Роль мониторинга в анализе и предупреждении опасного развития последствий глобальных антропогенных воздействий. 35. Нормативно-правовые акты, регулирующие взаимоотношения в области экологии и охраны окружающей среды. 36. Обнаружение загрязняющих веществ в атмосфере, воде, почве. Диагностика и эффективный химико-аналитический контроль объектов окружающей среды. Методы контроля воздействия на окружающую среду. 37. Методы очистки производственных выбросов в атмосферу от газообразных и аэрозольных загрязняющих веществ. Разработка и реализация новых технологий, направленных на снижение выбросов "парниковых" газов. 38. Методы предотвращения загрязнения гидросферы и очистка сточных вод. 39. Методы ликвидации вредных последствий применения удобрений и ядохимикатов.
Основная литература: 1. Андруз Дж., Бримблекумб П., Джикелс Т., Лисс П. Введение в химию окружающей среды. Пер. с англ. – М.: Мир, 1999. – 271 с., ил. 2. Бримблкумб П. Состав и химия атмосферы: пер. с англ. М.: Мир, 1998. 3. Голдовская Л.Н. Химия окружающей среды. М. БИНОМ. ЛЗ 2008г. 295 с. 4. Маршал В. Основные опасности химических производств. М.: Мир. 1989. 5. Скурлатов Ю.И. и др. Введение в экологическую химию: Учеб. пособие для хим. и хим.-технолог. спец. вузов/ Ю.И. Скурлатов, Г.Г. Дука, А. Мизити. – М.: Высшая школа, 1994. -400 с.: ил. 6. Тинсли И. Поведение химических загрязнителей в окружающей среде. М.: Мир, 1982. 7. Химия окружающей среды. Под ред. Дж. О. М. Бокриса. Перевод с английского М. Химия 1982г. 672 с. 8. Химия окружающей среды: Пер. с англ./ Под ред. А.П. Цыганкова. М.: Химия, 1982. 9. Экологическая химия. Основы и концепции. Учебное пособие. Перевод с немецкого. М Мир 1997г. 396 с. 10. Экологическая химия: Пер. с нем./ Под ред. Корте Ф. М.: Мир. 1996.
Дополнительная литература: 1. Анализ объектов окружающей среды. Инструментальные методы / Под ред. Р. Сониасси. М.: Мир, 1993. 2. Исидоров В.А. Органическая химия атмосферы. СПб., Химиздат, 2001г. 352 с., с ил. 3. Каталитические реакции и охрана окружающей среды Сычов А.Я., Травон С.О., Дука Г.Г., Скурлатов Ю.И./ Отв. ред. д-р хим. наук Д.Г. Батыр. – Кишинев: Штиинца, 1983. – 272 с., ил. 4. Легасов В.А. и др. Научные проблемы безопасности техносферы // Безопасность труда в промышленности. N1, 1988. с. 44–51. 5. Пэнгл Р. Методы системного анализа окружающей среды: Пер. с англ. / Под ред. Н.Н. Моисеева. М.: Мир, 1979. 6. Реймерс Н.Ф. Природопользование: словарь–справочник. М.: Мысль. 1990. 7. Трифонов К.И., Дивисилов В.А. Физико-химические процессы в техносфере. Учебник. – М.: ФОРУМ: ИНФРА-М, 2007. – 240 с., ил. 8. Фелленберг Г. Загрязнение природной среды. Введение в экологическую химию: Пер. с нем. М.: Мир, 1997. 9. Химия и общество: пер. с англ./ Американское химическое общество. М.: Мир, 1996. 10. Чибисова Н.В. Практикум по экологической химии. – Калининград: Изд-во Калинигр. ун-та, 1999. - 94 с. 11. Чибисова Н.В., Долгань Е.К. Экологическая химия - Калининград: Изд-во Калинигр. ун-та, 1998. - 113 с. 12. Экологическое аудирование промышленных производств. Учеб. пособие. М.: НУМЦ Госкомэкологии России, 1997.
Задания для тестового контроля по курсу «Экологическая химия» 1) Экосистемы – это а) среда обитания животных организмов; б) совокупность сообществ, взаимодействующих с факторами окружающей среды; в) условия окружающей среды, влияющие на живые организмы; г) первичные и вторичные факторы среды обитания живых организмов.
2) Компоненты неживой природы, влияющие на организм – это а) антропогенные факторы; б) абиотические факторы; в) биотические факторы; г) ресурсные циклы.
3) Экологический фактор, количественное значение которого выходит за рамки выносливости вида, называют а) основным; б) фоновым; в) витальным; г) лимитирующим.
4) Сообщество, созданное человеком – это а) биосфера; б) биоценоз; в) агроценоз; г) геобиоценоз.
5) Территория с присущими абиотическими факторами обитания – это а) экосистема; б) биогеоценоз; в) биосфера; г) биотоп.
6) Природная экосистема, не субсидируемая и движимая солнцем – это а)океан; б) агроэкосистема; в) пригороды; г) промышленная зона.
7) Оболочка земли, образованная почвенным покровом – это а) гидросфера; б) литосфера; в) земная кора; г) биосфера.
8) Содержание кислорода в объемных % в нижних слоях атмосферы равно а) 21% б) 78% в) 9% г) 18%
9) Название геохимической функции живого вещества, состоящей в связывании солнечной энергии с дальнейшим ее рассеиванием при потреблении органических соединений а) транспортная; б) концентрационная; в) энергетическая; г) окислительно-восстановительная.
10) К абиотическим факторам относятся: а) температура; б) растительные организмы; в) микроорганизмы; г) деятельность человека.
4) Фотохимические реакции – это реакции а) протекающие по радикальному механизму; б) сопровождающиеся образованием синглетного кислорода; в) протекающие при разрыве химических связей; г) протекающие при разрыве связей в молекулах за счет солнечного излучения.
5) Схема фотосинтеза:
6)
14) Разложение азотной кислоты осуществимо в атмосфере в результате процесса
17) Плотность воды а) в твердом состоянии меньше, чем в жидком; б) в жидком состоянии меньше, чем в твердом; в) одинакова в любой фазе; г) составляет 6,02 КДж/моль.
18) К макрокомпонентам химического состава природных вод относятся: e) Ca(HCO3)2 , Mg(HCO3)2; б) Fe2+, Cu2+, Mn2+, Co2+, Cr2+; в) K+, Na+, Mg2+,Cа2+,Cl-, SO42-, HCO3-; г) O2, N2, H2S, CH4 .
17)Одним из процессов самоочищения водоемов является: а) окисление минеральных и органических соединений; б) механическое удаление грубых примесей; в) коагуляция; г) диализ.
18)Массовая доля твердых частиц в почве составляет а) до 50%; б) 40 – 50%; в) 75-85%; г) 80-90%.
22) В основе строения макромолекулы лигнина лежит а) метиловый спирт; б) кумароновая кислота; в) фенилпропановое звено; г) фенолформальдегидная смола.
23) Попадание избытка нитратов в организм с водой и продуктами ведет к а) их восстановлению до нитритов и метгемоглобинемии; б) перекисному окислению липидов; в) их разложению до N2. 24) Биоконцентрирование - это а) обогащение организма химическими веществами за счет питания и потребления из окружающей среды; б) обогащение организма химическим веществом из окружающей среды; в) обогащение организма химическим веществом за счет питания.
22)Ксенобиотик – это а) вещество, нормируемое ПДК; б) вещество, вызывающее гибель 50% организмов; в) чужеродное для организма химическое вещество; г) чрезвычайно опасное химическое вещество.
23) Концентрация загрязняющего вещества в месте пребывания человека соотносится с ПДК а) С ≤ ПДК; б) С = ПДК; в) С ≥ ПДК.
24) К важнейшим видам абиотических превращений в природных средах относится а) реакция нейтрализации; б) перекисное окисление липидов; в) окислительно-восстановительные реакции.
25)Регулярное наблюдение и контроль за состояние окружающей среды называют а) экологическим мониторингом; б) экологической ситуацией; в) экологическими факторами; г) экологическими последствиями.
26)Вещества, вызывающие повышенную чувствительность организма к воздействию факторов внешней среды - это а) токсины; б) ксенобиотики; в) аллергены; г) канцерогены.
27)Экологическая ситуация, характеризующаяся глубокими необратимыми изменениями окружающей среды и окружающим здоровья населения, называется а) экологическим кризисом; б) экологическим риском; в) экологической ситуацией; г) экологической катастрофой.
28)Разработка и внедрение научно обоснованных, обязательных для внесения технических требований и норм, регламентирующих деятельность по отношению к окружающей среде, называется а) экологической экспертизой; б) экологической стандартизацией; в) экологическим мониторингом; г) экологическим моделированием.
29)Что называется толерантностью к экологическому фактору? а) оптимальная зона; б) диапазон выносливости организма; в) верхний пессимизм; г) нижний пессимизм. 30)Какой показатель не используется для характеристики качества воды? а) плотность; б) цветность; в) мутность; г) бактериальное число.
|

 а) A + hν В + С;
а) A + hν В + С;
 в) O2 + H2 H2O2;
в) O2 + H2 H2O2;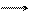
 а) H + O2 HO2;
а) H + O2 HO2;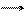
 в) HNO3 + hν NO2 + OH;
в) HNO3 + hν NO2 + OH;
 а) HNO3 H+ + NO3- ;
а) HNO3 H+ + NO3- ; в) HNO3 + NaOH NaNO3 + H2O;
в) HNO3 + NaOH NaNO3 + H2O;


