Орієнтація ПАР на поверхні води.Рис. Типові ізотерми адсорбції для різних температур.
4. Рівняння Фрейндліха та Ленгмюра Аналітично рівняння ізотерми адсорбції описують різні рівняння наприклад емпіричне рівняння Фрейндліха
а –кількість адсорбованого газу р- рівноважний тиск газу k, n – емпіричні константи для адсорбента та газу при певній температурі. Це рівняння застосовується в логарифмічному вигляді:
Воно є рівнянням прямої лінії в графіку який показує залежність
При підвищених концентраціях краще застосовувати рівняння Ленгмюра:
а –кількість адсорбованої речовини р- рівноважний тиск газу k,b – величини постійні для даної ізотерми. Якщо адсорбується не газ, а рідина то замість тиску необхідно підставити концентрацію.
5. Адсорбція на рідких адсорбентах. На відміну від твердих адсорбентів в цьому випадку адсорбція пов’язана зі зміною поверхневого натягу адсорбенту. Всі розчинні речовини по їх властивості до адсорбції можна поділити на поверхнево активні (ПАР) та поверхнево неактивні. Поверхнево активні речовини накопичуються на поверхні рідини-адсорбента та знижують її поверхневий натяг, поверхнево неактивні не накопичуються та не змінюють поверхневого натягу або навідь його дещо підвищують. Поверхнево-активні речовини є в більшості дифільними. Їх молекули містять як полярні (гідрофільні) так і неполярні (гідрофобні) групи. Асиметричність цих молекул орієнтує їх таким чином що гідрофільні групи повернуті до більш полярної фази (як правило це вода), а гідрофобні до менш полярної.
Полярна частина
ВОДА
Орієнтація ПАР на поверхні води.
Залежність між поверхневим натягом та концентрацією адсорбтиву (С) та його адсорбцією в поверхневому шарі (Г) описується рівнянням Гіббса:
З рівняння видно, що з збільшенням концентрації розчинної речовини поверхневий натяг зменшується.
6. Адсорбція на поверхі розділу тверде тіло - рідина. При цьому виникає адгезія. Адгезія – взаємодія між поверхнями конденсованих фаз з виникненням зв’язку між цими поверхнями. Адгезія – це результат прагнення системи до зменшення поверхневої енергії. Когезія – зчеплення частинок речовини усередині однієї фази. Змочування це поверхневе явище, яке полягає у взаємодії рідини з іншою поверхнею: 1. Повне незмочування 2. Повне змочування або розтікання. 3. Неповне змочування. Гідрофільна поверхня та що змочується водою, а гідрофобна не змочується.
На практиці використовують ефект збільшення гідрофільності поверхні (гідрофілізація поверхні) наприклад додаванням ПАР. На цьому явищі основана флотація руд. А також ефект збільшення гідрофобності поверхні (гідрофобізація поверхні).
7. Контрольні питання
|



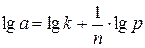
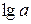 та
та 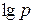 .
.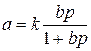
 Неполярна частина молекули
Неполярна частина молекули





