Ленгмюр изотермасыныњ коэффициентініњ физикалыќ маѓынасы ќандай?а) б±л адсорбцияныњ температуралыќ коэффициенті б) б±л адсорбцияныњ максимальді шамасы в) б±л адсорбцияныњ минимальді шамасы г) б±л сорбциялыќ процестердіњ тепе-тењдік константасы 6. Ленгмюр изотермасыныњ тењдеуін кµрсетіњдер: а) 7. Адсорбция деген не? Адсорбция деген: а) бір заттыњ басќа затта жинаќталуы б) бір заттыњ басќа заттыњ кµлемінде жинаќталуы в) бір заттыњ басќа заттыњ бетінде жинаќталуы г) процесс барысында реакция µнімдерініњ жинаќталуы 8. Фрейндлих изотермасыныњ тењдеуін кµрсетіњдер: а)
ГЛОССАРИЙ.
- Беткі керілу деп бос ауданды туғызуға қажет энергияны айтамыз. - Беттік активті заттар деп беткі керілуді тµмендететін заттар аталады. - Беттік – инактивтізаттар деп беттік керілуді жоѓарлататын заттарды айтады. - Адсорбция деп бір заттыњ басќа заттыњ бетінде жинаќталуы аталады. - Абсорбция деп бір заттыњ басќа заттыњ кµлемінде жинаќталуы аталады.
ӘДЕБИЕТТЕР:
1.Жуховицкий А.А., Шварцман А.А. “Физическая химия” 1964,стр.356-389, 1968,стр.289-314. 2.Практикум по физической химии под ред.С.В.Горбачева, 1974,стр.100-103.
№___ Сабаќ Таќырыбы: «ГАЛЬВАНИКАЛЫЌ ЭЛЕМЕНТТІЊ ТЕРМОДИНАМИКАСЫН ЗЕРТТЕУ»
Ж±мыстыњ маќсаты: 1. Температураныњ гальваникалыќ элементіњ ЭЌК – не єсерін зерттеу. 2. Гальваникалыќ элементтердіњ ЭЌК мєліметтері бойынша термодинамикалыќ есептеулерін игеру.
Материалдар жєне жабдыќтар: Термостат, потенциометр, гальваникалыќ элемент, термометр. Ж±мыстыњ мазм±ны жєне орындалу тєртібі:
ТЕОРИЯЛЫЌ Б¤ЛІМ
Химиялыќ энергия электр энергиясына айналу ‰шін белгілі шарттар саќталу керек, яѓни єрекеттесуші заттар мен реакция µнімдері металдыќ µткізгіш арќылы байланысќан екі электродтан жєне электролиттердіњ бір немесе екі жанасатын ерітінділерінен т±ратын гальваникалыќ тізбекті т‰зу керек. Мысалы, келесі реакция
ќалыпты жаѓдайда µтіп, тек жылу бµлінуімен сипатталады. Егер мырыш пластинкасын мырыштыњ к‰кіртќышќыл ерітіндісіне, ал мыс пластинкасын мыстыњ к‰кіртќышќыл ерітіндісіне салып, ерітінділерді бір-бірімен жанастырып, ал мырыш пен мысты металдыќ µткізгішпен байланыстырсаќ, онда гальваникалыќ элемент деп аталатын алынѓан ж‰йеде электр тоѓы пайда болады, яѓни (1) реакцияныњ химиялыќ энергиясы электр энергиясына айналады. 1 грамм-атом мырыштыњ электродтан ерітіндіге µтуі жєне сол уаќытта 1 грамм-атом мыстыњ мыс электродында бµлінуі 2 фарад электр тоѓыныњ жєне ЭЌК –іњ пайда болуымен сипатталады. Сондыќтан, гальваникалыќ элементтіњ жасайтын ж±мысы келесі тењдеуден аныќталуы м‰мкін:
м±нда
Егер ќарастырылатын реакция гальваникалыќ элементте изотермиялыќ жєне ќайтымды µтетін болса, онда осы кезде атќарылатын ж±мыс еркін энергияныњ кемуіне тењ болу керек, яѓни
м±нда
(2) мен (3) аламыз
Басќа жаѓынан еркін энергияныњ µзгерісі химиялыќ туыстыќтыњ тењдеуі бойынша есептелуі м‰мкін:
м±нда
Ќатты мырыш пен мыстыњ активтіліктері 1 тењ болѓандыќтан, онда
(6) тењдеуге (4) -ен
аламыз:
м±нда
Жалпы жаѓдайда, кез-келген гальваникалыќ элементтіњ электрќозѓаушы к‰ші келесі тењдеу бойынша есептеледі:
м±нда
(10) тењдеу электрќозѓаушы к‰штер теорияныњ негізгі тењдеуі - Нернст тењдеуі болып табылады. Ол гальваникалыќ элементтердіњ ЭЌК –і мен потенциалдарыныњ электролит ерітінділерініњ концентрациясына тєуелділігін аныќтайды. Гальваникалыќ элементті µтетін химиялыќ реакцияныњ барысында энтропияныњ µзгеруі (2) тењдеуді температура бойынша дифференциалдау арќылы аныќталады:
м±нда Энтальпия µзгерісі келесідей аныќталады:
Тепе-тењдік константасы
ЭЌК - і µлшеу ‰шін компенсациялыќ єдіс ќолданылады.
ТЄЖІРИБЕЛІК Б¤ЛІМ.
1. Зерттелетін гальваникалыќ элементті жинау керек. 2. Зерттелетін гальваникалыќ элементті температурасы 250С термостатќа 15-20 минутќа орнату керек. 3. 20 минуттан соњ 250С –та потенциометр арќылы гальваникалыќ элементтіњ ЭЌК µлшеу ќажет. 4. Зерттелетін гальваникалыќ элементін 400С (50,60) – та 15 – 20 минутќа термостатќа орнату ќажет. 5. 20 минуттан соњ 400С (50,60) температурасында потенциометрмен гальваникалыќ элементтіњ ЭЌК µлшеу керек. 6. Тєжірибелік мєліметтерді кестеге келтіру керек. 1 кесте.
ТЄЖІРИБЕЛІК МЄЛІМЕТТЕРДІ ¤ЊДЕУ
1. Температура µзгерісін есептеу:
2. Гальваникалыќ элементтіњ ЭЌК –іњ µзгерісін есептеу:
3. Келесі тењдеу бойынша гальваникалыќ элементтіњ ЭЌК-іњ температуралыќ коэффициентін есептеу:
4. (11) тењдеу бойынша энтропия µзгерісін аныќтау; 5. (2) тењдеу бойынша тєжірибелік температураларда Гиббс энергиясыныњ µзгерісін ( 6. (12) тењдеу бойынша тєжірибелік температураларда гальваникалыќ элементтіњ энтальпия µзгерісін ( 7. (13) тењдеуі бойынша тепе-тењдік константасын есептеу. 8. Есептеу мєліметтерін 1 кестеге келтіріњдер.
ЌОРЫТЫНДЫ
1. Тєжірибелік мєліметтерді талдаудан температураныњ гальваникалыќ элементтіњ ЭЌК –не єсерін аныќтау. 2. Термодинамикалыќ есептеулерді талдаудан, гальваникалыќ элементе ќандай процесс µтеді жєне ќандай баѓытта ж‰ретіндігін аныќтау.
Ж±мысты орындаѓан: Ж±мысты ќабылдаѓан: ___________________ ___________________ студенттіњ ќолы оќытушыныњ ќолы, мерзімі
Ж¦МЫСЌА ЖІБЕРІЛУ С¦РАЌТАРЫ
1. Ж±мыстыњ маќсаты ќандай? 2. Гальваникалыќ элемент, ЭЌК деген не? 3. Якобидіњ гальваникалыќ элементінде µтетін химиялыќ процестерді суреттењдер. 4. Энтальпияныњ, энтропияныњ жєне Гиббс энергиясыныњ физикалыќ маѓыналары ќандай? 5. Гальваникалыќ элементтіњ термодинамикасын ќалай есептеуге болады?
БАЌЫЛАУ С¦РАЌТАРЫ
ВАРИАНТ 1.
1. Физикалыќ маѓыналарды атањдар: 1.1. Электрод 1.2. ЭЌК 1.3. Диффузиялыќ потенциал 1.4. Энтальпия 1.5. Ж±мыс 2. I –текті электродтары жєне олардыњ ерекшеліктері. 3. Концентрациялыќ гальваникалыќ элементтер жєне олардыњ ерекшеліктері 4. ЭЌК аныќтаудыњ компенсациялыќ єдісініњ ерекшелігі неде? 5. ЭЌК-іњ электролиттер концентрациясына тєуелділігі ќандай? 3. Ж±мыстаѓы хлок‰міс электродыніњ ролі ќандай? 4. Келесі реакция арќылы ж±мыс жасайтын гальваникалыќ элементтіњ
ЭЌК –і 250С –та 0,2 тењ, ал 850С - 0,226 тењ. Осы гальваникалыќ элементініњ термодинамикасын есептењдер.
ВАРИАНТ 2.
1. Физикалыќ маѓыналарды атањдар: 1.1 Гальваникалыќ элемент 1.2. Стандартты потенциал 1.3. Электродты потенциал 1.4. Энтропия 1.5. Гиббс энергиясы 2. 2 –ші текті электродтар жєне олардыњ ерекшеліктері. 3. Тотыѓу – тотыќсыздану гальваникалыќ элементтер жєне олардыњ ерекшеліктері. 4. ЭЌК тікелей µлшеу єдістерініњ кемшілігі неде? 5. Потенциалдардыњ электролит концентрацияларына тєуелділігі ќандай? 5. Вестон элементініњ ролі ќандай? 6. Келесі реакцияныњ
жылулыќ эффектісі 250С – та 22750 кал/моль тењ. Осы элементтіњ ЭЌК –і температура 100С жоѓарлаѓанда 1,45.10-3 µседі. Элементтіњ 250С –ѓы ЭЌК-ін, энтропиясын жєне Гиббс энергиясын аныќтадар.
БЛИЦ – ТЕСТ 1. Келтірілген сызбалардыњ ќайсысы екінші текті электродты суреттейді? а) б) в) г) 2. Бірінші текті электродтар ‰шін электродтыќ потенциалдыњ ерітінді концентрациясына тєуелділігі ќандай болады? а) б) в) г) 3. 0,01 М FeSO4 ерітіндісінде темірдіњ электродтыќ потенциалы неге тењ? а) - 0,50 в б) + 0,38 в в) + 0,50 в г) -0,38 в 4. Егер а) ия б) жоќ в) білмеймін г) белгілі бір температурада іске асырылады 5. Стандарты жаѓдайда гальваникалыќ элементтіњ а) + 0,10 В б) – 0,10 В в) + 0,78 В г) – 0,78 В 6. а) 135,1 кДж б) 135,1 Дж в) 135,1 кал г) 135,1 ккал 7. а) 221950 Дж б) 164050 Дж в) -221950 Дж г) -164050 Дж
ГЛОССАРИЙ
- Потенциал деп бірлік электр зарядын шексіздіктен электр өрісінің берілген нүктесіне ауыстыру жұмысын айтады. - I текті электродтар - өз тұзының ерітіндісіне батырылған металдан құралған және катиондарға қатысты қайтымды келетін электродтар. - II текті электродтар – электрод металы осы металдыњ нашар еритін т±зымен ќапталѓан жєне аниондары бірдей жаќсы еритін электролит ерітіндісіне батырылѓан электродтар. - Стандартты электродтыќ потенциалдар деп стандарты жаѓдайда потенциаланықтаушы иондардыњ активтілігі бірге тең болѓандаѓы электродтыњ потенциалды айтады. - Гальваникалық элемент деп химиялық реакцияныњ энергиясы электр энергиясына айналатын жүйені айтады. - Электроқозғауыш күш деп бірлік электр зарядының электр өрісініњ бір нүктесінен екіншісіне тасымалдау жұмысын айтады.
ЄДЕБИЕТ
1. А.А.Жуховицкий, Л.А. Шварцман Физическая химия,1964,198-214; 1968, 163-176. 2. Практикум работ по физической химии под ред.С.В.Горбачева, 1974, стр.288-304. 3. Кратний справочник физ.-хим.величин под редакцией Мищенко К.П. М,1974 г. стр.134
№___ Сабаќ Таќырыбы: «ГАЛЬВАНИКАЛЫЌ ЭЛЕМЕНТТЕРДІЊ ЭЛЕКТРЌОЗЃАУШЫ К‡ШТЕРІ ЖЄНЕ ЭЛЕКТРОДТЫЌ ПОТЕНЦИАЛДАРДЫ АНЫЌТАУ»
Ж±мыстыњ маќсаты:
|

 б)
б)  в)
в)  г)
г) 
 б)
б)  в)
в)  г)
г) 

 , (1)
, (1) , (2)
, (2) электр ж±мысы, Дж;
электр ж±мысы, Дж; Фарадей саны, Кл;
Фарадей саны, Кл; элементтіњ электрќозѓаушы к‰ші, В;
элементтіњ электрќозѓаушы к‰ші, В; химиялыќ реакцияныњ элементарлы актісінда ќатысатын электрондар саны.
химиялыќ реакцияныњ элементарлы актісінда ќатысатын электрондар саны. , (3)
, (3) еркін энергияныњ µзгерісі, Дж. моль-1
еркін энергияныњ µзгерісі, Дж. моль-1 (4)
(4) (5)
(5) еркін энергияныњ стандарты µзгерісі, яѓни нормальдік туыстыќ;
еркін энергияныњ стандарты µзгерісі, яѓни нормальдік туыстыќ; реакцияѓа ќатысатын заттардыњ активтіліктері;
реакцияѓа ќатысатын заттардыњ активтіліктері; газ т±раќтысы,
газ т±раќтысы, 
 абсолютті температура.
абсолютті температура. (6)
(6) мєнін ќойып жєне келесіне ќабылдап
мєнін ќойып жєне келесіне ќабылдап (7)
(7) (8)
(8) (9)
(9) стандарты электрќозѓаушы к‰ші.
стандарты электрќозѓаушы к‰ші. (10)
(10) химиялыќ реакцияныњ элементарлы актысында ќатысатын электрондар саны;
химиялыќ реакцияныњ элементарлы актысында ќатысатын электрондар саны;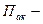 реакция µнімдерініњ активтіліктерініњ кµбейтіндісі;
реакция µнімдерініњ активтіліктерініњ кµбейтіндісі;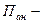 бастапќы заттардыњ активтіліктерініњ кµбейтіндісі.
бастапќы заттардыњ активтіліктерініњ кµбейтіндісі.
 (11)
(11) - гальваникалыќ элементтіњ температуралыќ коэффициенті деп аталады.
- гальваникалыќ элементтіњ температуралыќ коэффициенті деп аталады.
 (12)
(12) мєні бойынша есептеледі:
мєні бойынша есептеледі: (13)
(13)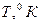

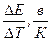







 ) есептеу;
) есептеу;


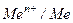

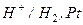




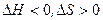 болѓан жаѓдайда гальваникалыќ элементе реакция µтуі м‰мкін ба?
болѓан жаѓдайда гальваникалыќ элементе реакция µтуі м‰мкін ба? ЭЌК неге тењ, егер стандарты потенциалдар
ЭЌК неге тењ, егер стандарты потенциалдар  жєне
жєне 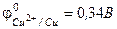
 реакциясыныњ
реакциясыныњ  неге тењ, егер
неге тењ, егер  гальваникалыќ элементтіњ ЭЌК 0,70 В тењ болса?
гальваникалыќ элементтіњ ЭЌК 0,70 В тењ болса? есептењдер, егер
есептењдер, егер 




