
Головна сторінка Випадкова сторінка
КАТЕГОРІЇ:
АвтомобіліБіологіяБудівництвоВідпочинок і туризмГеографіяДім і садЕкологіяЕкономікаЕлектронікаІноземні мовиІнформатикаІншеІсторіяКультураЛітератураМатематикаМедицинаМеталлургіяМеханікаОсвітаОхорона праціПедагогікаПолітикаПравоПсихологіяРелігіяСоціологіяСпортФізикаФілософіяФінансиХімія
Clasificarea cheluielilor publice
Дата добавления: 2015-08-17; просмотров: 823
|
|
Для характеристики реальних систем, що утворюються при взаємодії зрошувальних вод з ґрунтами, виходячи із термодинамічного принципу їх взаємозв’язку запропоновано використовувати спряжене визначення показників активності іонів Н+1, Са+2, Na+1 в зрошувальних водах і рівновеликих ґрунтових розчинах. Виражені через їх від’ємні логарифми (рН, рСа, рNa), названі показники є фізико-хімічними, що відображають відповідно кислотно-лужні (рН), буферні (рСа) і солонцеві (pNa) властивості ґрунтів.
Визначення показників активності іонів рСа і pNa експериментально здійснюють за допомогою іонно-селективних електродів з кальцієвою і натрієвою функціями на універсальному іонометрі ЭВ-74 (в лабораторних умовах) або переносним іонометром И-102 (в польових умовах).
Для оперативного контролю якості зрошувальних вод можна користуватись розрахунковим методом визначення показників активності іонів. При цьому розрахунок коефіцієнтів активності здійснюють за формулою Дебая-Гюккеля, яка дозволяє з певною точністю знаходити коефіцієнти активності іонів в розчинах, іонна сила яких не перевищує 0,06.
Іонну силу розчину m розраховують за формулою
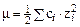 , (1.10)
, (1.10)
де 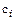 – концентрація і-го іону, моль/л;
– концентрація і-го іону, моль/л;
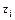 – заряд і-го іону.
– заряд і-го іону.
Для переходу від концентрації іонів в мг/л до моль/л необхідно перевести спочатку в г/л, тобто значення в мг/л розділити на 1000, потім розділити отримані значення на молярну масу. Молярна маса залежить від молекулярної маси хімічних елементів, що входять до даних іонів і не залежить від їх заряду. Отримані значення в моль/л будуть відрізнятьсь від мекв/л для двовалентних іонів (табл. 1.10).
Таблиця 1.10 – Перерахунок концентрації іонів в зрошувальній воді в різні форми (рН=8,2)
| Показник | Аніони | Катіони | Сума | |||||||
| СО3-2 | НСО3-1 | Cl-1 | SO4-2 | Ca+2 | Mg+2 | Na+1 | аніонів | катіонів | іонів | |
| Мг/л | - | |||||||||
| Еквівалентна маса | 35,5 | |||||||||
| Мекв/л | - | 3,00 | 1,49 | 3,75 | 2,75 | 2,25 | 3,24 | 8,24 | 8,24 | |
| %-екв | - | |||||||||
| Молярна маса | 35,5 | |||||||||
| Моль/л | - | 0,0030 | 0,0015 | 0,0019 | 0,0014 | 0,0012 | 0,0032 | 0,044 |
За формулою (1.10) визначаємо іонну силу для отриманих значень
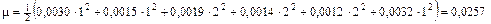 Величину активності іонів кальцію і натрію визначають за формулою
Величину активності іонів кальцію і натрію визначають за формулою
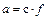 , (1.11)
, (1.11)
де 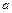 – активність іону, моль/л;
– активність іону, моль/л;
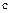 – концентрація іону, моль/л;
– концентрація іону, моль/л;
 – коефіцієнт активності який визначають за табл. 1.11 залежно від
– коефіцієнт активності який визначають за табл. 1.11 залежно від 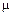 .
.
Для розглянутого прикладу коефіцієнт активності f буде складати:
Ø для одновалентного іону 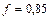 ;
;
Ø для двовалентного іону 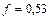 .
.
Тоді величина активності іонів буде:
Ø 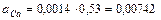 моль/л;
моль/л;
Ø 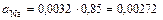 моль/л.
моль/л.
Показники рСа і pNa визначають як від’ємні логарифми від активності іонів за формулами
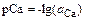 , (1.12)
, (1.12)
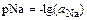 . (1.13)
. (1.13)
Отже, прологарифмувавши величину активності іонів отримуємо рСа=2,13, pNa=2,57 і розраховуємо:
Ø натрієво-кальцієвий потенціал, що характеризує процес осолонцювання –pNa-0,5рCa=2,13-0,5×2,57=0,845;
Ø воднево-натрієвий потенціал, що характеризує процес підлуження – рН-рNа=7,8-2,57=5,23;
Ø відношення потенціалів 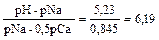 .
.
Таблиця 1.11 – Значення коефіцієнтів активності при різній іонній силі
| Іонна сила m | Коефіцієнт активності f | |
| одновалентний іони | двовалентний іони | |
| 0,001 0,002 0,003 0,004 0,005 0,006 0,007 0,008 0,009 0,010 | 0,96 0,95 0,95 0,93 0,92 0,92 0,92 0,91 0,90 0,89 | 0,86 0,79 0,74 0,73 0,72 0,69 0,67 0,66 0,64 0,63 |
| 0,015 0,020 0,025 0,030 0,035 0,040 0,045 0,050 0,055 0,060 | 0,88 0,87 0,85 0,84 0,83 0,83 0,82 0,81 0,80 0,80 | 0,59 0,55 0,53 0,50 0,49 0,47 0,45 0,44 0,42 0,40 |
Оцінювання зрошувальної води за термодинамічними показниками здійснюють за табл. 1.112 (ДСТУ 2730-94).
Таблиця 1.12 – Оцінювання якості зрошувальної води за термодинамічними показниками
| Буферність ґрунту | Термодинамічні потенціали зрошувальної води | Клас якості води | ||
| рNa-0,5pCa | pH-pNa | pH-pNa_ pNa-0,5pCa | ||
| Низька Середня Висока | Більше 1,35 Більше 1,25 Більше 1,20 | 3,0-4,0 3,0-4,5 3,0-5,0 | Менше 3,0 Менше 3,6 Менше 4,2 | І |
| Низька Середня Висока | 1,35-0,65 1,25-0,55 1,20-0,50 | 4,0-5,0 4,5-6,0 5,0-7,0 | 3,0-7,0 3,6-11,0 4,2-14,0 | ІІ |
Для розглянутого прикладу – середня буферність ґрунту (див. п. 1. 5), тоді за всіма потенціалами і їх відношенням якість зрошувальної води необхідно віднести до ІІ класу, тобто „Обмежено придатна для зрошення”. При використанні такої води необхідно застосовувати комплекс заходів для попередження деградації ґрунтів.
| <== предыдущая лекция | | | следующая лекция ==> |
| Conţinutul economic al cheltuielior publice | | | Nivelul, structura şi dinamica cheltuielilor |