
Головна сторінка Випадкова сторінка
КАТЕГОРІЇ:
АвтомобіліБіологіяБудівництвоВідпочинок і туризмГеографіяДім і садЕкологіяЕкономікаЕлектронікаІноземні мовиІнформатикаІншеІсторіяКультураЛітератураМатематикаМедицинаМеталлургіяМеханікаОсвітаОхорона праціПедагогікаПолітикаПравоПсихологіяРелігіяСоціологіяСпортФізикаФілософіяФінансиХімія
Р А П О Р Т
Дата добавления: 2015-08-27; просмотров: 719
|
|
1. Определить молярные доли изопропанола в исходной смеси xF и в кубовом остатке xW.
Для этого по данным, представленным в таблице равновесных составов (см. с. 56), построить график зависимости состава жидкости от температуры кипения (для интервала 100,0… tF, °С) и, используя значения зафиксированных температур tF и tW, определить искомые концентрации.
2. Определить экспериментальное значение молярной доли изопропанола в дистилляте xD, эксп.
Для этого использовать измеренное значение показателя преломления дистиллята. Молярная доля х [в (моль С3Н8О)/(моль раствора)] и показатель преломления[3] r водного раствора изопропилового спирта связаны соотношением:
| х = ехр (71,8504×r − 99,7753) . | (3.1.6) |
3. Определить количества исходной смеси nF и дистиллята nD, эксп по формуле (3.1.4).
Для этого использовать зафиксированные значения объёмов исходной смеси VF и дистиллята VD.
Плотность r (в кг/м3) водного раствора изопропилового спирта при комнатной температуре может быть рассчитана по формуле:
| r = (1,0064×10−3 + 3,827×10−4×х)−1. | (3.1.7) |
При расчёте по (3.1.5) молярной массы исследуемой системы рекомендуется считать компонентом А изопропиловый спирт, имеющий молярную массу  , а компонентом В — воду, молярная масса которой
, а компонентом В — воду, молярная масса которой  .
.
4. Рассчитать теоретическую концентрацию изопропанола в дистилляте xD, расч.
Полагая известными 3 параметра (xF, xW и nF) и решая систему уравнений (3.1.1)…(3.1.3) относительно xD, получают формулу для расчёта искомой концентрации:
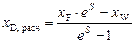 , ,
| (3.1.8) |
где 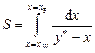 .
.
Для определения интеграла S рекомендуется предварительно вычислить значения интегрируемой функции f = (у* − х)−1 при различных значениях х, используя данные таблицы равновесных составов (см. с. 56). Значения у* при x = xW и x = xF могут быть найдены линейной интерполяцией по известным ближайшим табличным величинам у*. Величины х2…х k − 1 рекомендуется принять тождественными табличным. Подготовленную числовую информацию внести в таблицу:
| № п/п | х·102, моль моль | у*·102, моль моль | (х − у*)·102, моль моль | f |
| [xW] | ||||
| … | ||||
| k − 2 | ||||
| k − 1 | ||||
| k | [xF] |
Величина интеграла S, то есть площадь, ограниченная осью абсцисс, ординатами, проходящими через точки х = xW и х = xF, и кривой функции f, может быть определена по одной из квадратурных формул. Здесь рекомендуется применить формулу трапеций:
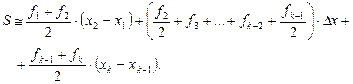
| (3.1.9) |
При начальной концентрации раствора не более 0,04 моль/моль рекомендуется принять Dх = 0,002 моль/моль соответственно шагу изменения концентрации (в интервале х = 0,0…0,04 моль/моль) в указанной таблице. При xF > 0,04 моль/моль рекомендуется принять Dх = 0,005 моль/моль.
5. Рассчитать теоретическое количество получаемого дистиллята nD, расч.
Решая систему уравнений (3.1.1)…(3.1.3) относительно пD, получают формулу для расчёта искомой величины:
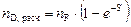 . .
| (3.1.10) |
Измеренные и рассчитанные параметры рекомендуется занести в таблицу:
| № | Исходная смесь | Остаток | |||||||
| VF, л | tF, °С | xF, моль моль | rF, кг м3 | MF, г_ моль | nF, моль | tW, °С | xW моль моль | ||
| Дистиллят | ||||||||
| VD, л | r | xD, эксп моль моль | rD, кг м3 | MD, г_ моль | nD, эксп моль | xD, расч моль моль | nD, расч моль | |
Проанализировать значения количества и качества (состава) дистиллята, полученные экспериментально и рассчитанные теоретически, и сделать выводы по работе.
| <== предыдущая лекция | | | следующая лекция ==> |
| ПРОТОКОЛ | | | ПРОТОКОЛ |