Предельные подвижности ионов
(См∙ см∙ моль-1) при 25º С
| Катион
| 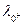
| Анион
| 
| | Н+
| 349, 8
| OH-
| 198, 0
| | К+
| 73, 5
| I-
| 76, 8
| | Na+
| 50, 1
| Br-
| 78, 4
| | Li+
| 38, 7
| Cl-
| 76, 3
| | Ag+
| 61, 9
| NO 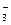
| 71, 4
| | Ba2+
| 127, 2
| CH3COO-
| 40, 9
| | Ca2+
| 119, 0
| SO 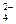
| 160, 0
| | Mg2+
| 106, 1
| [Fe(CN)6]3-
| 297, 0
| | Al3+
| 189, 0
| [Fe(CN)6]4-
| 444, 0
| | Fe3+
| 204, 0
|
|
| Таблица 6
Стандартные электродные потенциалы при Т=298 К
| Электрод
| Электродная реакция
| Е0, В
| | Li+/Li
| Li+ + e ↔ Li
| -3, 045
| | Rb+/Rb
| Rb+ + e ↔ Rb
| -2, 925
| | K+/K
| K+ + e ↔ K
| -2, 925
| | Cs+/Cs
| Cs+ + e ↔ Cs
| -2, 923
| | Ba2+/Ba
| Ba2+ + 2e ↔ Ba
| -2, 906
| | Ca2+/Ca
| Ca2+ + 2e ↔ Ca
| -2, 866
| | Na+/Na
| Na+ + e ↔ Na
| -2, 714
| | La3+/La
| La3+ + 3e ↔ La
| -2, 522
| | Mg2+/Mg
| Mg2+ + 2e ↔ Mg
| -2, 363
| | Be2+/Be
| Be2+ + 2e ↔ Be
| -1, 847
| | Al3+/Al
| Al3+ + 3e ↔ Al
| -1, 662
| | Ti2+/Ti
| Ti2+ + 2e ↔ Ti
| -1, 628
| | V2+/V
| V2+ + 2e ↔ V
| -1, 186
| | Mn2+/Mn
| Mn2+ + 2e ↔ Mn
| -1, 180
| | Sm3+/Sm2+
| Sm3+ + e ↔ Sm2+
| -1, 150
| | Cr2+/Cr
| Cr2+ + 2e ↔ Cr
| -0, 913
| | Zn2+/Zn
| Zn2+ + 2e ↔ Zn
| -0, 763
| | Cr3+/Cr
| Cr3+ + 3e ↔ Cr
| -0, 744
| | In3+/In2+
| In3+ + e ↔ In2+
| -0, 450
| | Fe2+/Fe
| Fe2+ + 2e ↔ Fe
| -0, 440
| | Cr3+/Cr2+
| Cr3+ + e ↔ Cr2+
| -0, 408
| | Cd2+/Cd
| Cd2+ + 2e ↔ Cd
| -0, 403
| | Ti3+/Ti2+
| Ti3+ + e ↔ Ti2+
| -0, 368
| | Co2+/Co
| Co2+ + 2e ↔ Co
| -0, 277
| | V3+/V2+
| V3+ + e ↔ V2+
| -0, 256
| | Ni2+/Ni
| Ni2+ + 2е ↔ Ni
| -0, 250
| | Sn2+/Sn
| Sn2+ + 2е ↔ Sn
| -0, 136
| | Pb2+/Pb
| Pb2+ + 2е ↔ Pb
| -0, 126
| | Fe3+/Fe
| Fe3+ + 3е ↔ Fe
| -0, 036
| | H+/H2
| H+ + е ↔ ½ H2
| 0, 000
| | Sn4+/Sn2+
| Sn4+ + 2е ↔ Sn2+
| +0, 150
| | Cu2+/Cu+
| Cu2+ + е ↔ Cu+
| +0, 153
| SO 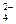 /H2S /H2S
| SO 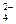 + 10Н+ + 8е ↔ H2S(водн) + 4Н2О + 10Н+ + 8е ↔ H2S(водн) + 4Н2О
| +0, 303
| | Cu2+/Cu
| Cu2+ + 2е ↔ Cu
| +0, 337
| | O2/OH-
| ½ O2 + Н2О + 2е ↔ OH-
| +0, 401
| | Cu+/Cu
| Cu+ + е ↔ Cu
| +0, 521
| | I2/I-
| I2 + 2е ↔ I-
| +0, 536
| | Fe3+/Fe2+
| Fe3+ + е ↔ Fe2+
| +0, 771
| | Ag+/Ag
| Ag+ + е ↔ Ag
| +0, 799
| | Hg2+/Hg
| Hg2+ + 2е ↔ Hg
| +0, 854
| 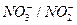
| 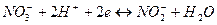
| +0, 940
| | Pd2+/Pd
| Pd2+ + 2е ↔ Pd
| +0, 987
| | Br2/Br-
| ½ Br2 + е ↔ Br-
| +1, 065
| 
| 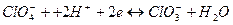
| +1, 190
| | Pt2+/Pt
| Pt2+ + 2е ↔ Pt
| +1, 200
| | Ti3+/Ti+
| Ti3+ + 2е ↔ Ti+
| +1, 250
|  Cr2O Cr2O 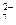 /Cr3+ /Cr3+
|  Cr2O Cr2O 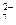 + 14Н+ + 6е ↔ Cr3+ + 7Н2О + 14Н+ + 6е ↔ Cr3+ + 7Н2О
| +1, 330
| | Cl2/Cl-
| ½ Cl2 + е ↔ Cl-
| +1, 359
| | PbO2/Pb2+
| PbO2 + 14Н+ + 2е ↔ Pb2+ + 2Н2О
| +1, 455
| | Au3+/Au
| Au3+ + 3е ↔ Au
| +1, 498
| MnO 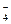 /Mn2+ /Mn2+
| MnO 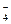 + 8Н+ + 5е ↔ Mn2+ + 4Н2О + 8Н+ + 5е ↔ Mn2+ + 4Н2О
| +1, 510
| | HClO2/HClO
| HClO2 + 2Н+ + 2е ↔ HClO + 2Н2О
| +1, 640
| | PbO2/PbSO4
| PbO2 + 4Н+ + SO 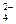 +2е ↔ PbSO4 + 2Н2О +2е ↔ PbSO4 + 2Н2О
| +1, 685
| | H2O2/H2O
| H2O2 + 2Н+ + 2е ↔ 2H2O
| +1, 776
| | Co3+/Co2+
| Co3+ + е ↔ Co2+
| +1, 810
| S2O 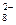 /SO /SO 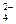
| S2O 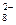 + 2е ↔ 2SO + 2е ↔ 2SO 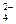
| +2, 010
| | H2/H-
| ½ H2 + е ↔ H-
| +2, 200
| | F2/F-
| ½ F2 + е ↔ F-
| +2, 866
|

Практические расчеты на срез и смятие При изучении темы обратите внимание на основные расчетные предпосылки и условности расчета...
|

Функция спроса населения на данный товар Функция спроса населения на данный товар: Qd=7-Р. Функция предложения: Qs= -5+2Р,где...
|

Аальтернативная стоимость. Кривая производственных возможностей В экономике Буридании есть 100 ед. труда с производительностью 4 м ткани или 2 кг мяса...
|

Вычисление основной дактилоскопической формулы Вычислением основной дактоформулы обычно занимается следователь. Для этого все десять пальцев разбиваются на пять пар...
|
|
Ситуация 26. ПРОВЕРЕНО МИНЗДРАВОМ
Станислав Свердлов закончил российско-американский факультет менеджмента Томского государственного университета...
Различия в философии античности, средневековья и Возрождения ♦Венцом античной философии было: Единое Благо, Мировой Ум, Мировая Душа, Космос...
Характерные черты немецкой классической философии 1. Особое понимание роли философии в истории человечества, в развитии мировой культуры. Классические немецкие философы полагали, что философия призвана быть критической совестью культуры, «душой» культуры.
2. Исследовались не только человеческая...
|
|
ОЧАГОВЫЕ ТЕНИ В ЛЕГКОМ Очаговыми легочными инфильтратами проявляют себя различные по этиологии заболевания, в основе которых лежит бронхо-нодулярный процесс, который при рентгенологическом исследовании дает очагового характера тень, размерами не более 1 см в диаметре...
Примеры решения типовых задач. Пример 1.Степень диссоциации уксусной кислоты в 0,1 М растворе равна 1,32∙10-2
Пример 1.Степень диссоциации уксусной кислоты в 0,1 М растворе равна 1,32∙10-2. Найдите константу диссоциации кислоты и значение рК.
Решение. Подставим данные задачи в уравнение закона разбавления
К = a2См/(1 –a) =...
Экспертная оценка как метод психологического исследования Экспертная оценка – диагностический метод измерения, с помощью которого качественные особенности психических явлений получают свое числовое выражение в форме количественных оценок...
|
|