Классы ферментовОксидоредуктазы. Трансферазы (феразы). Гидролазы. Лиазы (десмолазы). Изомеразы и мутазы. Лигазы (синтетазы).
1. Оксидоредуктазы Оксидоредуктазы – ферменты, катализирующие окислительно-восстановительные реакции с участием двух субстратов. Sвосст. + S¢ окисл. = Sокисл + S¢ восст. Ферменты катализируют реакции, в которых участвуют такие группы, как СН-ОН, СН-СН, С=О, СН-NН2, -СН-NН-. Примеры оксидоредуктаз: 1. Ферменты дыхательной цепи – цитохромы. 2. Каталаза – фермент, катализирующий расщепление Н2О2; предохраняет организм от вредного воздействия Н2О2. 3. Пероксидаза – фермент, ускоряющий окисление Н2О и О2 до Н2О2. 4. К оксидоредуктазам относятся дегидрогеназы – ферменты, отнимающие водород от одних органических веществ и передающие другим органическим соединениям (анаэробные дегидрогеназы) или О2 воздуха (аэробные дегидрогеназы). Анаэробные дегидрогеназы содержат коферменты НАД (козимаза), НАДФ, аэробные – ФАД. В клетке окислительные процессы происходят по нескольким механизмам: 1. Окисление по типу отнятия электронов:
2. Окисление по типу отнятия водорода: -2Н
3. Окисление путем присоединения к субстрату кислорода:
Оксидоредуктазы подразделяют на дегидрогеназы, оксидазы, оксигеназы. Кроме того, в митохондриях клеток содержится группа ферментов – промежуточных переносчиков электронов дыхательной цепи. Дегидрогеназы – оксидоредуктазы, которые окисляют субстрат путем отнятия водорода. Оксигеназы – ферменты, осуществляющие включение одного (оксигеназы) или двух (диоксигеназы) атомов кислорода в молекулу субстрата. Оксидазы – ферменты, осуществляющие окисление путем передачи восстановительного эквивалента от субстрата, либо на молекулярный кислород, либо на кислород пероксида водорода или органических перекисей. К оксидазам относятся пероксидазы и полифенолоксидазы. Пероксидазы – ферменты, окисляющие субстрат при помощи пероксида водорода:
где АН2, А – восстановленный и окисленный субстраты соответственно. Субстратами пероксидаз служат фенолы и ароматические соединения. Пероксидазы – железосодержащие ферменты, гемом которых является феррипротопорфирин IX. Окисление субстратов осуществляется по одноэлектронному механизму. Первой стадией каталитического процесса является образование комплекса между железом фермента и пероксидом водорода. Следовательно, окисление субстрата осуществляется пероксидом водорода, который активирован ферментом.
Е-Н2О + Н2О2 ® Е-Н2О2 + Н2О соединение 1
Е-Н2О2 + АН2 ® соединение 2 + АН·
соединение 2 + АН· ® Е-Н2О + А
Пероксидазы широко распространены в растительных тканях. Они находятся в клеточной стенке и пероксисомах. Известно более 20 изоформ пероксидаз с различной активностью. Роль пероксидаз в биохимии и физиологии растений окончательно не выяснена. Пероксидазы наряду с каталазой препятствуют накоплению пероксида водорода в клетке. Пероксидазы выполняют защитную функцию, играют важную роль в онтогенезе растений при патогенезе, противостоянии стрессу, повреждениях. Пероксидазы участвуют в нейтрализации продуктов вторичного обмена (фенолов), в регуляции гормонального статуса растений через окисление индолилуксусной кислоты, образование этилена из метионина, участвуют в процессах синтеза лигнина в клеточной стенке. Образованные в пероксидазных реакциях активные формы кислорода могут использоваться растениями в защите от патогена. Пероксидазы могут разрушать комплексы, содержащие радионуклеиды, препятствовать их накоплению, это чрезвычайно важно с позиции экологии Севера. Анализ ферментативной активности пероксидаз проводится фотоколориметрическим методом при длине волны 440 нм, рабочей длине кюветы – 2 см. Определение активности пероксидазы основано на образовании красно-коричневых окрашенных продуктов при окислении фенола, бензидина, гваякола, катехола и других фенольных соединений. Общая схема реакции:
красно-корич- невая окраска
Полифенолоксидаза – оксидоредуктаза, катализирующая окисление полифенолов. Определение активности полифенолоксидазы проводится фотоколориметрическим методом при длине волны 590 нм, рабочей длине кюветы 2 см при воздействии на систему пирокатехин-р-фенилендиамин. Реакция протекает следующим образом:
-2Н +1/2О2
о-хинон
NH2 NH
О-хинон р-фенилендиамин коричневый пирокахетин окрашенный продукт
Полифенолоксидаза содержится в высших растениях и в грибах. Массовая доля меди в данном ферменте составляет 0, 2-0, 3 %. Например, ее молекулярная масса у грибов равна 34500, а у чайного листа – 144000. Полифенолоксидаза участвует в окислении полифенолов и дубильных веществ, ее действием объясняется потемнение плодов и овощей при сушке, потемнение поверхности разрезанных яблок или картофельного клубня. Каталаза Каталаза относится к классу оксидоредуктаз. Биологическая роль каталазы состоит в том, что каталаза разрушает токсичную для животных и растительных клеток Н2О2. Н2О2 накапливается как рабочий продукт метаболизма. каталаза
Каталаза – двухкомпонентный фермент, состоящий из белка и простетической группы, которая содержит гематин и связывается с белком двумя карбоксилами. Каталаза локализуется в пероксисомах. Каталаза – быстродействующий фермент. При 00С одна молекула каталазы разлагает до 40000 молекул в секунду. Каталаза ингибируется синильной кислотой.
2. Трансферазы Трансферазы – ферменты, катализирующие перенос группы от субстрата S на субстрат S¢ :
S – G + S¢ ® S¢ - G + S Ацилтрансферазы – ферменты, переносящие ацильные группы R-СО- (например, ацетил СН3СО-). Ацетил-СоА + холин ® СоА + О-ацетилхолин Алкилтрансферазы – ферменты, переносящие алкильные группы (метилтрансферазы переносят СН3-, метил). Фосфотрансферазы – ферменты, преносящие группы, содержащие фосфор. Гликозилтрансферазы (2.4) – ферменты, катализирующие перенос остатков моносахаридов. К гликозилтрансферазам относятся фосфорилазы. Представителем фосфорилаз является крахмальная фосфорилаза (a-глюканфосфорилаза, 2.4.1.1).
3. Гидролазы Гидролазы – ферменты, катализирующие процессы гидролиза (гидролиз эфирных, сложноэфирных, пептидных и гликозильных связей, кислотных ангидридов, связей С-С, С-галоида, Р-N. Гидролазы подразделяются на эстеразы, карбогидразы, протеазы, амидазы, дезаминазы, фосфорилазы. Эстеразы – ферменты, катализирующие реакции расщепления и синтеза сложных эфиров. эстеразы
К эстеразам относятся липазы, танназы, хлорофиллазы, пектинэстеразы (пектазы), фосфатазы, сульфатазы. Липазы – эстеразы, катализирующие гидролиз и синтез жиров. СН2-О-СО-R1 СН2-ОН | |
| | СН2-О-СО- R3 СН2-ОН
Липазы имеют шифр 3.1.1.3. Танназа – фермент, катализирующий гидролиз таннин (сложного эфира). Хлорофиллаза – эстераза, катализирующая переэтерификацию хлорофилла. Фосфатазы ускоряют расщепление и синтез сложных эфиров, образованных спиртами и фосфорной кислотой. Фофатазы подразделяются на фосфатазы неспецифического и специфического действия. Неспецифические фосфатазы катализируют отщепление Н3РО4 от фосфорных эфиров, для них характерен широкий диапазон рН (4, 5-9, 0). К данным фосфатазам относятся рибонуклеаза и дезоксирибонуклеаза, катализирующие распад рибонуклеиновой и дезоксирибонуклеиновой кислот. Специфические фосфатазы действуют на фосфорные эфиры определенного состава. К ним относится фруктозодифосфатаза, действующая только на фруктозодифосфорную кислоту. Сульфатазы катализируют гидролиз и синтез сложных эфиров серной кислоты. Карбогидразы – ферменты, катализирующие гидролиз и синтез гликозидов, ди-, три- и полисахаридов. Карбогидразы подразделяются на олигазы и полиазы. К олигазам относятся a-глюкозидаза, b-глюкозидаза, a-галактозидаза, b-галактозидаза, b-фруктофуранозидаза. a-Глюкозидаза, мальтаза – фермент, расщепляющий a-глюкозидную связь в дисахаридах и глюкозидах. Биологическим субстратом для данного фермента являются мальтоза и сахароза. Содержится в тканях растений, в плесневых грибах, дрожжах, бактериях, в проросшем просяном зерне. Просяной солод применяют как добавку к ячменному солоду при изготовлении мальтозной патоки, так как он богат активной мальтазой. b-Глюкозидаза – фермент, расщепляющий b-глюкозидную связь в ди- и полисахаридах, b-глюкозидах (целлобиоза, пентибиоза, глюкозиды – амигдалин, арбутин). a-Галактозидаза – фермент, катализирующий гидролиз a-галактозидов, например, рафинозы и мелибиозы. a-Галактозидаза содержится в пивных дрожжах и в грибном солоде – такадиастазе (ферментном препарате, полученном из плесневых грибов. b-Галактозидаза (3.2.1.23), или лактаза – фермент, катализирующий гидролиз лактозы на глюкозу и галактозу. b-Галактозидаза (лактаза) содержится в бактериях, плесневых грибах, плодах миндаля, в молочных железах животного организма, в лактозных дрожжах. b-фруктофуранозидаза (3.2.1.26), сахараза, инвертаза – фермент, катализирующий расщепление сахарозы на глюкозу и фруктозу. a-Глюкозидаза гидролизует сахарозу у a-глюкозидного С-атома остатка глюкозы, а b-фруктофуранозидаза гидролизует связь у b-глюкозидного С-атома остатка фруктозы. b- фруктофуранозидаза (сахараза) катализирует также гидролизирует рафинозы (триозы) с образованием молекулы фруктозы и молекулы дисахарида мелибиозы.
|

 An+ электроны Am+
An+ электроны Am+ А1 А2
А1 А2  А1 +О2 А2
А1 +О2 А2 Н2О2 + АН2 А + 2 Н2О2,
Н2О2 + АН2 А + 2 Н2О2, Фенол + Н2О2 пероксидаза Хинон + Н2О
Фенол + Н2О2 пероксидаза Хинон + Н2О

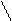


 ОН ОН О О
ОН ОН О О

 полифенолоксидаза
полифенолоксидаза


 + Н2О
+ Н2О










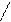
 + +
+ +

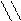
 2 Н2О2 2 Н2О + О2
2 Н2О2 2 Н2О + О2
 R-СО-О-R1 + Н2О R-СООН +R1 ОН
R-СО-О-R1 + Н2О R-СООН +R1 ОН СН- О-СО- R2 + 3 Н2О липаза СН-ОН + R1 СООН+ R2СООН +R3СООН
СН- О-СО- R2 + 3 Н2О липаза СН-ОН + R1 СООН+ R2СООН +R3СООН


