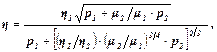Внутрішнє тертя у газахЯвище внутрішнього тертя пов’язано з виникненням сил тертя між шарами газу або рідини, що переміщуються паралельно один до одного з різними за величиною швидкостями. З боку шару, що рухається швидше, на шар, який рухається повільніше, діє прискорювальна сила. Навпаки, шар, що повільно рухається, гальмує шари газу, які рухаються швидше. Сили тертя, які при цьому виникають, напрямлені вздовж дотичної до поверхні зіткнення шарів. З погляду кінетичної теорії газів причиною внутрішнього тертя є накладання впорядкованого руху шарів газу з різними швидкостями на хаотичний тепловий рух молекул, інтенсивність якого залежить від температури. Завдяки тепловому руху молекули переходять з шару, що рухається з швидкістю Якщо різниця швидкостей руху різних шарів газу зовнішніми силами підтримується сталою, то і потік імпульсу від шару до шару буде сталим (стаціонарним), причому цей потік буде спрямований уздовж спадання швидкості. З таким випадком зустрічаємось при повільній течії газу (або рідини) між двома пластинами або у трубі під впливом сталої зовнішньої різниці тисків, спрямованої вздовж руху. Коли газ тече вздовж труби, то швидкості різних шарів розподілені так, як показано на рис. 79. Найбільша швидкість спостерігається в середній частині труби, що прилягає до осі, у міру наближення до стінок швидкість зменшу Кількісно перенесення імпульсу можна описати так само, як перенесення енергії у процесі теплопровідності. Розглянемо площадку S, паралельну швидкості течії газу і перпендикулярну до осі OX (рис. 80). Нехай
Молекули праворуч від S заміщуються іншими молекулами, які надійшли зліва і мають більший імпульс. У разі зіткнення цих молекул з молекулами, що були до цього праворуч від S, більша швидкість течії розподілиться між усіма молекулами праворуч, після чого швидкість течії цього шару, а, отже, й імпульс стануть більшими. Водночас швидкість й імпульс шару газу, який знаходиться ліворуч від S, зменшується. Отже, обмін молекулами, зумовлений тепловими рухами, приводить до вирівнювання швидкостей течії різних шарів газу. Таким є механізм перенесення імпульсу в напрямку осі OX від одного шару газу, який тече, до другого. Величина потоку імпульсу P, який переноситься за одиницю часу через одиницю площі площадки S, визначається різницею імпульсів Зліва направо рухатиметься кількість молекул, яка дорівнює
а справа наліво
Припускаємо, що всі молекули рухаються з однаковою тепловою швидкістю Молекули, які рухаються зліва направо, переносять імпульс
Відповідно, молекули, які рухаються справа наліво, переносять імпульс
Повна зміна імпульсу молекул
Якщо градієнт швидкості
поблизу площадки S, то
оскільки
де
або
Це рівняння внутрішнього тертя, або закон Ньютона. Сила внутрішнього тертя, що виникає у площині дотику двох шарів газу, що ковзають один відносно одного, пропорційна до площі їх дотику S і градієнта швидкості Коефіцієнт пропорційності
Приймаючи Внаслідок пропорційності Поряд з динамічною в’язкістю Між коефіцієнтами перенесення існують такі співвідношення:
Наявність цього зв’язку між коефіцієнтами процесів перенесення обумовлена однаковістю фізичної природи процесів перенесення і тим, що всі вони описуються однаковими рівняннями. ПУЛЮЙ ІВАН ПАВЛОВИЧ (1845-1918) Виміряв в 1877 р. коефіцієнти дифузії парів через пористі перегородки (стінки глиняних посудин) та їх температурні залежності. З дослідів з водяною парою, з парою ефіру, хлороформу, алкоголю зробив висновок, що пара дифундує крізь пористі стінки у відношенні, оберненому до квадратних коренів їх густин. Виконав вперше в 1874 р. найбільш систематичніше дослідження коефіцієнта внутрішнього тертя для різних газів. Досліджував повітря, вуглекислий газ, водень, пари води, спирту, бензолу, ацетону, ефіру. Показав, що з підвищенням температури η зростає за законом η=η0(1+αt)n, 2/3<n<3/4. Довів, що значення коефіцієнта в’язкості суміші газів, які хімічно не взаємодіють між собою, лежить між значеннями коефіцієнтів внутрішнього тертя компонент. Визначив експериментально, що гази з більшою молекулярною вагою мають за рівних кількостей більший вплив на коефіцієнт внутрішнього тертя суміші газів. Одержав для коефіцієнта внутрішнього тертя співвідношення
де p1, p2 – парціальні тиски, μ1, μ2 – молекулярні маси, η1, η2 – коефіцієнти внутрішнього тертя компонент.
|

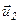 у шар, який рухається з швидкістю
у шар, який рухається з швидкістю  . При цьому молекули переносять імпульс
. При цьому молекули переносять імпульс 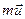 свого впорядкованого руху.
свого впорядкованого руху.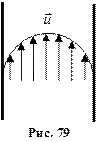 ється, а шар, що безпосередньо прилягає до стінок труби, перебуває у спокої. При такій течії імпульс переноситься від центрального шару, де швидкість найбільша, до шарів, які рухаються з меншою швидкістю. Через те, що цей процес пов’язаний зі зміною кількості руху, то газ поводить себе так, як коли б на нього діяла якась сила (сила внутрішнього тертя).
ється, а шар, що безпосередньо прилягає до стінок труби, перебуває у спокої. При такій течії імпульс переноситься від центрального шару, де швидкість найбільша, до шарів, які рухаються з меншою швидкістю. Через те, що цей процес пов’язаний зі зміною кількості руху, то газ поводить себе так, як коли б на нього діяла якась сила (сила внутрішнього тертя). . Завдяки обміну молекулами між обома шарами газу (обмін відбувається завдяки тепловим рухам) ця різниця зменшується.
. Завдяки обміну молекулами між обома шарами газу (обмін відбувається завдяки тепловим рухам) ця різниця зменшується.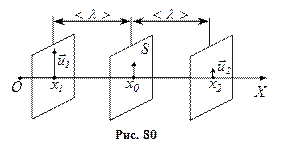
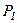 і
і 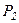 , які переносяться молекулами, що перетинають площадку S зліва і справа відповідно.
, які переносяться молекулами, що перетинають площадку S зліва і справа відповідно.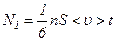 ,
,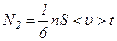 .
.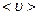 .Через площадку S протікатимуть лише ті молекули, які перебувають на відстані
.Через площадку S протікатимуть лише ті молекули, які перебувають на відстані 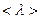 . Молекули, завдяки наявності в них теплової швидкості
. Молекули, завдяки наявності в них теплової швидкості 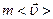 . Цей імпульс не розглядається. А мова йде про той імпульс
. Цей імпульс не розглядається. А мова йде про той імпульс 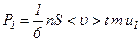 .
.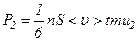 .
.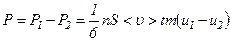 .
.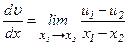
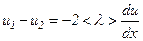 ,
,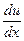 – зміна швидкості на одиницю довжини. Знак „–” показує, що зростанню x відповідає спадання u. Звідси
– зміна швидкості на одиницю довжини. Знак „–” показує, що зростанню x відповідає спадання u. Звідси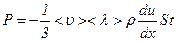 ,
,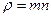 . Оскільки зміна імпульсу дорівнює імпульсу діючої сили, то
. Оскільки зміна імпульсу дорівнює імпульсу діючої сили, то 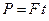 , де
, де 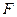 – сила взаємодії між шарами газу, що діє у поверхні їх дотику:
– сила взаємодії між шарами газу, що діє у поверхні їх дотику: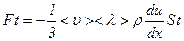 ,
,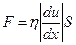 .
.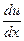 .
.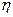 називається коефіцієнтом внутрішнього тертя або динамічною в’язкістю:
називається коефіцієнтом внутрішнього тертя або динамічною в’язкістю: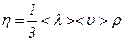 .
.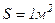 ,
, 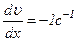 , маємо
, маємо 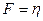 , тобто коефіцієнт в’язкості числово дорівнює силі внутрішнього тертя, що діє на
, тобто коефіцієнт в’язкості числово дорівнює силі внутрішнього тертя, що діє на  поверхні дотику шарів газу, що рухається паралельно при градієнті швидкості
поверхні дотику шарів газу, що рухається паралельно при градієнті швидкості 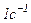 ,
, 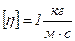 .
.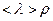 виходить, що, як і
виходить, що, як і 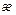 , коефіцієнт внутрішнього тертя не залежить від тиску, за винятком сильно розрідженого газу, коли середня довжина вільного пробігу молекул стає більшою від розмірів посудини.
, коефіцієнт внутрішнього тертя не залежить від тиску, за винятком сильно розрідженого газу, коли середня довжина вільного пробігу молекул стає більшою від розмірів посудини.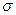 , яка визначається як динамічна в’язкість, поділена на густину:
, яка визначається як динамічна в’язкість, поділена на густину: 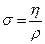 .
.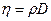 ,
, 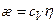 ,
, 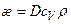 .
.