Цель
Получение Нитрата меди (II).
| Нитрат меди(II)
|
|
| Систематическое название
| Нитрат меди(II)
|
| Другие названия
| Медь азотнокислая
|
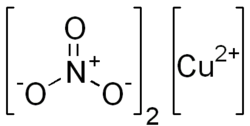
| Химическая формула
| Cu(NO3)2
|
| Внешний вид
| Бесцветные кристаллы (безводный) Голубые кристаллы (кристаллогидраты)
|
| Свойства
|
| Молярная масса
| безводный: 187,55 г/моль; тригидрат: 241,60 г/моль; гексагидрат: 295,64 г/моль
|
| Температура плавления
| безводный: 255 °C[1]; тригидрат: 114,5 °C; гексагидрат: 24,4 °C
|
| Температура разложения
| безводный: 170 °C
|
| Плотность
| безводный: 3,05 г/см³; тригидрат: 2,32 г/см³; гегсагидрат: 2,074 г/см³
|
| Растворимость в воде
| 124,7 г/100 мл
|
| Токсикологические данные
|
| LD50
| тригидрат: 940 мг/кг
|
| Структура
|
| Кристаллическая решётка
| безводный: ромбическая; тригидрат: ромбическая; гексагидрат: триклинная; 1,5- и 2,5-гидраты: моноклинная
|
| Термодинамические свойства
|
| Стандартная энтальпия образования
| безводный: −310 кДж/моль; тригидрат: −1217 кДж/моль
|
| Стандартная молярная энтропия
| +192 Дж/(К·моль)
|
| Стандартная энергия образования Гиббса
| −117 кДж/моль
|
| |
|
| |
|
Нитра́т ме́ди(II) — неорганическое вещество с формулой Cu(NO3)2, является солью двухвалентной меди и азотной кислоты. Безводный нитрат меди(II) представляет собой бесцветные гигроскопичные кристаллы. При поглощении влаги образует кристаллогидраты голубого цвета.
Получение
2,5г металлической меди облить в колбе (под тягой) 22,5г 30% азотной кислоты и слегка подогреть смесь на плитке. Когда выделение оксидов азота ослабеет, то нужно усилить нагревание до растворения меди. По окончанию растворения разбавляют жидкость равным объемом дистиллированной воды, фильтруют и, выпарив до появления кристаллической пленки, дают охладиться.
Выпавшие кристаллы отжимают между листами фильтровальной бумаги и, быстро высушив в теплом месте, помещают в банку с хорошо притертой пробкой.





