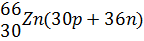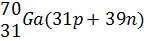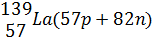Структура атома. Изотопы. Изотоны. Изобары. ПЕНЗЕНСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ
Кафедра «Химия»
«УТВЕРЖДАЮ»
Заведующий кафедрой «Химия»
Профессор, д.т.н. Ю.Перелыгин
«____»______________ 2012 г.
К началу XX века было установлено, что атом не является неделимым, как считали раньше, а представляет собой сложную систему. Было показано, что атом состоит из положительно заряженного ядра и движущихся вокруг него отрицательно заряженных электронов. Положительный заряд ядра компенсируется суммарным отрицательным зарядом электронов, так что атом, в целом, электронейтрален. Согласно современным представлениям, атомные ядра состоят из элементарных частиц: протонов и нейтронов. В ядре сосредоточена почти вся атомная масса, так как масса электронов в сравнении с массами протонов и нейтронов пренебрежимо мала. Таблица 1
Сумма числа протонов и нейтронов, содержащихся в ядре атома, называется массовым числом атома А. Так как массы протонов и нейтронов примерно равны единице, а вся масса атома сосредоточена в ядре, то и массовое число атома приближенно равно его относительной атомной массе Аr: Число протонов в ядре определяет величину положительного заряда ядра, чему соответствует порядковый номер элемента Z. Порядковый номер и массовое число атома условились проставлять слева от индекса элемента: порядковый номер – снизу, массовое число – сверху, например, Элементы, у которых ядра содержат одинаковое число протонов и разное число нейтронов, то есть, у которых порядковый номер одинаков, а массовые числа различны, называют изотопами (см. табл.2). Еще примеры изотопов: Элементы, у которых ядра содержат разное число протонов и одинаковое суммарное число протонов и нейтронов, то есть у которых порядковые номера различаются, а массовые числа одинаковы, называются изобарами (табл.2). Элементы, у которых ядра содержат одинаковое число нейтронов и разное число протонов, называются изотонами (табл.2). Таблица.2
|


 1
1