Вероятность нахождения электрона в пространстве. Квантовые числаТаким образом, можно говорить только о вероятности нахождения электрона в данной части пространства. В связи с этим в квантовой механике состояние микрочастицы полностью описывается не ее координатой и скоростью, а некоторой функцией. Эта математическая величина называется волновой функцией или орбиталью и обозначается греческой буквой «пси» ψ. Физический смысл имеет не сама волновая функция, а только произведение квадрата ее модуля на элементарный объем Часть пространства, где наиболее вероятно нахождение электрона, называется электронным облаком. В 1927 г. австрийский физик Шрёдингер выводит уравнение, связывающее волновую функцию с потенциальной и полной энергией электрона. Не вдаваясь в анализ уравнения Шрёдингера, укажем, лишь, что решить его – значит найти удовлетворяющую ему волновую функцию ψ. С точки зрения квантово-механической модели атома главное квантовое число можно определить следующим образом. 3.1. Главное квантовое число n характеризует размеры электронного облака и общий уровень энергии электрона в атоме. n = 1, 2, 3, 4, 5, 6, 7 K, L, N, O, P, Q. Состояние электрона в атоме, которое характеризуется определенным значением главного квантового числа n, называется энергетическим уровнем. 3.2. Орбитальное квантовое число l характеризует форму электронного облака. s – облако p – облако d –облако f – облако имеет более сложную
l = 0 l = 1 l = 2 l = 3 На первом энергетическом уровне могут находиться только s – облака. Иными словами, если n = 1, l = 0; если n = 2, l = 0, 1; если n = 3, l = 0, 1, 2; если n = 4, l = 0, 1, 2, 3, ⇒ Состояние электрона, которое характеризуется определенным значением l, называется энергетическим подуровнем. 3.3. Магнитное квантовое число
Любые возможные расположения s – облака в пространстве идентичны, поэтому s – состоянию соответствует единственное значение магнитного квантового числа
p- облака могут располагаться в пространстве тремя различными способами, поэтому для p - состояния возможны три различных значения: Для d – состояния возможны пять значений магнитного квантового числа, для f – состояния – семь значений (см. табл.3).
Таблица 3
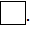
Энергии электронных облаков одного и того же размера и формы, но различным образом ориентированных в пространстве, начинают различаться только при наложении магнитного поля, отсюда и произошло название магнитного квантового числа. Состояние электрона в атоме, характеризующееся определенными значениями s, l и Графически орбиталь обозначается следующим образом: 3.4 Спиновое квантовое число
Вышеуказанными четырьмя квантовыми числами можно полностью охарактеризовать всю совокупность сложных движений электрона в атоме. Однако заполнение электронами орбиталей происходит не беспорядочно, а в соответствии с определенными принципами.
|

 равное вероятности нахождения электрона в элементарном объеме
равное вероятности нахождения электрона в элементарном объеме 
 .
. характеризует ориентацию электронного облака в пространстве.
характеризует ориентацию электронного облака в пространстве.



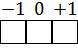



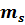 характеризует вращение электрона вокруг собственной оси (spin – волчок, юла). Более правильно говорить, что
характеризует вращение электрона вокруг собственной оси (spin – волчок, юла). Более правильно говорить, что  характеризует собственный магнитный момент электрона.
характеризует собственный магнитный момент электрона. и
и ).
).


