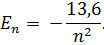Постулаты Бора1. Электрон вращается вокруг ядра, не излучая и не поглощая энергии, по строго определенным стационарным орбитам, удовлетворяющим теорию квантов.. На каждой из этих орбит электрон обладает определенной энергией. Чем дальше от ядра расположена орбита, тем большей энергией обладает находящийся на ней электрон. 2. При переходе электрона с одной стационарной орбиты на другу атом излучает или поглощает энергию в виде светового кванта. Для случая испускания энергии:
где Теория Бора позволила объяснить механизм образования оптического спектра. При переходе электрона с дальних энергетических уровней не один и тот же ближайший возникает спектральная серия. Одной линии соответствует отдельный переход электрона на данный уровень. Описывая движение электронов в атоме по стационарным орбитам, Бор эти орбиты пронумеровал. Ближайшая к ядру орбита получила порядковый номер 1, следующая - 2 и т. д. Эти порядковые номера были названы главными квантовыми числами. Нильс Бор, используя вышеперечисленные постулаты, вывел формулы для радиусов стационарных орбит и энергии стационарных орбит, куда входили главные квантовые числа n:
где
Отрицательный знак энергии означал устойчивость системы, которая тем более устойчива, чем ниже, то есть, чем более отрицательна ее энергия. Итак, согласно Бору, главное квантовое число n определяло:1) номер электронной орбиты; 2) радиус электронной орбиты; 3) энергию электрона на данной стационарной орбите. Однако впоследствии появились работы, в которых утверждалось, что электрон нельзя представлять в виде материальной частицы, движущейся по строго определенным орбитам, так как и орбит в нашем обыденном понимании в атоме не существует. Возникла необходимость в более совершенной модели атома, основанной на новых открытиях в микромире.
|


 – частота излучения светового кванта,
– частота излучения светового кванта,  - энергия атома при нахождении электрона на более удаленной от ядра орбите,
- энергия атома при нахождении электрона на более удаленной от ядра орбите, 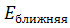 - энергия атома при нахождении электрона на более близкой к ядру орбите.
- энергия атома при нахождении электрона на более близкой к ядру орбите.
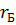 – радиус первой стационарной орбиты, равный
– радиус первой стационарной орбиты, равный