| Тема 11
| ТЕРМОДИНАМИКА
- раздел физики, изучающий свойства физических систем, находящихся в состоянии термодинамического равновесия, и процессы перехода между этими состояниями
|
| Термодинамическая система
| ➨ совокупность макроскопических тел, которые могут взаимодействовать между собой и внешней средой посредством теплообмена.
|
| Макроскопические
параметры
| ➨ величины, характеризующие состояние макроскопических тел без учета молекулярного строения тел (p, V,Т);
|
| Тепловое
равновесие
(термодинамическое равновесие)
| ➨ состояние термодинамической системы, к которому она самопроизвольно приходит через достаточно большой промежуток времени в условиях изоляции от окружающей среды;
➨ при тепловом равновесии прекращаются все виды теплообмена, температура составляющих термодинамической системы одинакова;
|
| Теплообмен
(теплопередача)
| ➨ процесс передачи энергии от одного тела к другому без совершения работы. Энергия передается от более нагретых тел к менее нагретым.
Виды теплообмена:
‒ конвекция,
‒ теплопроводност ь,
‒ тепловое излучение.
|
| ● конвекция
| ➨ перенос энергии потоками жидкости или газа;
|
| ● теплопроводность
| ➨ непосредственный обмен энергией между хаотически движущимися частицами взаимодействующих тел или частей одного и того же тела;
|
| ● тепловое излучение
| ➨ электромагнитное излучение, испускаемое веществом за счет расхода собственной внутренней энергии;
➨ тепловое излучение присуще газам, жидкостям и твердым телам;
|
| ТЕМПЕРАТУРА
| ➨ физическая величина, которая характеризует степень нагретости тела;
|
| ● с точки зрения ТД
| ➨ температура является величиной, характеризующей направление теплообмена;
|
| ● с точки зрения МКТ
| ➨ температура есть величина, характеризующая среднюю кинетическую энергию поступательного движения молекул идеального газа;
|
| ● абсолютный
нуль температуры
| ➨ температура, при которой прекращается поступательное движение молекул;
➨ температура абсолютного нуля равна - 273 С;
|
| Измерение
температуры
| ➨ прибор для измерения температуры посредством контакта с исследуемой средой; снабжен шкалой температур для отсчета показаний; в устройстве использовано свойство тел изменять объем при нагревании или охлаждении.
|
| ● термометр
|
| Термометрическая
величина
| ➨ физическая величина, служащая индикатором температуры.
Например, в спиртовом термометре:
термометрическое тело - спирт;
термометрическая величина -объем спирта;
|
| ТЕМПЕРАТУРНЫЕ
ШКАЛЫ
| ➨ системы сопоставимых значений температуры, представляющие собой конкретную функциональную числовую связь температуры со значениями измеряемого термометрического свойства;
|
● шкала Цельсия
t [0С]

| ➨ температурная шкала, в которой базовыми точками были приняты:
 - температура таяния льда; - температура таяния льда;
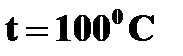 - температура кипения воды;
➨ интервал между этими значениями разделен на 100 равных частей, названных градусами Цельсия (0С), обозначается буквой t;
➨ в 1742 г. предложил шведский ученый А. Цельсий; шкала широко используется в настоящее время во всем мире; - температура кипения воды;
➨ интервал между этими значениями разделен на 100 равных частей, названных градусами Цельсия (0С), обозначается буквой t;
➨ в 1742 г. предложил шведский ученый А. Цельсий; шкала широко используется в настоящее время во всем мире;
|
| ● шкала Кельвина
T [К]
Т = t0C + 273 К
| ➨ абсолютная шкала температур; шкала разделена на 100 равных частей;
➨ величина градуса этой шкалы равна градусу шкалы Цельсия - (10С = 1К) и называется Кельвин (К); обозначается буквой Т;
 = 273 К; = 273 К;
 = 373 К;
0 К = -273 С.
➨ в 1848 г. шкала была предложена английским физиком У. Томсоном (лордом Кельвином). = 373 К;
0 К = -273 С.
➨ в 1848 г. шкала была предложена английским физиком У. Томсоном (лордом Кельвином).
|
● шкала Фаренгейта
tФ [0F]
| ➨ температурная шкала, в которой интервал между точками таяния льда и кипения воды разделен на 180 частей – градусов Фаренгейта (0F);
точке таяния льда присвоено значение 320F,
точке кипения воды 212 0F; обозначается tФ.
➨ в 1724 г. шкала предложена немецким физиком Д.Г. Фаренгейтом, традиционно применяется в ряде стран (в частности, в США, в Англии).
➨ Например, по Фаренгейту нормальная температура человеческого тела 980 F;
|
● шкала Реомюра
tR [0R]
 10R = 1,250С 10R = 1,250С
| ➨ температурная шкала, единицей которой являлся градус Реомюра (0R), равный 1/80 части температурного интервала между точками таяния льда (00 R) и кипения воды (800 R).
➨ в 1730 г. шкала предложена французским ученым Р.А. Реомюром. В России шкала использовалась до 1930 г., в настоящее время практически вышла из употребления;
|
| ВНУТРЕННЯЯ
ЭНЕРГИЯ
U [Дж]
| ➨ сумма кинетической энергии теплового движения молекул (атомов) и потенциальной энергии их взаимодействия;
|
● внутренняя энергия
одноатомного
идеального газа

| ➨ равна сумме средних кинетических энергий поступательного движения молекул, составляющих газ
 (
(  ; ;  ) )
|
● изменение
внутренней энергии

| ➨ в ТД процессе изменение внутренней энергии идеального газа определяется только изменением его температуры и не зависит от характера этого процесса.
|
| ● cпособы изменения
внутренней энергии
| ➨ 1) теплообмен (нагревание или охлаждение газа);
2) совершение работы (сжатие или
расширение газа);
|
| КОЛИЧЕСТВО
ТЕПЛОТЫ
Q [Дж]
| ➨ мера изменения внутренней энергии тел при теплообмене;
➨ калория – внесистемная единица количества теплоты
1 кал = 4,1868 Дж;
1 ккал = 4186,8 Дж
|
● теплоемкость
вещества
 
| ➨ физическая величина, численно равная количеству теплоты Q, которое необходимо сообщить телу для нагревания его на один градус
(10С или 1 К)
|
● удельная
теплоемкость
вещества
 
| ➨ количество теплоты Q, подводимое к веществу массой 1 кг для изменения его температуры на один градус (10С или 1 К);
➨одно и то же вещество, находящееся в разных агрегатных состояниях, имеет разную удельную теплоемкость;
Например, сльда = 2100 Дж/кг·К;
своды = 4200 Дж/кг·К
|
● теплота
нагревания  охлаждения
охлаждения

| ► с – удельная теплоемкость вещества;
 - масса вещества;
► формула справедлива в пределах одного агрегатного состояния вещества; - масса вещества;
► формула справедлива в пределах одного агрегатного состояния вещества;
|
● молярная
теплоемкость
 
| ➨ количество теплоты, подводимое к одному молю вещества для изменения его температуры на один градус (10С или 1 К);
|
● закон сохранения
количества теплоты
уравнение
теплового баланса
 
| ➨ в процессе теплообмена количество теплоты , отдаваемое телами с более высокой температурой, равно количеству теплоты , отдаваемое телами с более высокой температурой, равно количеству теплоты  , которое получают тела с более низкой температурой; , которое получают тела с более низкой температурой;
|
● пример уравнения
теплового баланса
с1m1(T1-  ) =
= с2m2( ) =
= с2m2( -T2) -T2)
| ➨ описывает состояние теплового равновесия двух тел с удельной теплоемкостью, массой и начальной температурой с1,m1,T1 и с2,m2,T2 соответственно и установившейся промежуточной общей температурой  (Т1> (Т1>  >Т2); >Т2);
|
РАБОТА
в термодинамике
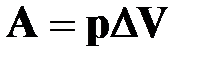

| ➨ находящийся в сосуде газ оказывает на поршень площадью S давление р=F/S, под действие которого поршень перемещается на расстояние  , изменяя объем газа на , изменяя объем газа на  и совершая работу и совершая работу  ; ;
|
● знак работы



|
 работа положительная при расширении газа работа положительная при расширении газа  ; ;
 работа отрицательная при сжатии газа работа отрицательная при сжатии газа  ; ;
 работа равна нулю, если объем газа не изменялся работа равна нулю, если объем газа не изменялся  с течением времени; с течением времени;
|
| Работа в изопроцессах
|
| ● изотермический
процесс
|
➨ или или 
|
| ● изобарный
процесс
|
➨ 
|
| ● изохорный
процесс
| ➨ А=0
|
| Графическое
изображение
работы
| 
|
| ЛЕКЦИЯ 9
|
| Закон сохранения энергии в тепловых процессах
| ➨ во всех процессах, происходящих в природе, энергия не исчезает и не создается, а переходит от одного тела к другому и превращается из одного вида в другой в эквивалентных количествах;
|
ПЕРВЫЙ ЗАКОН
термодинамики

| ➨ количество теплоты Q, сообщенное термодинамической системе, расходуется на изменение внутренней энергии ΔUсистемы и на совершение системой механической работы A;
|
| ● вечный двигатель
первого рода
| ➨ нельзя построить периодически действующий двигатель, который совершал бы работу большую, чем та энергия, которая подводится к двигателю извне.
|
| Применение первого закона ТД к изопроцессам
|
● изотермический
процесс

|
➨  = = или Q= или Q= 
|
● изобарный
процесс
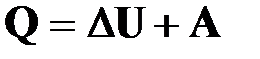
| ➨    

|
● изохорный
процесс 
|
➨  
|
● адиабатный
процесс 
|
➨    
|
| Необратимость
тепловых
процессов
| ➨ необратимыми называются такие процессы, которые могут самопроизвольно протекать только в одном направлении – от горячего тела к холодному; в обратном направлении они могут протекать только как одно из звеньев более сложного процесса.
Все реальные процессы – необратимые, протекают с невосполнимой потерей энергии на нагрев окружающей среды, преодоление сил трения.
|
| ВТОРОЙ ЗАКОН
термодинамики
| ➨ исторически открытие второго закона ТД было связано с изучением вопроса о максимальном КПД тепловых машин, проведенным французским ученым С. Карно. Позднее Клаузиус и Кельвин предложили различные по виду, но эквивалентные формулировки второго закона ТД;
|
| ● формулировка
Клаузиуса
| ➨ невозможен круговой процесс, единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому;
|
| ● формулировка Кельвина
| ➨ невозможен круговой процесс, единственным результатом которого является превращение теплоты, полученной от нагревателя, в эквивалентную ей работу;
|
| ● вечный двигатель
второго рода
| ➨ невозможно построить периодически действующую машину, которая целиком превращала бы в работу теплоту, извлекаемую из окружающих тел (океана, атм. воздуха);
|
| Статистическое
обоснование второго
закона ТД
| ➨ второй закон термодинамики является статистическим законом и описывает закономерности хаотического движения большого числа частиц, составляющих замкнутую систему;
|
Круговой процесс
(цикл)

| ➨ термодинамический процесс, в результате совершения которого рабочее тело возвращается в исходное состояние;
➨ на диаграммах состояния p-V, p-T и др. изображаются в виде замкнутых кривых;
➨ круговые процессы являются физической основой работы тепловых двигателей;
|
| ● прямой цикл
| ➨ круговой процесс, в котором рабочее тело совершает положительную работу за счет сообщенной ему теплоты;
➨ на диаграмме прямой цикл изображен замкнутой кривой, которая обходится по часовой стрелке ( ); );
|
| ● обратный цикл
| ➨ круговой процесс, в котором рабочее тело совершает отрицательную работу, т.е. над рабочим телом совершается и от него отводится равное количество теплоты;
➨ на диаграмме обратный цикл изображен замкнутой кривой, которая обходится против часовой стрелки ( ); );
|
| Тепловой двигатель
| ➨ периодически действующая машина, совершающая механическую работу за счет получаемого извне количества теплоты;
➨ периодичность заключается в многократном повторении одного и того же рабочего цикла – после расширения следует сжатие газа;
➨ реальные тепловые двигатели работают по разомкнутому циклу: после расширения газ выбрасывается и сжимается новая порция; цикл может быть замкнутый, тогда расширяется и сжимается одна и та же порция газа;
|
● устройство теплового
 двигателя двигателя
| ➨ Рабочее тело - газ или пар – при расширении совершает работу.
Нагреватель имеет температуру Тни передает количество теплоты Qнрабочему телу.
При сжатии рабочее тело передает холодильнику количество теплоты Qх; температура холодильника Тх меньше температуры нагревателя Тн; роль холодильника часто играет атмосфера.
Из закона сохранения энергии следует, что работа, совершаемая тепловой машиной за один цикл, равна
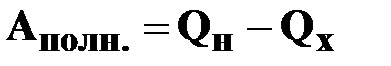
|
● КПД
теплового двигателя

| ➨ отношение работы А,совершенной тепловым двигателем, к количеству теплоты Qн, полученному от нагревателя;
|
| ● идеальный тепловой
двигатель
| ➨ двигатель, не имеющий потерь на механическое трение и работающий по особому круговому циклу, называемому циклом Карно;
|
 Цикл Карно
Изотермы - 1-2; 3-4
Адиабаты - 2-3; 4-1 Цикл Карно
Изотермы - 1-2; 3-4
Адиабаты - 2-3; 4-1
| ➨ представляет собой идеализацию цикла реальной тепловой машины; рабочим телом является идеальный газ;
цикл является прямым обратимым круговым процессом, состоящим из двух изотерм и двух адиабат;
➨ ( ) - изотермическое расширение - рабочее тело получает от нагревателя количество теплоты ) - изотермическое расширение - рабочее тело получает от нагревателя количество теплоты  ;
➨ ( ;
➨ ( ) - изотермическое сжатие - рабочее тело отдает холодильнику количество теплоты ) - изотермическое сжатие - рабочее тело отдает холодильнику количество теплоты  ;
➨ при адиабатном расширении и сжатии, энергия извне к рабочему телу не поступает и эти процессы происходят за счет изменения его внутренней энергии; ;
➨ при адиабатном расширении и сжатии, энергия извне к рабочему телу не поступает и эти процессы происходят за счет изменения его внутренней энергии;
|
КПД идеального
теплового двигателя

| ➨ увеличение КПД зависит от разности между температурами нагревателя Тн и холодильника Тх и не зависит от свойств рабочего тела и конструкции двигателя;
|
| Основные виды
тепловых двигателей
| ➨ по способам получения механического движения подразделяются на:
|
| ● поршневые
| ➨ паровые машины (КПД до 20%);
➨ двигатели внутреннего сгорания:
▪ карбюраторные (КПД- 18-24%) – создал в 1867г. Н. Отто, применяются в настоящее время;
▪ дизели (КПД - 30-39%) - создал в 1897г. Р.Дизель, применяются в настоящее время;
|
| ● ротационные
| ➨ паровая (КПД до 43%);
➨ газовая турбина (КПД – до 34%);
|
| ● реактивные
| ➨ ракетные двигатели
➨ воздушно-реактивные
|
(КПД до 42%)
|
| | | | |
| Тема 12
| ЖИДКОСТИ И ТВЕРДЫЕ ТЕЛА
|
| Агрегатные состояния
вещества
| ➨ характеризуются определенной внутренней структурой вещества и его свойствами. Различают три агрегатных состояния: твердое, жидкое, газообразное.
Четвертым агрегатным состоянием вещества считают плазму (ионизированный газ);
|
| · газ
| ➨ вещество летучее (занимающее весь предоставленный ему объем), легкосжимаемое.
|
| · жидкость
| ➨ вещество, которое, имея определенный объем, принимает форму сосуда, в котором оно находится; трудно сжимаемое.
|
| · твердое тело
| ➨ вещества, которые способны длительное время сохранять свои форму и объем без воздействия внешних сил.
Различают: кристаллические и аморфные тела.
|
| Изменения агрегатного
состояния вещества
| 
|
ЖИДКОСТЬ  ГАЗ ГАЗ
|
| Парообразование
| ➨ явление перехода твердого или жидкого вещества в пар;
|
| твердого вещества
| - сублимация (возгонка);
|
| жидкого вещества
| - испарение, кипение;
|
Сублимация (возгонка)
(твердое тело  пар) пар)
| ➨ переход вещества из твердого состояния в газообразное, минуя жидкое.
Примеры: бром, йод, нафталин, «сухой лед».
|
Испарение
(жидкость  пар) пар)
| ➨ процесс парообразования, происходящий с открытой поверхности жидкости.
Испарение зависит от:
1) рода жидкости; 2) температуры;
3) площади свободной поверхности;
4) внешнего давления; 5) скорости удаления молекул от поверхности жидкости.
|
Конденсация
(пар 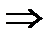 жидкость) жидкость)
| ➨ переход вещества из газообразного состояния в жидкое.
|
| В результате хаотического движения над поверхностью жидкости молекулы пара, попадая в сферу действия молекулярных сил, вновь возвращаются в жидкость.
|
| Пар
| ➨ совокупность молекул, вылетающих из жидкости.
|
| · насыщенный пар
| ➨ пар, находящийся в динамическом равновесии со своей жидкостью.
|
| ● динамическое равновесие
| ➨ равенство числа молекул, покинувших жидкость при испарении и вернувшихся в нее при конденсации.
|
| · ненасыщенный пар
| ➨ пар, не находящийся в динамическом равновесии со своей жидкостью (процесс испарения преобладает над процессом конденсации).
|
| Влажность воздуха
| ➨ характеризует наличие водяного пара в воздухе.
Различают: абсолютную и
относительную влажность воздуха.
|
● абсолютная влажность
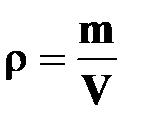 
| ➨ физическая величина, показывающая, какая масса паров воды находится в 1 м3 воздуха и равная отношению массы m водяного пара к объему воздуха V,в котором он находится;
➨ абсолютная влажность определяется либо плотностью  водяного пара в воздухе, либо парциальным давлением водяных паров, находящихся в воздухе водяного пара в воздухе, либо парциальным давлением водяных паров, находящихся в воздухе
|
● относительная влажность
  или
или
 
| ➨ физическая величина, характеризующая степень насыщения воздуха паром;
➨ равнаотношению абсолютной влажности  к плотности к плотности  насыщенного водяного пара при данной температуре, выраженное в процентах
или
➨ равна отношению давления р водяного пара, содержащегося в воздухе при данной температуре, к давлению р0 насыщенного пара при той же температуре, выраженное в процентах.
При понижении температуры относительная влажность увеличивается. насыщенного водяного пара при данной температуре, выраженное в процентах
или
➨ равна отношению давления р водяного пара, содержащегося в воздухе при данной температуре, к давлению р0 насыщенного пара при той же температуре, выраженное в процентах.
При понижении температуры относительная влажность увеличивается.
|
| ● точка росы
| ➨температура 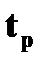 , при которой относительная влажность становится равной 100%.
При этой температуре в воздухе и соприкасающихся с ним предметах наблюдается конденсация водяных паров (выпадает роса). , при которой относительная влажность становится равной 100%.
При этой температуре в воздухе и соприкасающихся с ним предметах наблюдается конденсация водяных паров (выпадает роса).
|
| · приборы для
измерения влажности
| ➨ гигрометр, психрометр;
|
| Кипение жидкости
| ➨ парообразование, происходящее одновременно с поверхности и по всему объему жидкости при постоянной температуре.
С повышением внешнего давления температура кипения повышается, а с понижением давления – температура кипения понижается.
|
● теплота парообразования
 конденсации
конденсации
 [Дж] [Дж]
| ➨ теплота парообразования и теплота конденсации численно равны произведению удельной теплоты парообра-зования вещества 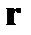 на его массу на его массу  . .
|
● удельная теплота
парообразования
 
| ➨ количество теплоты, необходимое для превращения при постоянной температуре 1 кг жидкости в пар.
|
ЖИДКОСТЬ  ТВЕРДОЕ ТЕЛО ТВЕРДОЕ ТЕЛО
|
| Плавление
твердых тел
| ➨ процесс перехода вещества из твердого состояния в жидкое, происходящий при определенной температуре с поглощением теплоты.
|
| Затвердевание
(кристаллизация)
твердых тел
| ➨ процесс перехода вещества из жидкого состояния в твердое, происходящий при определенной температуре с выделением теплоты.
|
● теплота плавления
 затвердевания
(кристаллизации)
затвердевания
(кристаллизации)
 [Дж] [Дж]
| ➨ теплота плавления и теплота кристаллизации численно равны произведению удельной теплоты плавления тела  на его массу на его массу  . .
|
● удельная теплота
плавления
 Дж/кг] Дж/кг]
|
| ➨ количество теплоты, необходимое для превращения 1 кг твердого вещества при температуре плавления в жидкость той же температуры.
|
· теплота, выделяющаяся
при сгорании топлива
 [Дж] [Дж]
| ➨ теплота, выделяющаяся при сгорании топлива, равна произведению удельной теплоты сгорания топлива  на массу вещества на массу вещества  ; ;
|
· удельная теплота
сгорания топлива
 Дж/кг] Дж/кг]
|
| ➨ количество теплоты, которое выделяет 1 кг топлива при полном его сгорании;
|
Кристаллические
тела
 все металлы,
графит,
алмаз,
кварц,
лед все металлы,
графит,
алмаз,
кварц,
лед
| ➨ твердые тела, состоящие из молекул (атомов, ионов), которые образуют строго упорядоченную структуру – кристаллическую решетку, связаны между собой силами межмолекулярного взаимодействия, расположены в узлах кристаллической решетки и совершают хаотичные колебаний вокруг положения равновесия;
➨ правильную геометрическую форму; периодически повторяющуюся внутреннюю структуру во всем объеме; обладают анизотропией.
|
| ● анизотротия
| ➨ зависимость физических свойств от направления внутри кристалла;
|
| ● изотропность
| ➨ физические свойства одинаковы по всем направлениям;
|
| ● монокристаллы
| ➨ кристаллическое твердое тело, представляющее собой один кристалл.
|
| ● поликристаллы
| ➨ твердые тела, состоящие из множества сросшихся монокристаллов; каждый маленький монокристалл анизотропен, а поликристалл – изотропен;
➨ поликристаллическое строение имеют большинство твердых тел (минералы, сплавы, керамика);
|
| Аморфные тела
смола,
янтарь,
стекло,
битум,
пластмассы
| ➨ не имеют строгой кристаллической решетки, атомы вещества хаотично расположены и совершают колебания вокруг положения равновесия; занимают промежуточное положение между кристаллическими твердыми телами и жидкостями; пластичны; не имеют определенной температуры плавления (затвердевания); изотропны.
|
| | | | | | | |
1. Григорьев, В.И. Силы в природе / В.И. Григорьев, Г.Я. Мякишев. – М.: Наука, 1983.
2. Иванов, Б.Н. Законы физики: уч. пособие для вузов. – М.: Высш. шк, 1986.
3. Ильин, В.А. История физики. Учебное пособие. М.: Издательский центр «Академия», 2003.
4. Платунов Е.С.Физика. Словарь-справочник / Е.С. Платунов, В.А. Самолетов, С.Е. Буравой. - СПб: Питер, 2005.
5. Савельев И.В. Курс общей физики. т.3. М.: Наука,1985.
6. Трофимова Т.И. Курс физики. М.: Высш.шк., 1985.
7. Физический энциклопедический словарь./Глав.ред. А.М. Прохоров-М.: Сов. энциклопедия, 1983.
8. Физическая энциклопедия: т.1-3.- М.: Изд-во Сов. Энциклопедия, 1988.
9. Яворский Б.М. Справочник по физике / Б.М. Яворский,
А.А. Детлаф. - М.: Наука, 1981.


 - температура таяния льда;
- температура таяния льда;
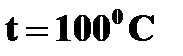 - температура кипения воды;
➨ интервал между этими значениями разделен на 100 равных частей, названных градусами Цельсия (0С), обозначается буквой t;
➨ в 1742 г. предложил шведский ученый А. Цельсий; шкала широко используется в настоящее время во всем мире;
- температура кипения воды;
➨ интервал между этими значениями разделен на 100 равных частей, названных градусами Цельсия (0С), обозначается буквой t;
➨ в 1742 г. предложил шведский ученый А. Цельсий; шкала широко используется в настоящее время во всем мире;
 = 273 К;
= 273 К;
 = 373 К;
0 К = -273 С.
➨ в 1848 г. шкала была предложена английским физиком У. Томсоном (лордом Кельвином).
= 373 К;
0 К = -273 С.
➨ в 1848 г. шкала была предложена английским физиком У. Томсоном (лордом Кельвином).

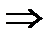




 (
(
 ;
;  )
)





 охлаждения
охлаждения

 - масса вещества;
► формула справедлива в пределах одного агрегатного состояния вещества;
- масса вещества;
► формула справедлива в пределах одного агрегатного состояния вещества;




 , отдаваемое телами с более высокой температурой, равно количеству теплоты
, отдаваемое телами с более высокой температурой, равно количеству теплоты  , которое получают тела с более низкой температурой;
, которое получают тела с более низкой температурой;
 ) =
= с2m2(
) =
= с2m2(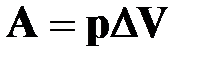

 , изменяя объем газа на
, изменяя объем газа на  и совершая работу
и совершая работу  ;
;



 ;
;
 ;
;
 с течением времени;
с течением времени;
 или
или 




 =
= или Q=
или Q= 
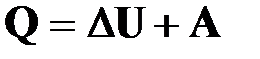












 );
);
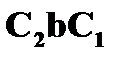 );
);
 двигателя
двигателя
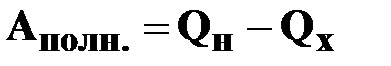

 Цикл Карно
Изотермы - 1-2; 3-4
Адиабаты - 2-3; 4-1
Цикл Карно
Изотермы - 1-2; 3-4
Адиабаты - 2-3; 4-1
 ) - изотермическое расширение - рабочее тело получает от нагревателя количество теплоты
) - изотермическое расширение - рабочее тело получает от нагревателя количество теплоты  ;
➨ (
;
➨ ( ) - изотермическое сжатие - рабочее тело отдает холодильнику количество теплоты
) - изотермическое сжатие - рабочее тело отдает холодильнику количество теплоты  ;
➨ при адиабатном расширении и сжатии, энергия извне к рабочему телу не поступает и эти процессы происходят за счет изменения его внутренней энергии;
;
➨ при адиабатном расширении и сжатии, энергия извне к рабочему телу не поступает и эти процессы происходят за счет изменения его внутренней энергии;


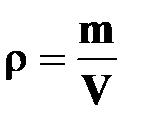

 водяного пара в воздухе, либо парциальным давлением водяных паров, находящихся в воздухе
водяного пара в воздухе, либо парциальным давлением водяных паров, находящихся в воздухе

 или
или

 насыщенного водяного пара при данной температуре, выраженное в процентах
или
➨ равна отношению давления р водяного пара, содержащегося в воздухе при данной температуре, к давлению р0 насыщенного пара при той же температуре, выраженное в процентах.
При понижении температуры относительная влажность увеличивается.
насыщенного водяного пара при данной температуре, выраженное в процентах
или
➨ равна отношению давления р водяного пара, содержащегося в воздухе при данной температуре, к давлению р0 насыщенного пара при той же температуре, выраженное в процентах.
При понижении температуры относительная влажность увеличивается.
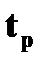 , при которой относительная влажность становится равной 100%.
При этой температуре в воздухе и соприкасающихся с ним предметах наблюдается конденсация водяных паров (выпадает роса).
, при которой относительная влажность становится равной 100%.
При этой температуре в воздухе и соприкасающихся с ним предметах наблюдается конденсация водяных паров (выпадает роса).
 [Дж]
[Дж]
 на его массу
на его массу  .
.


 [Дж]
[Дж]
 на его массу
на его массу  .
.
 Дж/кг]
Дж/кг]
 [Дж]
[Дж]
 на массу вещества
на массу вещества  ;
;
 Дж/кг]
Дж/кг]
 все металлы,
графит,
алмаз,
кварц,
лед
все металлы,
графит,
алмаз,
кварц,
лед



