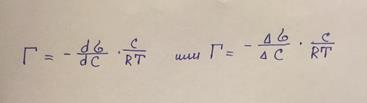Билет №3Изотерма адсорбции Гиббса, ее анализ. Теория Ленгмюра. Изотерма адсорбции – графическая зависимость величины удельной адсорбции (Г) от концентрации растворенного вещества или парциального давления газа либо пара при постоянной температуре.
Адсорбция положительна – вещество накапливается на поверхности фаз) характерно для ПАВ. Адсорбция отрицательна – вещество накапливается в обьеме, характерно для ПИВ. Теория Ленгмюра: 1)адсорбция молекул происходит не на всей поверхности адсорбента, а только на адсорбционных (активных) центрах, где имеются участки с нескомпансированными силовыми поясами.
2)каждый адсорбирующий центр может удерживать только 1 молекулу адсорбита при этом адсорбирующие молекулы не взаимодействуют со свободными молекулами, что и приводит к образованию мономолекулярного слоя поглощаемого вещества. Экзергонические и эндергонические процессы, протекающие в организме. Принцип энергетического сопротивления. Экзергонические реакции – G<0 и системой совершается работа (гидролиз АТФ) АТФ + Н2О=АДФ +Ф дельтаG>0 Эндергонические реакции – G>0 и над системой совершается работа (фосфорилирование глюкозы) Глюкоза +Ф= глюкоза-6-фосфат +Н2О дельтаG=3kкал/моль Принцип энергетического сопряжения: 1)Эндергоническая реакция осуществляется совместно и одновременно с экзергонической. 2)Абсолютное значение изменения свободной энергии для экзергонической реакции должно быть больше, чем для эндергонической. 3)Экзергоническая и эндергоническая реакция должны иметь общий промежуточный продукт.
|