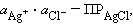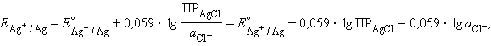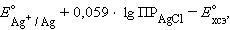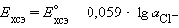А) Электронообменные электроды
1) Окислительно-восстановительные электроды состоят из электрохимически инертного проводника (платины, графита и т. д.), погруженного в раствор, в котором находятся окисленная и восстановленная формы потенциалопределяющего вещества. Такой инертный проводник способствует передаче электронов от восстановителя к окислителю через внешнюю цепь. Примерами таких электродов могут служить редокс-электроды с ионами в различных степенях окисления: (Pt)Sn4+, Sn2+, (Pt)Fe3+, Fe2+. Уравнение Нернста при 298 К:
2) Электроды первого рода - электроды, находящиеся в равновесии с катионами, одноименными с металлом, и обратимые по отношению к ним. Простейший электронообменный электрод - металлическая пластинка, погруженная в раствор или расплав электролита Zn/Zn2+; Cu/Cu2+ и т. д. Уравнение Нернста для электрода первого рода при 298 К
3) Электроды второго рода представляют собой металлические электроды, покрытые слоем труднорастворимой соли того же металла. При погружении в раствор соли одноименного аниона его потенциал будет определяться активностью иона в растворе. 3.1.) Хлорсеребряный электрод (ХСЭ) Ag0, AgCl|Cl- представляет собой серебряный проводник, покрытый твердым AgCl, который погружен в насыщенный раствор KCl. Серебро электрохимически взаимодействует со своим ионом: Ag+ + e- = Ag. Уравнение Нернста для этого процесса:
Однако в присутствии труднорастворимого AgCl активность ионов серебра очень мала и ее трудно определить. Но активность ионов Ag+ связана с легко задаваемой в данной системе активностью ионов Cl- произведением растворимости хлорида серебра ПРAgCl:
Откуда:
Подставляя это выражение в (1)
и обозначив
получим уравнение Нернста для хлорсеребряного электрода:
где Е0 ХСЭ = + 1,37425 В
Потенциалопределяющими являются ионы хлора, а электродный процесс может быть представлен уравнением
Именно ХСЭ получили очень широкое распространение в потенциометрии, они обладают многими достоинствами: высокая воспроизводимость, возможность изготовления в малых размерах, применимость в различных средах, водных и неводных растворах. Они используются в цепях без жидкостных соединений. [1, стр. 14] 3.2.) Каломельный электрод (КЭ) Hg|Hg2Cl2|Cl- - это ртуть, находящаяся в контакте с пастой из смеси ртути и каломели Hg2Cl2, которая, в свою очередь, соприкасается с насыщенным раствором KCl. Принцип действия каломельного электрода тот же, что и хлорсеребряного. Электроды второго рода обеспечивают стабильное поддержание электродных потенциалов за счет постоянно большой и неизменной концентрации анионов. Поэтому они применяются как электроды сравнения в потенциометрической ячейке.
|

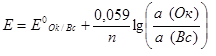
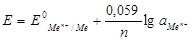
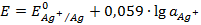 (1)
(1)